
Caractéristiques de l'acide hypobromeux, structure, utilisations

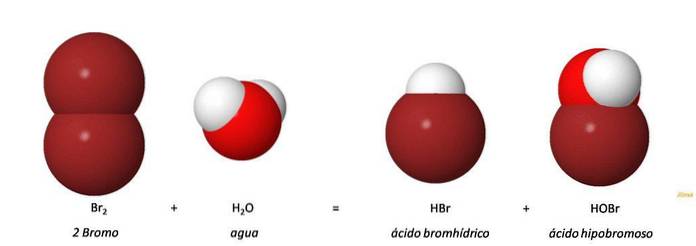
le acide hypobromeux (HOBr, HBrO) est un acide inorganique produit par l'oxydation de l'anion bromure (Br-). L'addition de brome à l'eau donne de l'acide bromhydrique (HBr) et de l'acide hypobromeux (HOBr) par une réaction de disproportionation. Br2 + H2O = HOBr + HBr
L'acide hypobromeux est un acide très faible, quelque peu instable, existant sous forme de solution diluée à température ambiante. Il est produit dans les organismes vertébrés à sang chaud (y compris les humains), par l'action de l'enzyme éosinophile peroxydase.
La découverte que l'acide hypobromeux peut réguler l'activité du collagène IV a attiré beaucoup d'attention..
Index des articles
- 1 Structure
- 1.1 2D
- 1.2 3D
- 2 Propriétés physiques et chimiques
- 3 utilisations
- 4 Interactions biomoléculaires
- 5 Références
Structure
2D
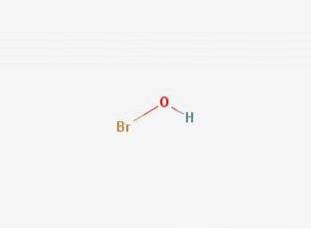
3D

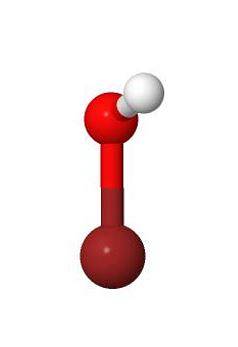
Proprietes physiques et chimiques
- Aspect solides jaunes: solides jaunes.
- Apparence: solides jaunes.
- Poids moléculaire: 96,911 g / mol.
- Point d'ébullition: 20-25 ° C.
- Densité: 2,470 g / cm3.
- Acidité (pKa): 8,65.
- Les propriétés chimiques et physiques de l'acide hypobromeux sont similaires à celles des autres hypohalites..
- Il se présente sous forme de solution diluée à température ambiante.
- Les solides d'hypobromite sont de couleur jaune et ont une odeur aromatique particulière.
- C'est un bactéricide puissant et un désinfectant pour l'eau.
- Il a un pKa de 8,65 et se dissocie partiellement dans l'eau à pH 7.
Applications
- L'acide hypobromeux (HOBr) est utilisé comme agent de blanchiment, oxydant, déodorant et désinfectant, en raison de sa capacité à tuer les cellules de nombreux agents pathogènes.
- Il est utilisé par l'industrie textile comme agent de blanchiment et de séchage.
- Également utilisé dans les spas et les spas comme agent germicide.
Interactions biomoléculaires
Le brome est omniprésent chez les animaux sous forme de bromure ionique (Br-), mais jusqu'à récemment, sa fonction essentielle était inconnue..
Des recherches récentes ont montré que le brome est essentiel pour l'architecture de la membrane basale et le développement des tissus.
L'enzyme peroxydain utilise HOBr pour réticuler la sulfilimine, qui est réticulée dans les échafaudages de collagène IV de la membrane basale..
L'acide hypobrome est produit dans les organismes vertébrés à sang chaud par l'action de l'enzyme éosinophile peroxydase (EPO).
L'EPO génère HOBr à partir de H2O2 et Br- en présence d'une concentration plasmatique de Cl-.
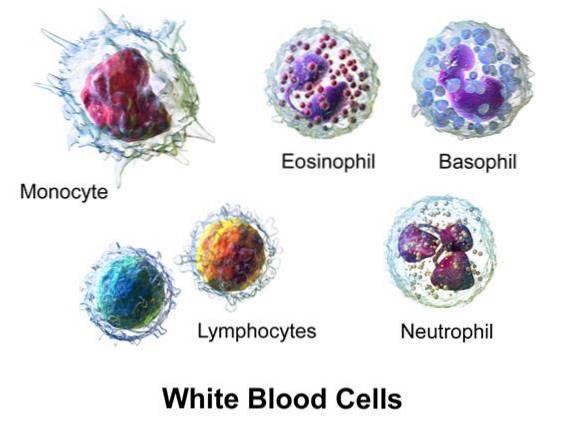
La myéloperoxydase (MPO), à partir de monocytes et de neutrophiles, génère de l'acide hypochloreux (HOCl) à partir de H2O2 et Cl-.
L'EPO et la MPO jouent un rôle important dans les mécanismes de défense de l'hôte contre les agents pathogènes, en utilisant respectivement HOBr et HOCl.
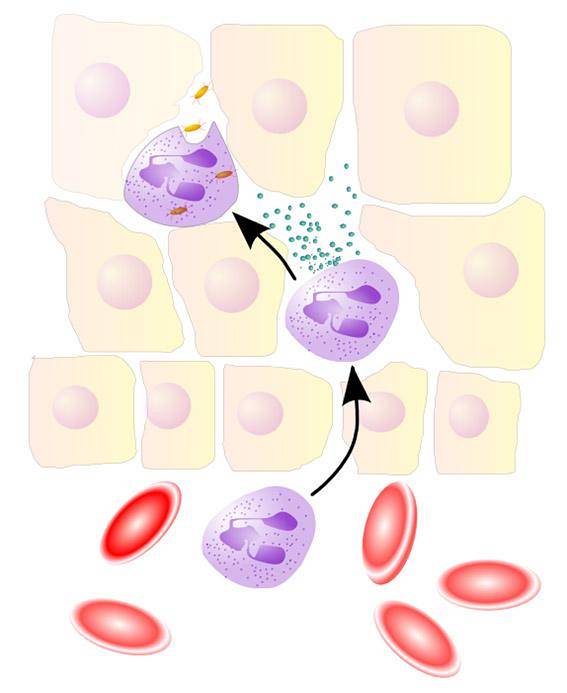
Le système MPO / H2O2 / Cl- en présence de Br- génère également HOBr en faisant réagir le HOCl formé avec Br-. Plus qu'un puissant oxydant, HOBr est un puissant électrophile.
La concentration plasmatique de Br- est plus de 1000 fois inférieure à celle de l'anion chlorure (Cl-). Par conséquent, la production endogène de HOBr est également inférieure à celle de HOCl.
Cependant, HOBr est nettement plus réactif que HOCl lorsque l'oxydabilité des composés étudiés n'est pas pertinente, de sorte que la réactivité de HOBr pourrait être plus associée à sa force électrophile qu'à son pouvoir oxydant (Ximenes, Morgon & de Souza, 2015).
Bien que son potentiel redox soit inférieur à celui de HOCl, HOBr réagit avec les acides aminés plus rapidement que HOCl.
L'halogénation du cycle tyrosine par HOBr est 5000 fois plus rapide que celle de HOCl.
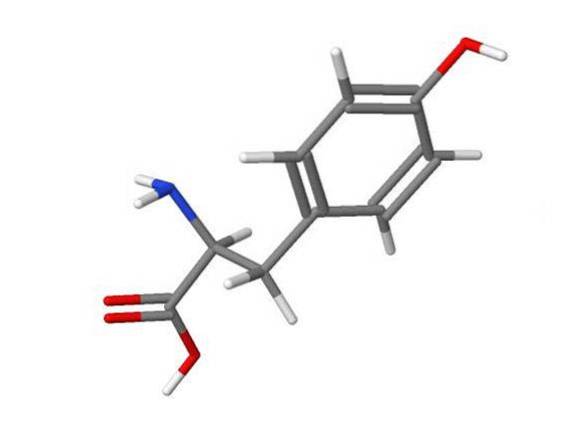
HOBr réagit également avec les nucléosides nucléosidiques et l'ADN.
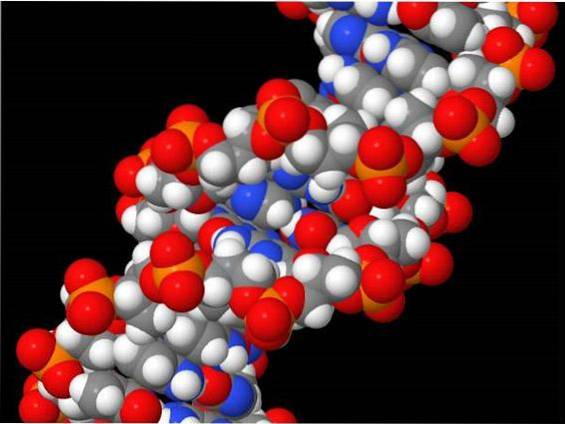
La 2'-désoxycytidine, l'adénine et la guanine génèrent la 5-bromo-2'-désoxycytidine, la 8-bromoadénine et la 8-bromoguanine dans les systèmes EPO / H2O2 / Br- et MPO / H2O2 / Cl- / Br- (Suzuki, Kitabatake et Koide , 2016).
McCall et coll. (2014) ont montré que Br est un cofacteur nécessaire à la formation de réticulations sulfilimine catalysées par l'enzyme peroxidasine, une modification post-traductionnelle essentielle à l'architecture du collagène IV des membranes basales et au développement des tissus..
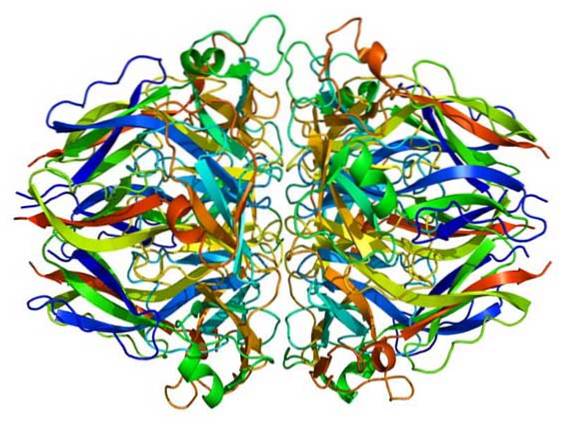
Les membranes basales sont des matrices extracellulaires spécialisées qui sont des médiateurs clés de la transduction du signal et du support mécanique des cellules épithéliales..
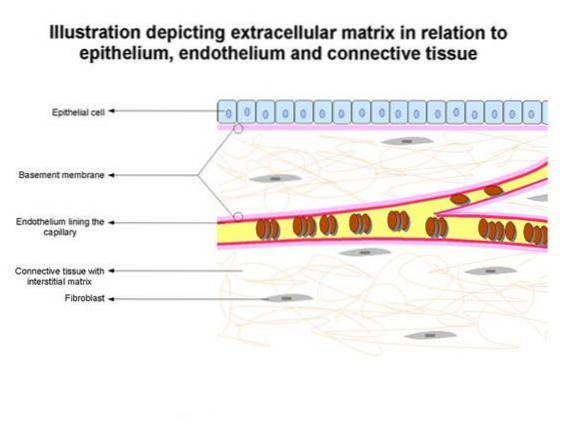
Les membranes basales définissent l'architecture du tissu épithélial et facilitent la réparation tissulaire après une blessure, entre autres fonctions..
Un échafaudage de collagène IV réticulé avec de la sulfilimine est intégré dans la membrane basale, ce qui donne la fonctionnalité de matrice dans les tissus multicellulaires de tous les animaux..
Les échafaudages de collagène IV fournissent une résistance mécanique, servent de ligand pour les intégrines et autres récepteurs de surface cellulaire et interagissent avec des facteurs de croissance pour établir des gradients de signalisation..
La sulfilimine (sulfimide) est un composé chimique qui contient une double liaison soufre-azote. Les liaisons sulfilimine stabilisent les brins de collagène IV présents dans la matrice extracellulaire.
Ces liaisons lient de manière covalente les résidus méthionine 93 (Met93) et hydroxylysine 211 (Hyl211) des brins polypeptidiques adjacents pour former un trimère de collagène plus grand..
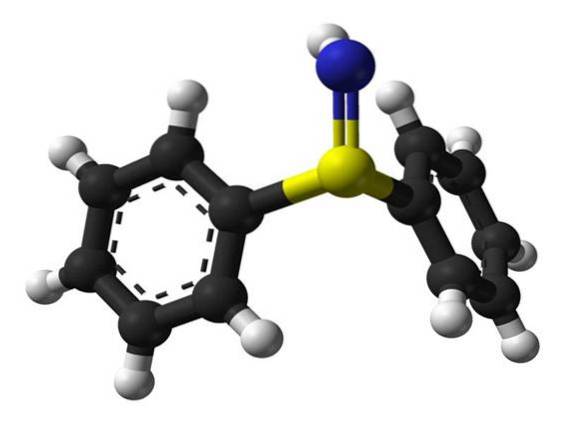
La peroxydaine forme respectivement de l'acide hypobromeux (HOBr) et de l'acide hypochloreux (HOCl) à partir du bromure et du chlorure, qui peuvent induire la formation de réticulations sulfilimine..
Le bromure, converti en acide hypobrome, forme un intermédiaire de l'ion bromosulfonium (S-Br) qui participe à la formation de réticulations.
McCall et coll. (2014) ont démontré que la carence alimentaire en Br est mortelle chez la drosophile, tandis que le remplacement du Br restaure sa viabilité.
Ils ont également établi que le brome est un oligo-élément essentiel pour tous les animaux en raison de son rôle dans la formation des liaisons sulfilimine et du collagène IV, ce qui est d'une importance vitale pour la formation des membranes basales et le développement des tissus..
Les références
- ChemIDplus, (2017). Structure 3D de 13517-11-8 - Acide hypobromeux [image] Récupéré de nih.gov.
- ChemIDplus, (2017). Structure 3D de 60-18-4 - Tyrosine [USAN: INN] [image] Récupéré de nih.gov.
- ChemIDplus, (2017). Structure 3D de 7726-95-6 - Brome [image] Récupéré de nih.gov.
- ChemIDplus, (2017). Structure 3D de 7732-18-5 - Eau [image] Récupérée de nih.gov.
- Emw, (2009). Protéine COL4A1 PDB 1li1 [image] Récupérée de wikipedia.org.
- Mills, B. (2009). Diphenylsulfimide-from-xtal-2002-3D-balls [image] Récupéré de wikipedia.org.
- PubChem, (2016). Acide hypobromeux [image] Récupéré de nih.gov.
- Steane, R. (2014). La molécule d'ADN - rotative en 3 dimensions [image] Récupéré de biotopics.co.uk
- Thormann, U. (2005). NeutrophilerAktion [image] Récupéré de wikipedia.org.



Personne n'a encore commenté ce post.