
Structure du groupe acyle, caractéristiques, composés et dérivés
le groupe acyle C'est un fragment moléculaire qui, en chimie organique, est généralement dérivé d'acides carboxyliques. Sa formule est RCO, où R est un substituant carbone, alkyle ou aryle, lié de manière covalente et directement au groupe carbonyle, C = O. Il ne s'agit généralement que d'une fraction de la structure d'un composé organique, comme une biomolécule..
On dit qu'il dérive d'un acide carboxylique, RCOOH, car il suffira d'éliminer le groupe hydroxyle, OH, pour obtenir le groupe acyle, RCO. A noter que ce groupe comprend une large famille de composés organiques (et inorganiques). Cette famille est généralement connue sous le nom de composés acylés (et non d'asile).

Dans l'image supérieure, nous avons la formule développée du groupe acyle. Il est facile de le reconnaître en observant n'importe quelle structure moléculaire, car il est toujours situé aux extrémités et est indiqué par le groupe carbonyle. Un exemple de cela que nous verrons dans la molécule d'acétyl-CoA, essentielle pour le cycle de Krebs.
L'incorporation de ce groupe dans une molécule est connue sous le nom de réaction d'acylation. Le groupe acyl fait partie de la routine de travail dans les synthèses organiques.
Index des articles
- 1 Structure et caractéristiques du groupe acyle
- 2 Composés et dérivés
- 2.1 - Chlorures
- 2.2 - Radical
- 2.3 - Cation
- 2.4 - Amides
- 2.5 - Aldéhydes
- 2.6 - Cétones et esters
- 2.7 - Commentaire général
- 3 Exemples de groupe acyle
- 4 Références
Structure et caractéristiques du groupe acyle
La structure du groupe acyle dépend de l'identité de R. L'atome de carbone de ladite chaîne latérale R, ainsi que le C = O auquel il est attaché, sont situés dans le même plan. Le segment RCO de la première image est donc plat.
Cependant, ce fait pourrait sembler insignifiant sans les caractéristiques électroniques de C = O: l'atome de carbone a un léger déficit d'électrons. Cela le rend susceptible d'être attaqué par des agents nucléophiles, riches en électrons. Ainsi, le groupe acyle est réactif, étant un site spécifique dans lequel les synthèses organiques sont effectuées..
Composés et dérivés
En fonction des chaînes R ou des atomes placés à droite de RCO, différents composés ou dérivés du groupe acyle sont obtenus.
- Les chlorures
Supposons par exemple qu'un atome de chlore soit placé à droite de RCO. Cela remplace maintenant cette sinuosité représentée dans la première image, restant comme: RCOCl. Nous avons alors quelques dérivés appelés chlorures d'acyle.
Maintenant, en changeant l'identité de R dans RCOCl, nous obtenons plusieurs chlorures d'acyle:
-HCOCl, R = H, chlorure de méthanoyle, composé radicalement instable
-CH3COCl, R = CH3, chlorure d'acétyle
-CH3CHdeuxCOCl, R = CHdeuxCH3, chlorure de propionyle
-C6H5COCl, R = C6H5 (noyau benzénique), chlorure de benzoyle
Le même raisonnement s'applique aux fluorures, bromures et iodures d'acyle. Ces composés sont utilisés dans des réactions d'acylation, dans le but d'incorporer du RCO en tant que substituant à une molécule plus grande; par exemple, à un cycle benzénique.
- Radical
L'acyle peut exister momentanément sous forme de radical, RCO •, provenant d'un aldéhyde. Cette espèce est très instable et est immédiatement disproportionnée par rapport à un radical alkyle et au monoxyde de carbone:
RC • = O → R • + C≡O
- Cation
Le groupe acyle peut également se présenter sous forme de cation, RCO+, étant un intermédiaire qui réagit pour acyler une molécule. Cette espèce contient deux structures de résonance représentées dans l'image ci-dessous:
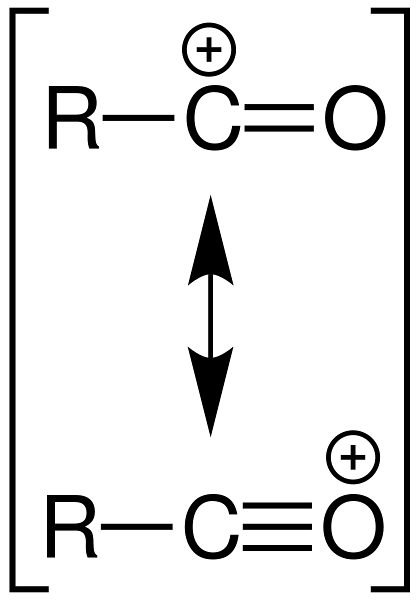
Notez comment la charge partielle positive est répartie entre les atomes de carbone et d'oxygène. De ces deux structures, [R-C≡O+], avec la charge positive sur l'oxygène, est le plus prédominant.
- Amides
Supposons maintenant qu'au lieu d'un atome Cl, nous plaçons un groupe amino, NHdeux. Nous aurons alors un amide, RCONHdeux, RC (O) NHdeux ou RC = ONHdeux. Ainsi, en changeant finalement l'identité de R, on obtiendra une famille d'amides.
- Aldéhydes
Si au lieu de NHdeux nous plaçons un atome d'hydrogène, nous obtiendrons un aldéhyde, RCOH ou RCHO. Notez que le groupe acyle est toujours présent même lorsqu'il est passé à l'arrière-plan d'importance. Les aldéhydes et les amides sont des composés acylés.
- Cétones et esters
En poursuivant le même raisonnement, on peut substituer H à une autre chaîne latérale R, ce qui donnera naissance à une cétone, RCOR 'ou RC (O) R'. Cette fois, le groupe acyle est plus "caché", car l'une des deux extrémités peut être considérée comme RCO ou R'CO.
D'autre part, R 'peut également être substitué à OR', donnant naissance à un ester, RCOOR '. Dans les esters, le groupe acyle est reconnu à l'œil nu car il se trouve sur le côté gauche du groupe carbonyle.
- Commentaire général
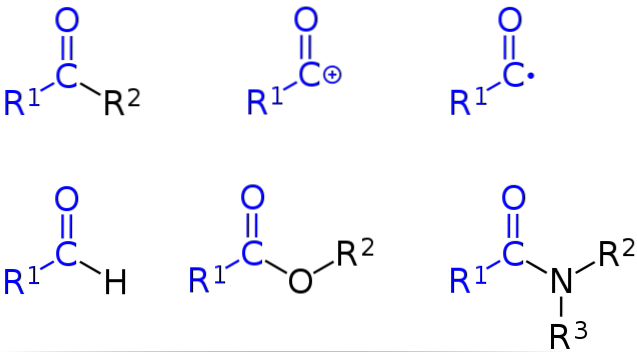
L'image du haut représente globalement tout ce qui est discuté dans cette section. Le groupe acyle est surligné en bleu, et en partant du coin supérieur, de gauche à droite, on a: cétones, cation acyle, radical acyle, aldéhyde, esters et amides.
Bien que le groupe acyle soit présent dans ces composés, ainsi que dans les acides carboxyliques et les thioesters (RCO-SR '), le groupe carbonyle est généralement donné plus d'importance lors de la définition de ses moments dipolaires. Le RCO est plus intéressant lorsqu'il est trouvé comme substituant, ou lorsqu'il est directement lié à un métal (acyles métalliques).
Selon le composé, RCO peut avoir des noms différents, comme on le voit dans la sous-section sur les chlorures d'acyle. Par exemple, CH3Le CO est connu sous le nom d'acétyle ou d'éthanoyle, tandis que CH3CHdeuxCO, propionyle ou propanoyle.
Exemples de groupe acyle

L'un des exemples les plus représentatifs de composés acylés est l'acétyl-CoA (image du haut). Notez qu'il est immédiatement identifié car il est surligné en bleu. Le groupe acyle de l'acétyl-CoA, comme son nom l'indique, est acétyle, CH3CO. Bien que cela puisse ne pas en avoir l'air, ce groupe est essentiel dans le cycle de Krebs de notre corps.
Les acides aminés contiennent également le groupe acyle, mais, encore une fois, il a tendance à passer inaperçu. Par exemple, pour la glycine, NHdeux-CHdeux‐COOH, son groupe acyle devient le segment NHdeux-CHdeux-CO, et s'appelle glycyl. Pendant ce temps, pour la lysine, son groupe acyle devient NHdeux(CHdeux)4CHNHdeuxCO, qui s'appelle lysyl.
Bien que cela ne soit généralement pas discuté très régulièrement, les groupes acyle peuvent également provenir d'acides inorganiques; c'est-à-dire que l'atome central ne doit pas nécessairement être du carbone, mais peut également être constitué d'autres éléments. Par exemple, un groupe acyle pourrait également être RSO (RS = 0), dérivé de l'acide sulfonique, ou RPO (RP = 0), dérivé de l'acide phosphonique..
Les références
- Morrison, R. T. et Boyd, R, N. (1987). Chimie organique. 5e édition. Éditorial Addison-Wesley Interamericana.
- Carey F. (2008). Chimie organique. (Sixième édition). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chimie organique. (10e édition.). Wiley plus.
- Wikipédia. (2020). Groupe acyle. Récupéré de: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (11 février 2020). Définition du groupe acyle et exemples. Récupéré de: thinkco.com
- Laura Foist. (2020). Groupe Acyl: Définition et structure. Étude. Récupéré de: study.com
- Steven A. Hardinger. (2017). Glossaire illustré de chimie organique: groupe acyle. Récupéré de: chem.ucla.edu



Personne n'a encore commenté ce post.