
Caractéristiques et fonctions des hémocyanines

le hémocyanines sont des protéines responsables du transport de l'oxygène en phase liquide chez les invertébrés qui comprennent exclusivement les arthropodes et les mollusques. Les hémocyanines dans l'hémolymphe remplissent un rôle analogue à celui de l'hémoglobine dans le sang chez les oiseaux et les mammifères. Cependant, son efficacité en tant que convoyeur est moindre.
Étant donné que les hémocyanines sont des protéines qui utilisent du cuivre au lieu du fer pour piéger l'oxygène, elles deviennent bleues lorsqu'elles sont oxydées. On peut dire que les animaux qui l'utilisent sont des animaux à sang bleu.
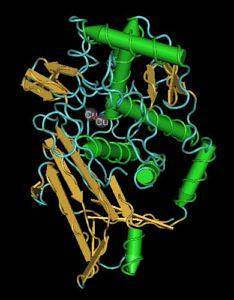
Nous, comme les autres mammifères, au contraire, sommes des animaux à sang rouge. Pour remplir cette fonction, chaque molécule de cette métalloprotéine nécessite deux atomes de cuivre pour chaque oxygène complexé..
Une autre différence entre les animaux à sang bleu et à sang rouge est la façon dont ils transportent l'oxygène. Dans le premier, l'hémocyanine est directement présente dans l'hémolymphe de l'animal. L'hémoglobine, en revanche, est transportée par des cellules spécialisées appelées érythrocytes..
Certaines des hémocyanines sont parmi les protéines les plus connues et les mieux étudiées. Ils ont une grande diversité structurelle et se sont avérés très utiles dans un large éventail d'applications médicales et thérapeutiques chez l'homme..
Index des articles
- 1 Caractéristiques générales
- 2 fonctions
- 2.1 Autres fonctions
- 3 utilisations
- 4 Références
Caractéristiques générales
Les hémocyanines les mieux caractérisées sont celles qui ont été isolées à partir de mollusques. Ce sont parmi les plus grandes protéines connues, avec des masses moléculaires comprises entre 3,3 et 13,5 MDa.
Les hémocyanines de mollusque sont d'énormes moulages creux de glycoprotéines multimères qui, cependant, peuvent être trouvées solubles dans l'hémolymphe de l'animal..
L'une des raisons de leur forte solubilité est que les hémocyanines ont une surface avec une charge négative très élevée. Ils forment des sous-unités de décamères ou multidécamères compris entre 330 et 550 kDa, qui comprennent environ sept unités fonctionnelles paralogiques.
Un gène paralogue est celui qui résulte d'un événement de duplication génétique: une protéine paralogue provient de la traduction d'un gène paralogue. En fonction de l'organisation de leurs domaines fonctionnels, ces sous-unités interagissent entre elles pour former des décamères, didecamers et tridecamers..
L'hémocyanine arthropode, en revanche, est l'hexamérie. Dans son état natif, il peut être trouvé comme un entier de multiples d'hexamères (de 2 x 6 à 8 x 6). Chaque sous-unité pèse entre 70 et 75 kDa.
Une autre caractéristique remarquable des hémocyanines est qu'elles sont structurellement et fonctionnellement stables dans une plage de température assez large (de -20 ° C à plus de 90 ° C)..
Selon l'organisme, les hémocyanines peuvent être synthétisées dans des organes spécialisés de l'animal. Chez les crustacés, ce sont les hépatopancréas. Dans d'autres organismes, ils sont synthétisés notamment dans des cellules telles que les cyanocytes de chélicères, ou les rogocytes de mollusques..
Caractéristiques
La fonction la plus connue des hémocyanines est liée à leur participation au métabolisme énergétique. L'hémocyanine rend la respiration aérobie possible chez une majorité significative d'invertébrés.
La réaction bioénergétique la plus importante chez les animaux est la respiration. Au niveau cellulaire, la respiration permet la dégradation des molécules de sucre de manière contrôlée et successive, par exemple pour obtenir de l'énergie.
Pour mener à bien ce processus, un accepteur d'électrons final est nécessaire, qui à toutes fins utiles est, par excellence, l'oxygène. Les protéines responsables de leur capture et de leur transport sont variées.
Beaucoup d'entre eux utilisent un complexe d'anneaux organiques qui complexent le fer afin d'interagir avec l'oxygène. L'hémoglobine, par exemple, utilise une porphyrine (groupe hème).
D'autres utilisent des métaux tels que le cuivre dans le même but. Dans ce cas, le métal forme des complexes temporaires avec des résidus d'acides aminés du site actif de la protéine porteuse..
Bien que de nombreuses protéines de cuivre catalysent des réactions oxydatives, les hémocyanines réagissent avec l'oxygène de manière réversible. L'oxydation a lieu dans une étape dans laquelle le cuivre passe de l'état I (incolore) à l'état II oxydé (bleu).
Il transporte l'oxygène dans l'hémolymphe, dans lequel il représente 50 à plus de 90% de la protéine totale. Pour tenir compte de son rôle physiologique important, bien qu'avec une faible efficacité, l'hémocyanine peut être trouvée à des concentrations aussi élevées que 100 mg / mL..
Autres fonctions
Les preuves accumulées au fil des ans indiquent que les hémocyanines remplissent d'autres fonctions en plus d'agir en tant que transporteurs d'oxygène. Les hémocyanines participent à la fois aux processus homéostatiques et physiologiques. Il s'agit notamment de la mue, du transport d'hormones, de l'osmorégulation et du stockage des protéines..
D'autre part, il a été prouvé que les hémocyanines jouent un rôle fondamental dans la réponse immunitaire innée. Les peptides d'hémocyanine et les peptides associés présentent une activité antivirale ainsi qu'une activité phénoloxydase. Cette dernière activité, la phénoloxydase respiratoire, est liée aux processus de défense contre les agents pathogènes.
Les hémocyanines fonctionnent également comme des protéines précurseurs peptidiques avec une activité antimicrobienne et antifongique. D'autre part, il a été prouvé que certaines hémocyanines ont une activité antivirale intrinsèque non spécifique.
Cette activité n'est pas cytotoxique pour l'animal lui-même. Dans la lutte contre d'autres agents pathogènes, les hémocyanines peuvent s'agglutiner en présence, par exemple, de bactéries et arrêter l'infection.
Il est également important de noter que les hémocyanines participent à la production d'espèces réactives de l'oxygène (ROS). Les ROS sont des molécules fondamentales dans le fonctionnement du système immunitaire, ainsi que dans les réponses aux agents pathogènes chez tous les eucaryotes.
Applications
Les hémocyanines sont de puissants immunostimulants chez les mammifères. Pour cette raison, ils ont été utilisés comme transporteurs hypoallergéniques de molécules incapables de susciter une réponse immunitaire par elles-mêmes (haptènes)..
D'autre part, ils ont également été utilisés comme transporteurs efficaces d'hormones, de médicaments, d'antibiotiques et de toxines. Ils ont également été testés comme composés antiviraux potentiels et comme compagnons de thérapies chimiques contre le cancer..
Enfin, il existe des preuves que les hémocyanines de certains crustacés ont une activité antitumorale dans certains systèmes animaux expérimentaux. Les traitements contre le cancer qui ont été testés comprennent ceux de la vessie, de l'ovaire, du sein, etc..
D'un point de vue structurel et fonctionnel, les hémocyanines ont leurs propres caractéristiques qui les rendent idéales pour le développement de nouveaux nanomatériaux biologiques. Ils ont été utilisés, par exemple, dans la génération de biocapteurs électrochimiques avec un succès considérable.
Les références
- Abid Ali, S., Abbasi, A. (011) Hémocyanine de scorpion: Le sang bleu. DM Verlag Dr. Müller, Allemagne.
- Coates, C. J., Nairn, J. (2014) Diverses fonctions immunitaires des hémocyanines. Immunologie développementale et comparée, 45: 43-55.
- Kato, S., Matsui, T., Gatsogiannis, C., Tanaka, Y. (2018) Hémocyanine mollusque: structure, évolution et physiologie. Revues biophysiques, 10: 191-202.
- Metzler, D. (2012) Biochimie: Les réactions chimiques des cellules vivantes. Elsevier, NY, États-Unis.
- Yang, P., You, J., Li, F., Fei, J., Feng, B., He, X. Zhou, J. (2013) Plateforme de biocapteur électrochimique basée sur une hémocyanine- [email protected] NP- film nano-composite hybride de noir de carbone. Méthodes analytiques, 5: 3168-3171.
- Zanjani, N. T., Saksena, M. M., Dehghani, F., Cunningham, A. L. (2018) De l'océan au chevet: le potentiel thérapeutique des hémocyanines mollusques. Chimie médicinale actuelle, 25: 2292-2303.


Personne n'a encore commenté ce post.