
Structure de l'hydrure de lithium, propriétés, production, utilisations

le hydrure de lithium c'est un solide inorganique cristallin dont la formule chimique est LiH. C'est le sel inorganique le plus léger, son poids moléculaire n'est que de 8 g / mol. Il est formé par l'union d'un lithium-ion Li+ et un ion hydrure H-. Les deux sont liés par une liaison ionique.
LiH a un point de fusion élevé. Il réagit facilement avec l'eau et de l'hydrogène gazeux est produit dans la réaction. Il peut être obtenu par réaction entre le lithium métal fondu et l'hydrogène gazeux. Il est largement utilisé dans les réactions chimiques pour obtenir d'autres hydrures.
Le LiH a été utilisé pour se protéger contre les rayonnements dangereux tels que ceux trouvés dans les réacteurs nucléaires, c'est-à-dire les rayonnements ALPHA, BETA, GAMMA, les protons, les rayons X et les neutrons..
Il a également été proposé pour la protection des matériaux des fusées spatiales propulsées par propulsion thermique nucléaire. Des études sont même en cours pour être utilisées comme protection de l'être humain contre les rayonnements cosmiques lors de futurs voyages sur la planète Mars..
Index des articles
- 1 Structure
- 2 Nomenclature
- 3 propriétés
- 3.1 État physique
- 3.2 Poids moléculaire
- 3.3 Point de fusion
- 3.4 Point d'ébullition
- 3.5 Température d'auto-inflammation
- 3.6 Densité
- 3.7 Solubilité
- 3.8 Autres propriétés
- 4 Obtention
- 5 Utilisation comme écran de protection contre les rayonnements dangereux
- 5.1 - Dans les réacteurs nucléaires
- 5.2 - Dans les systèmes spatiaux de propulsion thermique nucléaire
- 5.3 - En protection contre les rayonnements cosmiques
- 6 Utilisation comme moyen de stockage et de transport sûrs de l'hydrogène
- 7 Utilisation dans des réactions chimiques
- 8 Références
Structure
L'hydrogène dans l'hydrure de lithium a une charge négative H-, car il a soustrait un électron du métal, qui se présente sous la forme d'un ion Li+.
La configuration électronique du cation Li+ est: [He] 1sdeux ce qui est très stable. Et la structure électronique de l'anion hydrure H- est: 1sdeux, qui est également très stable.
Le cation et l'anion sont unis par des forces électrostatiques.
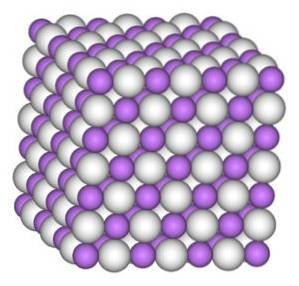
Le cristal d'hydrure de lithium a la même structure que le chlorure de sodium NaCl, c'est-à-dire une structure cristalline cubique.
Nomenclature
- Hydrure de lithium
- LiH
Propriétés
État physique
Solide cristallin blanc ou incolore. Le LiH commercial peut être bleu-gris en raison de la présence de petites quantités de lithium métal..
Poids moléculaire
8 g / mol
Point de fusion
688 ºC
Point d'ébullition
Il se décompose à 850 ºC.
La température d'auto-inflammation
200 ºC
Densité
0,78 g / cm3
Solubilité
Réagit avec l'eau. Il est insoluble dans les éthers et les hydrocarbures.
Autres propriétés
L'hydrure de lithium est beaucoup plus stable que les hydrures des autres métaux alcalins et peut être fondu sans décomposition..
Il n'est pas affecté par l'oxygène s'il est chauffé à des températures inférieures au rouge. Il n'est pas non plus affecté par le chlore Cldeux et acide chlorhydrique HCl.
Le contact de LiH avec la chaleur et l'humidité provoque une réaction exothermique (génère de la chaleur) et un dégagement d'hydrogène Hdeux et hydroxyde de lithium LiOH.
Il peut former une fine poussière qui peut exploser au contact des flammes, de la chaleur ou des matières oxydantes. Il ne doit pas entrer en contact avec du protoxyde d'azote ou de l'oxygène liquide, car il pourrait exploser ou s'enflammer.
Il s'assombrit lorsqu'il est exposé à la lumière.
Obtention
L'hydrure de lithium a été obtenu en laboratoire par réaction entre le lithium métal fondu et l'hydrogène gazeux à une température de 973 K (700 ºC).
2 Li + Hdeux → 2 LiH
De bons résultats sont obtenus lorsque la surface exposée du lithium fondu est augmentée et lorsque le temps de sédimentation du LiH est diminué. C'est une réaction exothermique.
Utiliser comme écran de protection contre les rayonnements dangereux
Le LiH possède un certain nombre de caractéristiques qui le rendent intéressant pour une utilisation comme protection pour les humains dans les réacteurs nucléaires et les systèmes spatiaux. Voici quelques-unes de ces caractéristiques:
- Il a une teneur élevée en hydrogène (12,68% en poids de H) et un nombre élevé d'atomes d'hydrogène par unité de volume (5,85 x 1022 H atomes / cm3).
- Son point de fusion élevé lui permet d'être utilisé dans des environnements à haute température sans fondre.
- Il présente une faible pression de dissociation (~ 20 torr à son point de fusion) qui permet au matériau d'être fondu et congelé sans se dégrader sous une faible pression d'hydrogène..
- Il a une faible densité, ce qui le rend attractif pour une utilisation dans les systèmes spatiaux..
- Cependant, ses inconvénients sont sa faible conductivité thermique et ses mauvaises propriétés mécaniques. Mais cela n'a pas diminué son applicabilité.
- Les pièces LiH qui servent de boucliers sont fabriquées par pressage à chaud ou à froid et par fusion et coulée dans des moules. Bien que cette dernière forme soit préférée.
- A température ambiante, les pièces sont protégées de l'eau et de la vapeur d'eau et aux températures élevées par une petite surpression d'hydrogène dans un récipient scellé.
- Dans les réacteurs nucléaires
Dans les réacteurs nucléaires, il existe deux types de rayonnement:
Rayonnement directement ionisant
Ce sont des particules hautement énergétiques qui transportent une charge électrique, comme les particules alpha (α) et bêta (β) et les protons. Ce type de rayonnement interagit très fortement avec les matériaux des boucliers, provoquant une ionisation en interagissant avec les électrons des atomes des matériaux à travers lesquels ils passent..
Rayonnement indirectement ionisant
Ce sont des neutrons, des rayons gamma (γ) et des rayons X, qui sont pénétrants et nécessitent une protection massive, car ils impliquent l'émission de particules chargées secondaires, qui sont celles qui provoquent l'ionisation..

Selon certaines sources, LiH est efficace pour protéger les matériaux et les personnes contre ces types de rayonnement.
- Dans les systèmes spatiaux de propulsion thermique nucléaire
Le LiH a récemment été choisi comme modérateur potentiel et comme matériau de protection contre les radiations nucléaires pour les systèmes de propulsion thermique nucléaire des engins spatiaux à très long voyage..

Sa faible densité et sa forte teneur en hydrogène permettent de réduire efficacement la masse et le volume du réacteur nucléaire..
- En protection contre les rayonnements cosmiques
L'exposition aux rayonnements spatiaux est le risque le plus important pour la santé humaine dans les futures missions d'exploration interplanétaire.
Dans l'espace lointain, les astronautes seront exposés à tout le spectre des rayons cosmiques galactiques (ions de haute énergie) et des événements d'éjection de particules solaires (protons)..
Le danger d'exposition aux radiations est aggravé par la durée des missions. De plus, la protection des lieux que les explorateurs habiteront doit également être prise en compte.

Dans cette veine, une étude réalisée en 2018 a indiqué que parmi les matériaux testés, le LiH offre la plus grande réduction de rayonnement par gramme par cmdeux, étant ainsi l'un des meilleurs candidats à utiliser dans la protection contre les rayonnements cosmiques. Cependant, ces études doivent être approfondies.
Utilisation comme moyen de stockage et de transport sûr pour l'hydrogène
Obtenir de l'énergie à partir de Hdeux C'est quelque chose qui a été étudié pendant plusieurs dizaines d'années et qui a déjà trouvé une application pour remplacer les combustibles fossiles dans les véhicules de transport..
Le Hdeux peut être utilisé dans les piles à combustible et contribuer à la réduction de la production de COdeux et nonX, évitant ainsi l'effet de serre et la pollution. Cependant, un système efficace pour stocker et transporter H n'a pas encore été trouvédeux en toute sécurité, léger, compact ou de petite taille, rapide à ranger et à libérer le Hdeux tout aussi rapide.
L'hydrure de lithium LiH est l'un des hydrures alcalins qui a la plus grande capacité de stockage de Hdeux (12,7% en poids de H). Relâchez Hdeux par hydrolyse selon la réaction suivante:
LiH + HdeuxO → LiOH + Hdeux
LiH fournit 0,254 kg d'hydrogène pour chaque kg de LiH. De plus, il a une capacité de stockage élevée par unité de volume, ce qui signifie qu'il est léger et est un support compact pour le stockage de Hdeux.

De plus, LiH se forme plus facilement que d'autres hydrures de métaux alcalins et est chimiquement stable aux températures et pressions ambiantes. Le LiH peut être transporté du fabricant ou du fournisseur à l'utilisateur. Ensuite, par hydrolyse de LiH, H est générédeux et ceci est utilisé en toute sécurité.
L'hydroxyde de lithium LiOH formé peut être renvoyé au fournisseur qui régénère le lithium par électrolyse, puis produit à nouveau du LiH..
LiH a également été étudié avec succès pour être utilisé en conjonction avec l'hydrazine boratée dans le même but..
Utilisation dans les réactions chimiques
LiH permet la synthèse d'hydrures complexes.
Il est utilisé, par exemple, pour préparer le triéthylborohydrure de lithium, qui est un nucléophile puissant dans les réactions de déplacement d'halogénures organiques..
Les références
- Sato, Y. et Takeda, O. (2013). Système de stockage et de transport d'hydrogène grâce à l'hydrure de lithium utilisant la technologie du sel fondu. Dans la chimie des sels fondus. Chapitre 22, pages 451-470. Récupéré de sciencedirect.com.
- NOUS. Bibliothèque nationale de médecine. (2019). Hydrure de lithium. Récupéré de: pubchem.ncbi.nlm.nih.gov.
- Wang, L. et coll. (2019). Etude de l'impact de l'effet thermique noyau de l'hydrure de lithium sur la réactivité du réacteur à lit de particules de propulsion nucléaire. Annales de l'énergie nucléaire 128 (2019) 24-32. Récupéré de sciencedirect.com.
- Cotton, F. Albert et Wilkinson, Geoffrey. (1980). Chimie inorganique avancée. Quatrième édition. John Wiley et fils.
- Giraudo, M. et coll. (2018). Tests basés sur des accélérateurs de l'efficacité du blindage de différents matériaux et multicouches utilisant des ions légers et lourds à haute énergie. Recherche sur les radiations 190; 526-537 (2018). Récupéré de ncbi.nlm.nih.gov.
- Welch, F.H. (1974). Hydrure de lithium: un matériau de protection de l'ère spatiale. Nuclear Engineering and Design 26, 3, février 1974, pages 444-460. Récupéré de sciencedirect.com.
- Simnad, M.T. (2001). Réacteurs nucléaires: matériaux de protection. Dans Encyclopédie des matériaux: science et technologie (deuxième édition). Pages 6377-6384. Récupéré de sciencedirect.com.
- Hügle, T. et coll. (2009). Hydrazine borane: un matériau de stockage de l'hydrogène prometteur. J. Am. Chem. Soc. 2009, 131, 7444-7446. Récupéré de pubs.acs.org.



Personne n'a encore commenté ce post.