
Structure, utilisations, propriétés du lauryl sulfate de sodium

le laurylsulfate de sodium est un sel organique formé par l'union de l'ion sodium Na+ et l'ion laurylsulfate n-COnzeH2. 3CHdeuxOURS3-. Sa formule chimique est CH3-(CHdeux)dix-CHdeux-OURS3-N / A+. Il est également connu sous le nom de dodécyl sulfate de sodium car la chaîne hydrocarbonée a 12 atomes de carbone. C'est un composant des produits de bain moussant.
Le laurylsulfate de sodium est un composé qui agit sur la surface qui se situe entre deux phases, par exemple entre le liquide et le gaz, ou entre l'eau et l'huile. Cela le rend capable d'agir comme un détergent car il se lie aux gouttelettes d'huile ou de graisse, ou de petites portions de saleté, et les sépare de l'eau sous la forme d'une particule flottante, qui est ensuite facilement rincée..

Il sert également de dispersant pour les ingrédients des produits alimentaires, améliorant leur texture et est utilisé dans le shampooing pour animaux de compagnie car il repousse les puces et les tiques. Il agit également comme humectant dans les médicaments pour animaux et est utilisé dans l'agriculture, les peintures, les plastiques et la recherche en chimie et en biologie..
Il existe des études qui indiquent qu'il brise les membranes qui entourent certains virus et bactéries, agissant dans certains cas comme un agent antimicrobien.
Index des articles
- 1 Structure
- 2 Nomenclature
- 3 propriétés
- 3.1 État physique
- 3.2 Poids moléculaire
- 3.3 Point de fusion
- 3.4 Poids spécifique
- 3.5 Solubilité
- 3.6 Autres propriétés
- 3.7 Mécanisme d'action en tant que tensioactif
- 4 Obtention
- 5 utilisations
- 5.1 Lors du nettoyage
- 5.2 En cosmétique
- 5.3 Dans l'industrie alimentaire
- 5.4 Dans les applications vétérinaires
- 5.5 Dans les produits pharmaceutiques
- 5.6 En médecine
- 5.7 Dans diverses applications
- 5.8 Dans les laboratoires de recherche chimique et biologique
- 5.9 Dans l'industrie pétrolière
- 6 Références
Structure
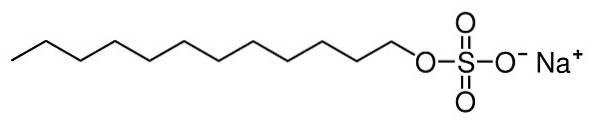
Le laurylsulfate de sodium ou le dodécylsulfate de sodium est un composé organique ionique formé par un cation sodium Na+ et un anion dodécylsulfate n-COnzeH2. 3CHdeuxOURS3-. le n dans votre formule compacte pour indiquer qu'il s'agit d'une chaîne droite (non ramifiée).
L'anion dodécyl sulfate a une chaîne hydrocarbonée linéaire de 12 atomes de carbone attachée à un sulfate -OSO3- par l'oxygène, il a donc une seule charge négative.
Nomenclature
- Laurylsulfate de sodium
- Sulfate de dodécyle de sodium
- SLS Sulfate de lauryle de sodium)
Propriétés
État physique
Solide blanc ou crème sous forme de cristaux, de flocons ou de poudre.
Poids moléculaire
288,38 g / mol
Point de fusion
205,5 ºC
Poids spécifique
Supérieur à 1,1 à 20 ºC
Solubilité
Il est modérément soluble dans l'eau: 15 g / 100 mL à 20 ºC.
Autres propriétés
Le laurylsulfate de sodium est un tensioactif ou tensioactif ionique. Cela signifie qu'il a un effet sur la surface qui sépare deux phases non miscibles..
C'est un tensioactif anionique car la partie qui effectue l'action tensioactive est l'anion laurylsulfate COnzeH2. 3CHdeuxOURS3- et pas de sodium Na+.
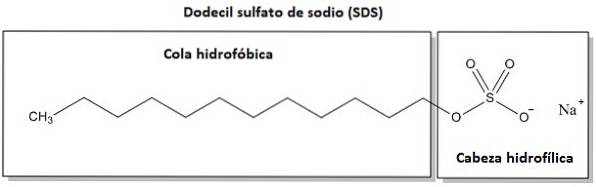
C'est un composé amphiphile, cela signifie qu'une partie de la molécule a une affinité pour l'eau (elle est hydrophile) et une autre section a une similitude ou une attraction pour les huiles et les graisses et repousse l'eau (elle est hydrophobe).
La partie hydrophile est l'endroit où se trouve la charge négative de l'anion, c'est-à-dire les oxygènes du groupe OSO3- de la molécule. La fraction hydrophobe est la chaîne hydrocarbonée ou COnzeH2. 3CHdeux-.
Il est facilement biodégradable et seulement faiblement toxique.
Mécanisme d'action en tant que surfactant
L'action qu'il exerce en tant que tensioactif est de modifier ou de changer la tension superficielle, en particulier dans les solutions aqueuses. Cela vous permet d'émulsionner les graisses et les huiles.
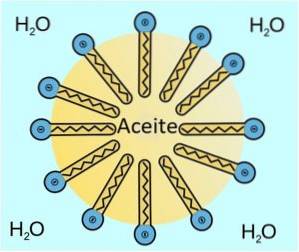
Le mécanisme d'action est qu'il est situé sur la surface de contact entre les deux liquides, là où la tension superficielle diminue..
Pour ce faire, la tête ou la partie hydrophile OSO3- est mis en contact avec l'eau et la colle ou la partie hydrophobe COnzeH2. 3CHdeux- se trouve à l'intérieur de l'huile ou de la graisse.
Obtention
Il est dérivé de l'huile de noix de coco ou de palme, entre autres huiles. A partir de ceux-ci, on obtient de l'acide laurylique, qui est un acide gras. Celui-ci subit un processus de réduction (à l'opposé de l'oxydation) pour obtenir de l'alcool laurylique..
Pour obtenir du laurylsulfate de sodium, l'alcool laurique est mis à réagir avec de l'acide sulfurique HdeuxSW4 et du sulfate d'acide laurylique est obtenu. Puis ce dernier, étant un acide, est neutralisé avec de l'hydroxyde de sodium NaOH.
n-COnzeH2. 3CHdeuxOH (alcool laurique) + HdeuxSW4 → n-COnzeH2. 3CHdeuxOURS3H (laurylsulfate acide)
n-COnzeH2. 3CHdeuxOURS3H + NaOH → n-COnzeH2. 3CHdeuxOURS3-N / A+ (laurylsulfate de sodium)
Applications
En raison de sa capacité en tant que tensioactif ou tensioactif, le laurylsulfate de sodium sert de détergent, d'émulsifiant, de dispersant, d'humectant, etc..
En nettoyage
C'est l'un des principaux composants des liquides vaisselle. Il est également essentiel dans les dentifrices ou les dentifrices, car il agit dans la formation de mousse, il hydrate et se disperse dans ces produits et dans de nombreux autres produits de nettoyage..


En cosmétique
Il est utilisé dans les lotions, shampooings, gels, bains moussants, bases de pommades, crèmes et décolorants pour les cheveux, entre autres..

Voici quelques-unes de ses autres utilisations:
Dans l'industrie alimentaire
Le dodécyl sulfate de sodium est utilisé très fréquemment dans l'industrie alimentaire, par exemple, dans les pâtes et les crèmes pour permettre une bonne dispersion des ingrédients, et dans les jus de fruits, entre autres aliments.
Il agit généralement comme dispersant, émulsifiant et épaississant. Améliore la texture de certains produits de boulangerie. Augmente la stabilité et allonge la durée de conservation des aliments.
Dans les applications vétérinaires
Le laurylsulfate de sodium agit comme un répulsif contre les puces et les tiques, c'est pourquoi il est utilisé dans les shampooings pour chiens et chats..

Il sert également d'agent mouillant dans certains antibiotiques et antimicrobiens pour l'administration orale ou topique (usage externe) pour les animaux. Il a une application dans les médicaments anthelminthiques.
Dans les produits pharmaceutiques
Le laurylsulfate de sodium a une large application dans l'industrie pharmaceutique pour ses propriétés tensioactives. Il fonctionne comme émulsifiant, dispersant, humectant, parmi de nombreuses autres actions.
Il a également la particularité de jouer le rôle de véhicule de transport dans divers médicaments, par exemple dans les médicaments que l'on souhaite pénétrer à travers la muqueuse buccale..
En médecine
Certaines sources d'information rapportent que le laurylsulfate de sodium a une action antivirale contre certains virus et bactéries.
Par exemple, il agit contre le virus VIH ou le virus de l'immunodéficience humaine, contre l'herpès simplex de type 2 et contre le virus du papillome humain. De plus, il a une action microbicide contre la chlamydia.
Sa puissante activité de dénaturation des protéines inhibe l'activité infectieuse des virus en solubilisant l'enveloppe virale en la perturbant. Son activité microbicide agit contre certains types de virus enveloppés et non enveloppés.
Le laurylsulfate de sodium a été utilisé dans la préparation d'échantillons sanguins pour la numération des globules rouges.
Dans diverses applications
- Dans l'industrie métallurgique: dans la galvanoplastie des métaux, en particulier du zinc et du nickel.
- En agriculture: comme microbicide, fongicide, bactéricide et comme émulsifiant dans les insecticides.
- Dans les peintures et agents de décapage: comme émulsifiant et pénétrant dans les laques, vernis et décapants de peinture.
- Dans l'industrie des plastiques et du caoutchouc: comme additif pour les plastiques et le latex. Améliore la résistance à la traction de certains polymères. En polymérisation en émulsion.
Dans les carburants pour fusées: comme agent anti-mousse.
Dans les laboratoires de recherche chimique et biologique
Le laurylsulfate de sodium sert d'outil de recherche en biochimie. Il est largement utilisé pour sa capacité à perturber ou désordre les membranes des micro-organismes.
Ses capacités à perturber la structure des tissus et à inhiber l'activité de certaines enzymes conduisent les biochimistes à l'utiliser comme composant clé de nombreux réactifs utilisés pour purifier les acides du noyau des cellules, comme l'ARN et l'ADN, ou les acides nucléiques..
Les membranes des micro-organismes sont principalement constituées de protéines et de lipides (graisses). Puisqu'il s'agit d'un détergent chargé négativement, le laurylsulfate de sodium adsorbe ou adhère fortement à la structure protéique, neutralisant toutes les charges positives. Il forme ainsi des associations hydrophobes internes, donnant à chaque protéine la même charge négative nette globale..
C'est la raison pour laquelle il est utilisé dans la séparation électrophorétique des protéines et des lipides, car comme ils ont une charge négative, les protéines sont mobilisées différemment contre un champ électrique..
Il est également utilisé pour déterminer la force relative du gluten dans des échantillons de farine ou de blé moulu. Le gluten est un type de protéine présent dans le blé.
Les particules de gluten sont hydratées par le laurylsulfate de sodium et les sédiments. Plus le volume de sédiments est élevé, plus la force des protéines de gluten dans l'échantillon est élevée..
Le laurylsulfate de sodium est également utilisé dans la caractérisation des composés NH ammonium quaternaire.4+. Il est également utilisé comme composé tensioactif de référence dans les tests de toxicité pour les espèces aquatiques et mammifères..
Dans l'industrie pétrolière
Le dodécyl sulfate de sodium est utilisé comme antiémulsifiant dans la technique d'extraction d'huile par fracturation hydraulique. fracturation hydraulique) des formations rocheuses riches en cela. Sert à empêcher la formation d'émulsions dans le fluide de fracture.
Les références
- NOUS. Bibliothèque nationale de médecine. (2019). Sulfate de dodécyle de sodium. Récupéré de: pubchem.ncbi.nlm.nih.gov.
- Farrell Jr., R.E. (2010). Ribonucléases résilientes. Sulfate de dodécyle de sodium. In RNA Methodologies (quatrième édition). Récupéré de sciencedirect.com.
- Righetti, G. et Boschetti, E. (2013). Méthodologies et protocoles détaillés. In Low-Abundance Proteome Discovery. Récupéré de sciencedirect.com.
- Kirk-Othmer (1994). Encyclopédie de la technologie chimique. Quatrième édition. John Wiley et fils.
- (2016). Analyse du blé et de la farine. Dans la farine de blé. Récupéré de sciencedirect.com.
- Franz-Montan, M. et coll. (2017). Systèmes nanostructurés pour l'administration transbuccale de médicaments. In Nanostructures for Oral Medicine. Récupéré de scienceirect.



Personne n'a encore commenté ce post.