
Justification, technique et utilisations du test de catalase
La test de catalase est une méthodologie utilisée dans les laboratoires de bactériologie pour révéler la présence de l'enzyme catalase dans les bactéries qui la possèdent. Avec la coloration de Gram, ce sont les principaux tests à effectuer sur les micro-organismes nouvellement isolés. Ces tests guident le microbiologiste sur les étapes à suivre pour l'identification définitive du microorganisme en question..
En général, les bactéries contenant du cytochrome possèdent l'enzyme catalase, ce qui signifie que les bactéries aérobies et anaérobies facultatives devraient la posséder. Cependant, il existe des exceptions, telles que Streptococcus, qui, bien que des micro-organismes anaérobies facultatifs ne possèdent pas l'enzyme catalase..
C'est pourquoi le test de la catalase est principalement utilisé pour distinguer les familles des Staphylococacées et des Micrococacées (toutes deux catalase positives) de la famille des Streptococacées (catalase négative)..
De même, le genre Bacillus (catalase positive) se distingue du genre Clostridium (catalase négative), entre autres.
Index des articles
- 1 Justification
- 2 Technique de routine pour le test de catalase
- 2.1 - Méthode de glissement
- 2.2 - Méthode directe en culture pure
- 2.3 -Méthode avec tube capillaire ou Fung et Petrishko
- 2.4 -Méthode Taylor et Achanzar pour les tests de catalase qui donnent des
- 3 Test de catalase pour les espèces de Mycobacterium
- 3.1 -Matériaux
- 3.2 -Préparation des réactifs
- 3.3 -Procédure
- 4 Utilisation
- 5 Contrôle de la qualité
- 6 Limitations
- 7 Références
Base
La catalase est une enzyme classée comme une hydroperoxydase, cela signifie qu'elle utilise du peroxyde d'hydrogène (HdeuxOU ALORSdeux).
Il est également considéré comme une oxydoréductase, car dans la réaction à laquelle il participe, il y a un élément qui sert de donneur d'électrons (substance réductrice) et un autre de récepteur d'électrons (substance oxydante).
La catalase est une protéine qui contient un groupe prosérique avec quatre atomes de fer trivalents (Fe+++), il s'agit donc d'une homoprotéine. L'ion ferrique reste oxydé pendant la réaction.
On peut dire que la catalase est une enzyme détoxifiante, car sa fonction est d'éliminer les substances produites lors du métabolisme bactérien et toxiques pour les bactéries. Parmi ces substances se trouve le peroxyde d'hydrogène.
Le peroxyde d'hydrogène est formé à partir de la décomposition des sucres par voie aérobie. Ce processus se déroule comme suit:
L'ion superoxyde (Odeux-) (radical libre) est le produit final de l'assimilation du glucose par voie aérobie. Ceci est toxique et est éliminé par l'enzyme superoxyde dismutase qui le transforme en oxygène gazeux et peroxyde d'hydrogène.
Le peroxyde d'hydrogène est également toxique pour les bactéries et doit être éliminé. L'enzyme catalase décompose le peroxyde d'hydrogène en eau et en oxygène.
La catalase peut agir sur des substrats autres que le peroxyde d'hydrogène, tels que les alcools, les aldéhydes, les acides, les amines aromatiques et les phénols. Cependant, le peroxyde d'hydrogène peut également être utilisé par la catalase pour oxyder d'autres composés toxiques tels que l'alcool méthylique et éthylique..
De même, la catalase est présente dans les cellules phagocytaires, la protégeant de l'action toxique du peroxyde d'hydrogène..
Technique de routine pour le test de catalase
-Méthode de la diapositive
Matériaux
3% de peroxyde d'hydrogène (10 volumes).
Lame de microscope
Manche en plastique jetable ou cure-dent en bois.
Traiter
Prélevez une quantité suffisante de la colonie à étudier sans toucher à la gélose dont elle est issue. La colonie doit être fraîche, c'est-à-dire d'une culture de 18 à 24 heures.
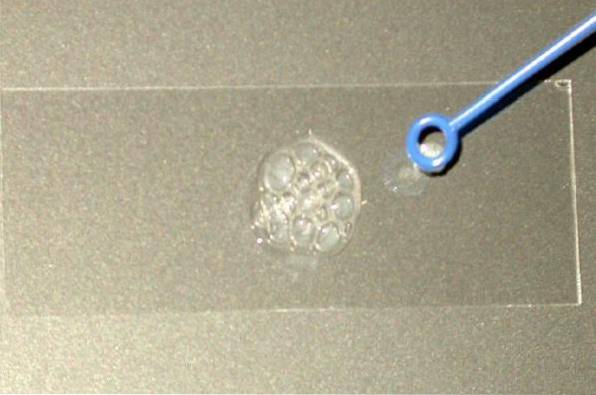
Placez la colonie sur la lame sèche et ajoutez dessus une goutte de peroxyde d'hydrogène à 3% (vous pouvez également utiliser HdeuxOU ALORSdeux 30%). Observez immédiatement si des bulles sont libérées ou non.
Interprétation
Réaction positive: dégagement de gaz, mis en évidence par la formation de bulles (fort bullage).
Réaction négative: pas de formation de bulles.
-Méthode directe en culture pure
Placer 1 ml de HdeuxOU ALORSdeux 3% sur une plaque pure ou une culture en coin qui ne contient pas de sang (de préférence gélose nutritive). Observez s'il y a ou non formation de bulles immédiatement. Vous pouvez également utiliser HdeuxOU ALORSdeux 30%.
Il est interprété de la même manière que la méthode d'objet porta.
-Tube capillaire ou méthode Fung et Petrishko
Remplir un tube capillaire de 67 mm à une hauteur de 20 mm avec 3% de peroxyde d'hydrogène par capillarité.
Touchez la colonie isolée à étudier avec le capillaire plein de HdeuxOU ALORSdeux à 3%. Observez si le capillaire se remplit de bulles en 10 secondes environ. Cette méthode permet une semi-quantification de la réaction en croisements:
Pas de croix, pas de bulles (réaction négative).
+ --Peu de bulles (réaction faible ou retardée).
++ -Bulles abondantes (réaction modérée).
+++ -Les bulles atteignent l'extrême opposé (réaction énergétique).
-Méthode de Taylor et Achanzar pour les tests de catalase douteux
Sur une lame propre et sèche, placez une colonie isolée, puis placez une goutte de HdeuxOU ALORSdeux 0,5% et couvrir avec une lamelle. Observez s'il y a ou non formation de bulles piégées.
Interprétation: la présence de bulles indique une réaction positive. Pas de bulles, cela est interprété comme une réaction négative.
Test de catalase pour les espèces de Mycobacterium
Cette technique doit être réalisée en contrôlant le pH et la température. Il doit être exécuté sous une hotte à flux laminaire, car la manipulation des différentes espèces de Mycobacterium est dangereuse.
-Matériaux
Peroxyde d'hydrogène 30% ou 110 volumes (superoxal).
Tampon phosphate pH 7
10% Tween 80
Culture en coin de Mycobacterium pendant 3 à 4 semaines
-préparation de réactifs
Tampon phosphate pH 7
Peser:
1,361 g (KHdeuxPO4) phosphate monopotassique anhydre.
1,420 g de phosphate disodique anhydre (Na2HPO3).
Dissoudre les deux sels dans un peu d'eau distillée stérile et compléter à 1000 ml avec de l'eau.
10% Tween 80
Faire une dilution 1:10 au Tween 80 qui est commercialement concentré, pour ce faire, procédez comme suit:
Prendre 1 ml de Tween 80 et le placer dans un peu d'eau distillée, dissoudre puis compléter le volume avec de l'eau jusqu'à 10 ml.
Réactif final
Mélanger une quantité de tampon phosphate avec une quantité de 10% Tween 80 (à parts égales). Définissez en laboratoire la quantité que vous souhaitez préparer.
-Traiter
Placer 5 ml de tampon phosphate dans un tube à essai stérile à bouchon à vis (bakélite).
Avec une boucle d'inoculation, prélever suffisamment de colonies d'une croissance de Mycobacterium ensemencée en quartiers et dissoudre dans le tampon phosphate.
Bouchez le tube sans trop serrer le fil. Placer au bain-marie à 68 ° C pendant 20 à 30 minutes. Retirer et refroidir à 22-25 ° C
Mesurez 0,5 ml du réactif final (mélange) et ajoutez-le au tube contenant la solution froide. Observer la formation ou non de bulles.
Il est interprété de la même manière que les techniques précédentes.
Utiliser
Lorsque la croissance des colonies est obtenue en milieu enrichi, une coloration de Gram et un test de catalase doivent être réalisés sur les colonies obtenues. Cela guidera le microbiologiste sur les procédures à suivre pour une identification définitive..

Contrôle de qualité
Pour évaluer les bonnes performances du réactif de peroxyde d'hydrogène, utilisez des souches de contrôle fraîchement cultivées, telles que Staphylococcus aureus comme contrôle positif et souches de Streptococcus sp comme contrôle négatif.
Une autre alternative qui sert de contrôle positif est de placer une goutte de peroxyde d'hydrogène sur la gélose au sang, les érythrocytes ont de la catalase, donc, il y aura un bullage si le réactif est en bon état.
Une gélose au chocolat peut être utilisée comme contrôle négatif, ici les érythrocytes sont déjà lysés et le test est négatif.
Limites
-N'utilisez pas d'anciennes cultures pour le test, car cela peut conduire à de faux négatifs.
-Évitez de prendre des colonies à partir de cultures de gélose au sang, si vous faites attention de ne pas toucher la gélose; cette procédure peut conduire à de faux positifs, car les érythrocytes contiennent de la catalase.
-Si vous prenez l'eau de Cologne en boucle de platine, n'inversez pas l'ordre de la procédure car cela peut conduire à de faux positifs. En effet, le platine est capable de réagir avec le peroxyde d'hydrogène, provoquant un bullage..
-N'utilisez pas le réactif de peroxyde d'hydrogène s'il est très ancien, car le réactif est très instable et a tendance à se dégrader avec le temps..
-Conservez le réactif de peroxyde d'hydrogène à l'abri de la lumière et réfrigéré pour éviter tout dommage..
-Effectuer un contrôle de qualité sur le réactif de peroxyde d'hydrogène à chaque fois qu'il est utilisé.
-Tenez compte du fait que si le HdeuxOU ALORSdeux à 30% les réactions sont plus fortes que celles réalisées avec HdeuxOU ALORSdeux à 3%.
Les références
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Diagnostic microbiologique. 5e éd. Éditorial Panamericana S.A. Argentine.
- Forbes B, Sahm D, Weissfeld A. (2009). Diagnostic microbiologique Bailey & Scott. 12 éd. Éditorial Panamericana S.A. Argentine.
- Mac Faddin J. (2003). Tests biochimiques pour l'identification des bactéries d'importance clinique. 3e éd. Éditorial Panamericana. Buenos Aires. Argentine.
- Laboratoires BD. Réactif Catalase-Gotario. Disponible sur: http://winklerltda.cl
- Laboratoires Vorrectímica. Eau oxygénée. Équivalence entre les volumes et le pourcentage. Disponible sur: v adéquatesimica.com



Personne n'a encore commenté ce post.