
Volume atomique Comment il varie dans le tableau périodique et les exemples
le volume atomique est une valeur relative qui indique la relation entre la masse molaire d'un élément et sa densité. Donc, ce volume dépend de la densité de l'élément, et la densité dépend à son tour de la phase et de la façon dont les atomes sont disposés en son sein..
Ainsi le volume atomique d'un élément Z n'est pas le même dans une phase autre que celle qu'il présente à température ambiante (liquide, solide ou gazeuse), ou lorsqu'il fait partie de certains composés. Ainsi, le volume atomique de Z dans le composé ZA est différent de celui de Z dans le composé ZB.

Parce que? Pour le comprendre, il est nécessaire de comparer des atomes avec, par exemple, des billes. Les billes, comme celles bleuâtres de l'image ci-dessus, ont une bordure de matière très bien définie, visible grâce à leur surface brillante. En revanche, la frontière des atomes est diffuse, bien qu'ils puissent être considérés comme sphériques à distance.
Ainsi, ce qui détermine un point au-delà de la frontière atomique est la probabilité nulle de trouver un électron, et ce point peut être plus ou plus proche du noyau en fonction du nombre d'atomes voisins interagissant autour de l'atome considéré..
Index des articles
- 1 Volume et rayon atomique
- 2 Formule supplémentaire
- 3 Comment le volume atomique varie-t-il dans le tableau périodique?
- 3.1 Volumes atomiques des métaux de transition
- 4 exemples
- 4.1 Exemple 1
- 4.2 Exemple 2
- 5 Références
Volume atomique et rayon
En interagissant avec deux atomes H dans la molécule Hdeux, les positions de leurs noyaux sont définies ainsi que les distances entre eux (distances internucléaires). Si les deux atomes sont sphériques, le rayon est la distance entre le noyau et la frontière floue:
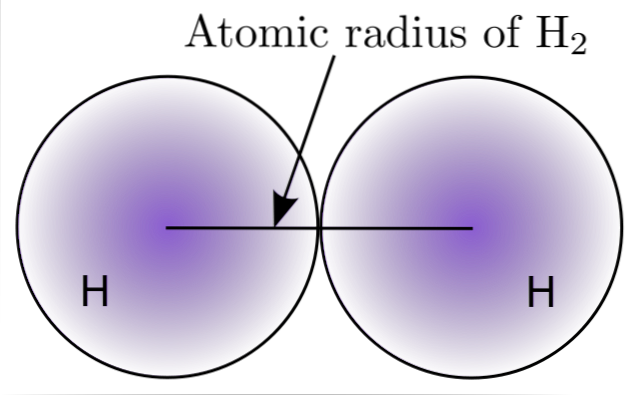
Dans l'image ci-dessus, vous pouvez voir comment la probabilité de trouver un électron diminue à mesure qu'il s'éloigne du noyau. Ensuite, en divisant la distance internucléaire par deux, le rayon atomique est obtenu. Ensuite, en supposant une géométrie sphérique pour les atomes, la formule est utilisée pour calculer le volume d'une sphère:
V = (4/3) (Pi) r3
Dans cette expression, r est le rayon atomique déterminé pour la molécule Hdeux. La valeur de V calculée par cette méthode imprécise peut changer si, par exemple, H est considérédeux à l'état liquide ou métallique. Cependant, cette méthode est très imprécise car les formes des atomes sont très éloignées de la sphère idéale dans leurs interactions..
Pour déterminer les volumes atomiques dans les solides, de nombreuses variables concernant la disposition sont prises en compte, et qui sont obtenues par diffraction des rayons X..
Formule supplémentaire
La masse molaire exprime la quantité de matière qui a une mole d'atomes d'un élément chimique.
Ses unités sont g / mol. Par contre, la densité est le volume qu'un gramme de l'élément occupe: g / mL. Puisque les unités de volume atomique sont en mL / mol, il faut jouer avec les variables pour arriver aux unités souhaitées:
(g / mol) (mL / g) = mL / mol
Ou qu'est-ce qui est pareil:
(Masse molaire) (1 / D) = V
(Masse molaire / D) = V
Ainsi, le volume d'une mole d'atomes d'un élément peut être facilement calculé; tandis qu'avec la formule du volume sphérique, le volume d'un atome individuel est calculé. Pour arriver à cette valeur à partir du premier, une conversion est nécessaire via le numéro d'Avogadro (6.02 · 10-2. 3).
Comment le volume atomique varie-t-il sur le tableau périodique?
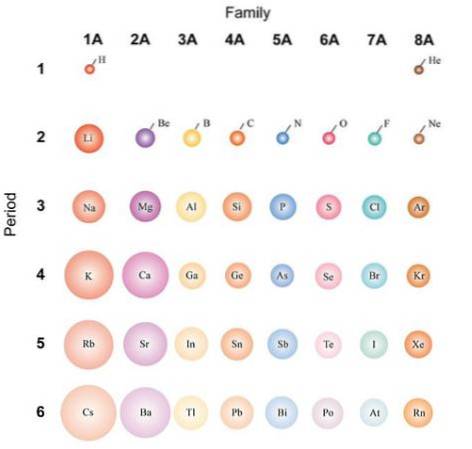
Si les atomes sont considérés comme sphériques, alors leur variation sera la même que celle observée dans les rayons atomiques. Dans l'image ci-dessus, qui montre des éléments représentatifs, il est illustré que de droite à gauche les atomes deviennent plus petits; au lieu de cela, de haut en bas, ils deviennent plus volumineux.
En effet, au cours de la même période, le noyau incorpore des protons lorsqu'il se déplace vers la droite. Ces protons exercent une force attractive sur les électrons externes, qui ressentent une charge nucléaire efficace Zef, inférieure à la charge nucléaire réelle Z.
Les électrons des coquilles intérieures repoussent ceux de la coquille extérieure, réduisant l'effet du noyau sur eux; c'est ce qu'on appelle l'effet d'écran. Dans la même période, l'effet d'écran ne peut pas contrecarrer l'augmentation du nombre de protons, de sorte que les électrons de la coque interne n'empêchent pas les atomes de se contracter..
Cependant, descendre dans un groupe permet de nouveaux niveaux d'énergie, ce qui permet aux électrons de s'orbiter plus loin du noyau. De même, le nombre d'électrons dans la coque interne augmente, dont les effets de blindage commencent à être diminués si le noyau ajoute à nouveau des protons..
Pour ces raisons, on apprécie que le groupe 1A possède les atomes les plus volumineux, contrairement aux petits atomes du groupe 8A (ou 18), celui des gaz rares..
Volumes atomiques des métaux de transition
Les atomes de métal de transition incorporent des électrons dans les orbitales d internes. Cette augmentation de l'effet d'écran et, ainsi que de la charge nucléaire réelle Z, s'annule presque également, de sorte que leurs atomes conservent une taille similaire dans la même période..
En d'autres termes: dans une période, les métaux de transition présentent des volumes atomiques similaires. Cependant, ces petites différences sont extrêmement importantes lors de la définition des cristaux métalliques (comme s'il s'agissait de billes métalliques).
Exemples
Deux formules mathématiques sont disponibles pour calculer le volume atomique d'un élément, chacune avec ses exemples correspondants.
Exemple 1
Compte tenu du rayon atomique de l'hydrogène -37 pm (1 picomètre = 10-12m) - et césium -265 pm-, calculez leurs volumes atomiques.
En utilisant la formule du volume sphérique, nous avons alors:
VH= (4/3) (3,14) (37 pm)3= 212.07 pm3
VCs= (4/3) (3,14) (265 pm)3= 77912297,67 pm3
Cependant, ces volumes exprimés en picomètres sont exorbitants, ils sont donc transformés en unités d'angströms, en les multipliant par le facteur de conversion (1Å / 100pm)3:
(21h073) (1 Å / 100 h)3= 2,1207 × 10-4 À3
(77912297,67 pm3) (1 Å / 100 h)3= 77,912 Å3
Ainsi, les différences de taille entre le petit atome H et l'atome volumineux Cs sont mises en évidence numériquement. Il faut garder à l'esprit que ces calculs ne sont que des approximations sous l'affirmation qu'un atome est totalement sphérique, qui erre devant la réalité.
Exemple 2

La densité de l'or pur est de 19,32 g / mL et sa masse molaire de 196,97 g / mol. En appliquant la formule M / D pour calculer le volume d'une mole d'atomes d'or, on obtient:
VAu= (196,97 g / mol) / (19,32 g / mL) = 10,19 mL / mol
Autrement dit, 1 mole d'atomes d'or occupe 10,19 ml, mais quel volume un atome d'or occupe-t-il spécifiquement? Et comment l'exprimer en unités de pm3? Pour cela, appliquez simplement les facteurs de conversion suivants:
(10,19 mL / mol) · (mol / 6,02 · 10-2. 3 atomes) · (1 m / 100 cm)3(13h / 10-12m)3= 16,92 · 106 après-midi3
En revanche, le rayon atomique de l'or est de 166 pm. Si les deux volumes sont comparés - celui obtenu par la méthode précédente et celui calculé avec la formule du volume sphérique - on constatera qu'ils n'ont pas la même valeur:
VAu= (4/3) (3,14) (166 pm)3= 19,15 · 106 après-midi3
Laquelle des deux est la plus proche de la valeur acceptée? Celui qui se rapproche le plus des résultats expérimentaux obtenus par diffraction des rayons X de la structure cristalline de l'or.
Les références
- Helmenstine, Anne Marie, Ph.D. (09 décembre 2017). Définition du volume atomique. Récupéré le 6 juin 2018 de: thinkco.com
- Mayfair, Andrew. (13 mars 2018). Comment calculer le volume d'un atome. Découvrir. Récupéré le 6 juin 2018 sur: scaimer.com
- Wiki Kids Ltd. (2018). Courbes de volume atomique de Lothar Meyer. Récupéré le 6 juin 2018 de: wonderwhizkids.com
- Lumen. Tendances périodiques: rayon atomique. Extrait le 6 juin 2018 de: courses.lumenlearning.com
- Camilo J. Derpich. Volume atomique et densité. Récupéré le 6 juin 2018 de: es-puraquimica.weebly.com
- Whitten, Davis, Peck et Stanley. Chimie. (8e éd.). Apprentissage CENGAGE, p 222-224.
- Fondation CK-12. (22 février 2010). Tailles atomiques comparatives. [Chiffre]. Extrait le 6 juin 2018 de: commons.wikimedia.org
- Fondation CK-12. Édition (22 février 2010). Rayon atomique de Hdeux. [Chiffre]. Extrait le 6 juin 2018 de: commons.wikimedia.org


Personne n'a encore commenté ce post.