
Structure de l'adénine, biosynthèse, fonctions
La adénine Il s'agit d'une base azotée de type purine, présente dans les acides ribonucléiques (ARN) et désoxyribonucléiques (ADN) d'organismes vivants et de virus. Certaines des fonctions de ces biopolymères (ARN et ADN) sont le stockage, la réplication, la recombinaison et le transfert d'informations génétiques.
Pour constituer des acides nucléiques, l'atome d'azote 9 de l'adénine forme d'abord une liaison glycosidique avec le premier carbone 1 (C1 ') du ribose (d'ARN) ou du 2'-désoxyribose (d'ADN). De cette manière, l'adénine forme le nucléoside adénosine ou adénosine.
Deuxièmement, le groupe hydroxyle (-OH) du carbone 5 'du sucre (ribose ou 2'-désoxyribose), de l'adénosine, forme une liaison ester avec un groupe phosphate..
Dans les cellules vivantes, selon le nombre de groupes phosphate présents, il peut s'agir d'adénosine-5'-monophosphate (AMP), d'adénosine-5'-diphosphate (ADP) et d'adénosine-5'-triphosphate (ATP). Des équivalents possédant du 2'-désoxyribose existent également. Par exemple, le désoxyadénosine-5'-monophosphate (dAMP), etc..
Index des articles
- 1 Structure et caractéristiques
- 2 Biosynthèse
- 3 Rôles dans le métabolisme oxydatif et réducteur
- 4 Fonctions dans l'expression génique
- 5 Fonctions du métabolisme énergétique
- 6 Autres fonctions
- 7 Synthèse prébiotique
- 8 Utilisation comme facteur thérapeutique et de culture cellulaire
- 9 Références
Structure et caractéristiques
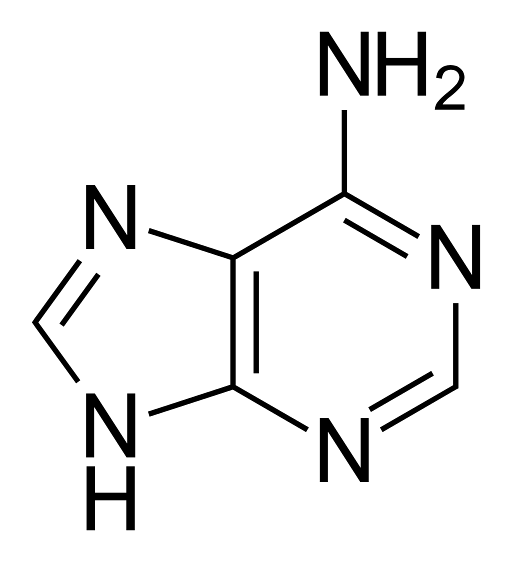
L'adénine, appelée 6-aminopurine, a la formule empirique C5H5N5, et a un poids moléculaire de 135,13 g / mol, étant purifié sous forme d'un solide jaune pâle, avec un point d'ébullition de 360 ° C..
Sa molécule a une structure chimique à double cycle avec des doubles liaisons conjuguées, qui est la fusion d'une pyrimidine avec un groupe imidazole. Pour cette raison, l'adénine est une molécule hétérocyclique plate..
Il a une solubilité relative de 0,10 g / mL (à 25 ºC), dans des solutions aqueuses acides et basiques, avec un pKa de 4,15 (à 25 ºC).
Pour cette même raison, il est susceptible d'être détecté par absorbance à 263 nm (avec un coefficient d'absorption de E1,2 mM = 13,2 millions-1.cm-1 dans 1,0 M HCl), aire du spectre électromagnétique correspondant au proche ultraviolet.
Biosynthèse
La biosynthèse des nucléotides puriques est identique chez pratiquement tous les êtres vivants. Il commence par le transfert d'un groupe amino de la glutamine au substrat 5-phosphoribosyl-1-pyrophosphate (PRPP) et produit de la 5-phosphoribosylamine (PRA).
Il s'agit d'une réaction catalysée par la glutamine-PRPP transférase, une enzyme clé dans la régulation de cette voie métabolique..
Après des ajouts séquentiels des acides aminés glutamine, glycine, méthényl-folate, aspartate, Ndix-le formyl-folate en PRA, y compris les condensations et la cyclisation, est produit de l'inosine-5'-monophosphate (IMP), dont l'unité hétérocyclique est l'hypoxanthine (6-oxypurine).
Ces ajouts sont entraînés par l'hydrolyse de l'ATP en ADP et en phosphate inorganique (Pi). Par la suite, un groupe amino de l'aspartate est ajouté à l'IMP, dans une réaction couplée à l'hydrolyse de la guanosine-triphosphate (GTP), pour finalement générer de l'AMP.
Ce dernier exerce le contrôle de cette voie de biosynthèse par rétroaction négative, agissant sur les enzymes qui catalysent la formation de PRA et la modification de l'IMP.
Comme pour la dégradation d'autres nucléotides, la base azotée des nucléotides adénosine passe par un processus appelé «recyclage».
Le recyclage consiste en le transfert d'un groupe phosphate du PRPP à l'adénine et forme de l'AMP et du pyrophosphate (PPi). Il s'agit d'une seule étape catalysée par l'enzyme adénine phosphoribosyltransférase.
Rôles dans le métabolisme oxydatif et réducteur
L'adénine fait partie de plusieurs molécules importantes du métabolisme oxydatif, qui sont les suivantes:
- Flavin adénine dinucléotide (FAD / FADHdeux) et le nicotinamide adénine dinucléotide (NAD+/ NADH), qui participent aux réactions d'oxydoréduction transférant des ions hydrure (: H-).
- Coenzyme A (CoA), qui participe à l'activation et au transfert des groupes acyle.
Au cours du métabolisme oxydatif, le NAD+ il fonctionne comme un substrat accepteur d'électrons (ions hydrure) et forme du NADH. Alors que FAD est un cofacteur qui accepte les électrons et devient FADHdeux.
D'autre part, l'adénine forme le nicotinamide adénine dinucléotide phosphate (NADP+/ NADPH), qui intervient dans la réduction du métabolisme. Par exemple, le NADPH est un substrat donneur d'électrons lors de la biosynthèse des lipides et des désoxyribonucléotides..
L'adénine fait partie des vitamines. Par exemple, la niacine est le précurseur du NAD+ et NADP+ et la riboflavine est le précurseur de la FAD.
Fonctions dans l'expression génique
L'adénine fait partie de la S-adénosylméthionine (SAM), qui est un donneur de radical méthyle (-CH3) et participe à la méthylation des résidus adénine et cytosine chez les procaryotes et les eucaryotes.
Chez les procaryotes, la méthylation fournit son propre système de reconnaissance d'ADN, protégeant ainsi l'ADN de ses propres enzymes restrictives..
Chez les eucaryotes, la méthylation détermine l'expression des gènes; c'est-à-dire qu'il établit quels gènes devraient être exprimés et lesquels ne devraient pas être exprimés. De plus, les méthylations d'adénine peuvent marquer les sites de réparation de l'ADN endommagé..
De nombreuses protéines qui se lient à l'ADN, comme les facteurs de transcription, ont des résidus d'acides aminés glutamine et asparagine qui forment des liaisons hydrogène avec l'atome N.7 d'adénine.
Fonctions du métabolisme énergétique
L'adénine fait partie de l'ATP, qui est une molécule à haute énergie; c'est-à-dire que son hydrolyse est exergonique et que l'énergie libre de Gibbs est une valeur élevée et négative (-7,0 Kcal / mol). Dans les cellules, l'ATP participe à de nombreuses réactions qui nécessitent de l'énergie, telles que:
- Stimuler les réactions chimiques endergoniques catalysées par des enzymes impliquées dans le métabolisme intermédiaire et l'anabolisme, par la formation d'intermédiaires à haute énergie ou de réactions couplées.
- Promouvoir la biosynthèse des protéines dans les ribosomes, en permettant l'estérification des acides aminés avec leur ARN de transfert correspondant (ARNt), pour former un aminoacyl-ARNt.
- Augmentez le mouvement des produits chimiques à travers les membranes cellulaires. Il existe quatre types de protéines de transport: P, F, V et ABC. Les types P, F et V portent des ions et le type ABC porte des substrats. Par exemple, Na ATPase+/ K+, classe P, vous avez besoin d'un ATP pour pomper dans la cellule deux K+ et sur trois Na+.
- Stimule la contraction musculaire. Fournit l'énergie qui dirige le glissement du filament d'actine sur la myosine.
- Boostez le transport nucléaire. Lorsque la sous-unité bêta du récepteur hétérodimérique se lie à l'ATP, elle interagit avec les composants du complexe des pores nucléaires.
Autres fonctions
L'adénosine sert de ligand pour les protéines réceptrices présentes dans les neurones et les cellules de l'épithélium intestinal, où elle agit comme un messager extracellulaire ou neuromodulateur, lorsque des changements se produisent dans le métabolisme énergétique cellulaire.
L'adénine est présente dans de puissants agents antiviraux tels que l'arabinosiladénine (araA), qui est produite par certains micro-organismes. De plus, il est présent dans la puromycine, un antibiotique qui inhibe la biosynthèse des protéines et est produit par des microorganismes du genre Streptomyces.
Dans l'AMP, il sert de substrat pour les réactions qui génèrent le second AMP cyclique messager (AMPc). Ce composé, produit par l'enzyme adénylate cyclase, est essentiel dans une grande partie des cascades de signalisation intracellulaire, nécessaires à la prolifération et à la survie des cellules, ainsi qu'à l'inflammation et à la mort cellulaire..
Le sulfate à l'état libre n'est pas réactif. Une fois qu'il entre dans la cellule, il devient adénosine-5'-phosphosulfate (APS), puis 3'-phosphoadénosine-5'-phosphosulfate (PAPS). Chez les mammifères, PAPS est le donneur de groupes sulfate et forme des esters de sulfate organiques tels que ceux de l'héparine et de la chondroïtine..
Dans la biosynthèse de la cystéine, la S-adénosylméthionine (SAM) sert de précurseur pour la synthèse de la S-adénosylhomocystéine, qui est transformée en plusieurs étapes, catalysées par des enzymes, en cystéine..
Synthèse prébiotique
Expérimentalement, il a été démontré que la conservation du cyanure d'hydrogène (HCN) et de l'ammoniac (NH3), dans des conditions de laboratoire similaires à celles qui prévalaient au début de la Terre, de l'adénine est produite dans le mélange résultant. Cela se produit sans la nécessité de la présence de cellules vivantes ou de matériel cellulaire..
Les conditions prébiotiques comprennent l'absence d'oxygène moléculaire libre, une atmosphère hautement réductrice, un rayonnement ultraviolet intense, de grands arcs électriques tels que ceux générés lors des tempêtes et des températures élevées. Cela suppose que l'adénine était la base azotée principale et la plus abondante formée au cours de la chimie prébiotique..
Ainsi, la synthèse de l'adénine constituerait une étape clé qui rendrait possible l'origine des premières cellules. Ceux-ci devaient avoir une membrane qui formait un compartiment fermé, à l'intérieur duquel se trouveraient les molécules nécessaires à la construction des premiers polymères biologiques nécessaires à l'auto-perpétuation..
Utilisation comme facteur thérapeutique et de culture cellulaire
L'adénine est, avec d'autres composés chimiques organiques et inorganiques, un ingrédient essentiel de la recette utilisée dans tous les laboratoires de biochimie, de génétique, de biologie moléculaire et de microbiologie dans le monde, pour faire croître des cellules viables au fil du temps..
En effet, les variétés de cellules normales sauvages peuvent détecter et capturer l'adénine disponible dans l'environnement environnant et l'utiliser pour synthétiser leurs propres nucléosides adénine..
Il s'agit d'une forme de survie cellulaire, qui économise des ressources internes en synthétisant des molécules biologiques plus complexes à partir de simples précurseurs prélevés de l'extérieur..
Dans des modèles expérimentaux de maladie rénale chronique, les souris ont une mutation dans le gène de l'adénine phosphoribosyltransférase qui produit une enzyme inactive. Ces souris reçoivent des solutions commerciales contenant de l'adénine, du citrate de sodium et du glucose, par voie intraveineuse, pour favoriser leur récupération rapide..
Ce traitement repose sur le fait que le PRPP, le métabolite initial de la biosynthèse des purines, est synthétisé à partir du ribose-5-phosphate par la voie du pentose phosphate, dont le métabolite de départ est le glucose-6-phosphate. Cependant, bon nombre de ces solutions ne sont pas approuvées par les organismes de réglementation internationaux pour un usage humain..
Les références
- Burnstock, G. 2014. Purines et purinocepteurs. Présentation de la biologie moléculaire. Références Modules en sciences biomédicales. Adresse Word Wide Web: https://doi.org/10.1016/B978-0-12-801238-3.04741-3
- Claramount, D. et coll. 2015. Modèles animaux de maladies chroniques pédiatriques. Néphrologuejeà,35 (6): 517-22.
- Coade, S. et Pearson, J. 1989. Métabolisme des nucléotides adénine. Recherche sur la circulation, 65: 531-37
- Dawson, R. et coll. 1986. Données pour la recherche biochimique. Clarendon Press, Oxford.
- DrougBank. 2019. Fiche Adenine Chemichal. Adresse Web Word Wide: https://www.drugbank.ca/drugs/DB00173
- Horton, R; Moran, L; Scrimgeour, G; Perry, M. et Rawn, D. 2008. Principes de biochimie. 4e édition. Éducation Pearson.
- Knight, G. 2009. Récepteurs purinergiques. Encyclopédie des neurosciences. 1245-52. Adresse Word Wide Web: https://doi.org/10.1016/B978-008045046-9.00693-8
- Mathews, Van Holde, Ahern. 2001. Biochimie. 3e édition.
- Murgola, E. 2003. Adenine. Encyclopédie de la génétique. Adresse Word Wide Web: https://doi.org/10.1006/rwgn.2001.0008
- Murray, R; Granner, D; Mayes, P. et Rodwell, V. 2003. La biochimie illustrée de Harper. 26e Édition. Entreprises McGraw-Hill.
- Nelson, DL et Cox, M. 1994. Lehninger. Principes de biochimie. 4e édition. Ed Omega.
- Sigma-Aldrich. 2019. Fiche chimique Adenine. Adresse Word Wide Web: https://www.sigmaaldrich.com/catalog/product/aldrich/ga8626?lang=en



Personne n'a encore commenté ce post.