
Caractéristiques et exemples de carbone anomérique
le carbone anomérique c'est un stéréocentre présent dans les structures cycliques des glucides (mono ou polysaccharides). Étant un stéréocentre, plus précisément un épimère, on en dérive deux diastéréoisomères, désignés par les lettres α et β; ce sont les anomères, et font partie de la nomenclature étendue dans le monde des sucres.
Chaque anomère, α ou β, diffère par la position du groupe OH du carbone anomérique par rapport au cycle; mais dans les deux, le carbone anomérique est le même, et il est situé au même endroit dans la molécule. Les anomères sont des hémiacétals cycliques, le produit d'une réaction intramoléculaire dans la chaîne ouverte des sucres; que ce soit des aldoses (aldéhydes) ou des cétoses (cétones).
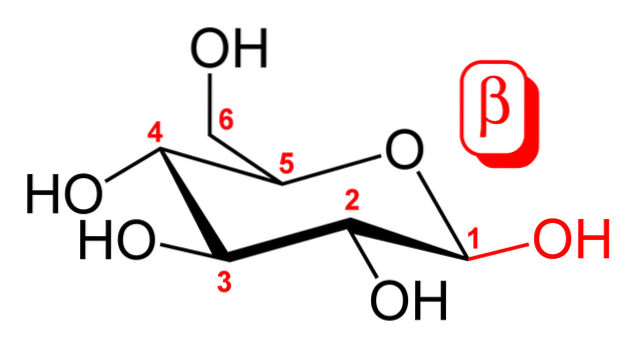
L'image du haut montre la conformation de la chaise pour le β-D-glucopyranose. Comme on peut le voir, il est constitué d'un cycle à six chaînons, comprenant un atome d'oxygène entre les carbones 5 et 1; ce dernier, ou plutôt le premier, est le carbone anomérique, qui forme deux liaisons simples avec deux atomes d'oxygène.
Si vous regardez de près, le groupe OH attaché au carbone 1 est orienté au-dessus de l'anneau hexagonal, tout comme le groupe CHdeuxOH (carbone 6). C'est l'anomère β. L'anomère α, d'autre part, ne différerait que dans ce groupe OH, qui serait situé en bas de l'anneau, tout comme s'il s'agissait d'un diastéréoisomère trans..
Index des articles
- 1 hémiacétals
- 1.1 Hémiacétal cyclique
- 2 Caractéristiques du carbone anomérique et comment le reconnaître
- 3 exemples
- 3.1 Exemple 1
- 3.2 Exemple 2
- 3.3 Exemple 3
- 4 Références
Hémiacétals
Il est nécessaire d'approfondir un peu le concept d'hémiacétals pour mieux comprendre et distinguer le carbone anomérique. Les hémiacétals sont le produit d'une réaction chimique entre un alcool et un aldéhyde (aldoses) ou une cétone (cétoses).
Cette réaction peut être représentée par l'équation chimique générale suivante:
ROH + R'CHO => ROCH (OH) R '
Comme on peut le voir, un alcool réagit avec un aldéhyde pour former l'hémiacétal. Que se passerait-il si R et R 'appartenaient à la même chaîne? Dans ce cas, vous auriez un hémiacétal cyclique, et la seule façon possible de le former est que les deux groupes fonctionnels, -OH et -CHO, sont présents dans la structure moléculaire..
De plus, la structure doit être constituée d'une chaîne flexible, et de liaisons capables de faciliter l'attaque nucléophile de l'OH vers le carbone carbonyle du groupement CHO. Lorsque cela se produit, la structure se ferme en un anneau à cinq ou six chaînons..
Hémiacétal cyclique
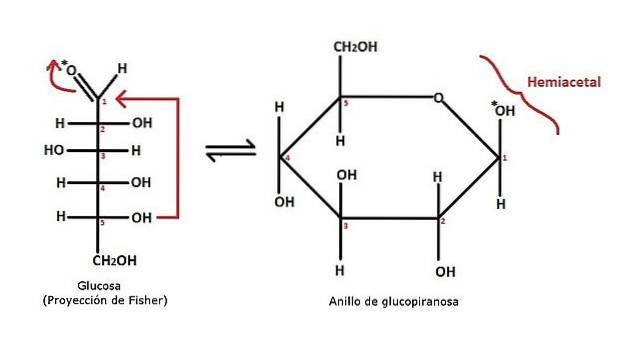
Un exemple de la formation d'un hémiacétal cyclique pour le monosaccharide de glucose est montré dans l'image ci-dessus. On peut voir qu'il s'agit d'un aldose, avec un groupe aldéhyde CHO (carbone 1). Celui-ci est attaqué par le groupe OH du carbone 5, comme indiqué par la flèche rouge.
La structure passe d'une chaîne ouverte (glucose) à un anneau pyraneux (glucopyranose). Au début, il peut n'y avoir aucune relation entre cette réaction et celle qui vient d'être expliquée pour l'hémiacétal; mais si vous regardez attentivement l'anneau, en particulier dans la section C5-O-C1(OH) -Cdeux, on appréciera que cela correspond au squelette attendu pour un hémiacétal.
Les carbones 5 et 2 représentent respectivement R et R 'de l'équation générale. Comme ceux-ci font partie de la même structure, il s'agit alors d'un hémiacétal cyclique (et l'anneau suffit pour être évident).
Caractéristiques du carbone anomérique et comment le reconnaître
Où est le carbone anomérique? Dans le glucose, il s'agit du groupe CHO, qui peut subir une attaque nucléophile par OH soit par le bas, soit par le haut. Selon l'orientation de l'attaque, deux anomères différents se forment: α et β, comme déjà évoqué..
Par conséquent, une première caractéristique que possède ce carbone est que dans la chaîne ouverte du sucre, c'est celui qui subit l'attaque nucléophile; c'est-à-dire que c'est le groupe CHO, pour les aldoses, ou le groupe RdeuxC = O, pour les cétoses. Cependant, une fois que l'hémiacétal cyclique ou le cycle est formé, ce carbone peut sembler avoir disparu..
C'est là qu'il existe d'autres caractéristiques plus spécifiques pour le localiser dans tout anneau pyraneux ou furaneux de tous les glucides:
-Le carbone anomérique est toujours à droite ou à gauche de l'atome d'oxygène qui compose l'anneau.
-Plus important encore, il est lié non seulement à cet atome d'oxygène, mais aussi au groupe OH, provenant de CHO ou RdeuxC = O.
-Il est asymétrique, c'est-à-dire qu'il a quatre substituants différents.
Avec ces quatre caractéristiques, il est facile de reconnaître le carbone anomérique en regardant n'importe quelle «structure douce».
Exemples
Exemple 1
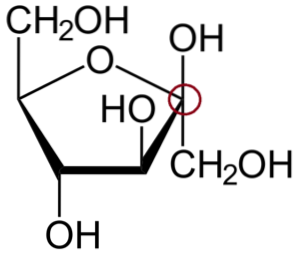
Ci-dessus se trouve le β-D-fructofuranose, un hémiacétal cyclique avec un cycle à cinq chaînons..
Pour identifier le carbone anomérique, vous devez d'abord regarder les carbones sur les côtés gauche et droit de l'atome d'oxygène qui compose l'anneau. Ensuite, celui qui est lié au groupe OH est le carbone anomérique; qui dans ce cas, est déjà cerclé de rouge.
Il s'agit de l'anomère β car l'OH du carbone anomère est au-dessus du cycle, tout comme le groupe CHdeuxOh.
Exemple 2
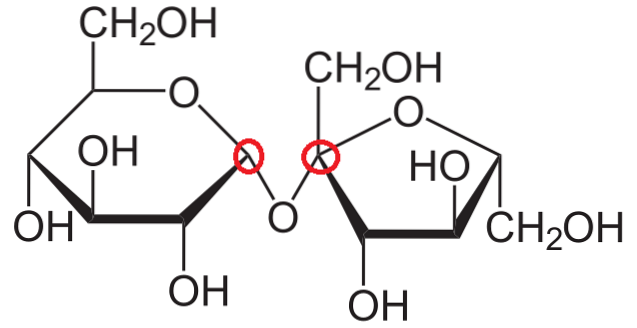
Maintenant, nous essayons d'expliquer quels sont les carbones anomères dans la structure du saccharose. Comme on peut le voir, il se compose de deux monosaccharides liés de manière covalente par une liaison glycosidique, -O-.
L'anneau de droite est exactement le même que celui que nous venons de mentionner: le β-D-fructofuranose, seulement il est «retourné» vers la gauche. Le carbone anomérique reste le même pour le cas précédent, et répond à toutes les caractéristiques que l'on en attendrait.
En revanche, l'anneau de gauche est l'α-D-glucopyranose.
En répétant la même procédure de reconnaissance de carbone anomérique, en regardant les deux carbones sur le côté gauche et droit de l'atome d'oxygène, on constate que le carbone droit est celui qui est lié au groupe OH; qui participe à la liaison glycosidique.
Par conséquent, les deux carbones anomères sont reliés par la liaison -O- et sont donc entourés de cercles rouges..
Exemple 3
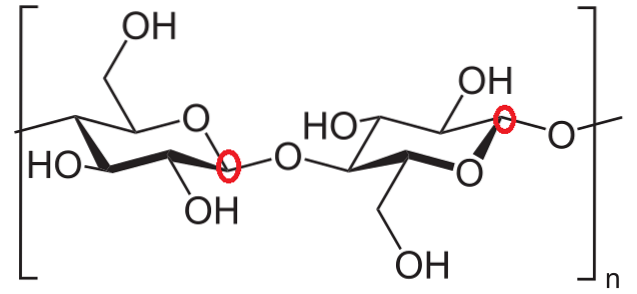
Enfin, il est proposé d'identifier les carbones anomères de deux unités glucose dans la cellulose. Encore une fois, les carbones autour de l'oxygène dans le cycle sont observés, et on constate que dans le cycle glucose à gauche, le carbone anomérique participe à la liaison glycosidique (entourée du cercle rouge).
Dans le cycle glucose à droite, cependant, le carbone anomérique est à droite de l'oxygène et est facilement identifié car il est lié à l'oxygène de la liaison glycosidique. Ainsi, les deux carbones anomères sont entièrement identifiés.
Les références
- Morrison, R. T. et Boyd, R, N. (1987). Chimie organique. 5ta Édition. Éditorial Addison-Wesley Interamericana.
- Carey F. (2008). Chimie organique. (Sixième édition). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chimie organique. Amines. (dixe édition.). Wiley plus.
- Rendina G. (1974). Techniques de biochimie appliquées. Interamericana, Mexique.
- Chang S. (s.f.). Un guide sur le carbone anomérique: qu'est-ce qu'un carbone anomérique? [PDF]. Récupéré de: chem.ucla.edu
- Gunawardena G. (13 mars 2018). Charbon anomérique. Chimie LibreTexts. Récupéré de: chem.libretexts.org
- Foist L. (2019). Carbone anomérique: définition et aperçu. Étude. Récupéré de: study.com



Personne n'a encore commenté ce post.