
Structure chimique, propriétés et utilisations du carbure de silicium

le Carbure de silicium C'est un solide covalent composé de carbone et de silicium. Il est d'une grande dureté avec une valeur de 9,0 à 10 sur l'échelle de Mohs, et sa formule chimique est SiC, ce qui peut suggérer que le carbone est lié au silicium par une triple liaison covalente, avec une charge positive (+) sur Si et un charge négative (-) sur le carbone (+Oui≡C-).
En fait, les liaisons de ce composé sont totalement différentes. Il a été découvert en 1824 par le chimiste suédois Jön Jacob Berzelius, alors qu'il tentait de synthétiser des diamants. En 1893, le scientifique français Henry Moissani a découvert un minéral dont la composition contenait du carbure de silicium.

Cette découverte a été faite en examinant des échantillons de roche provenant du cratère d'une météorite dans Devil's Canyon, aux États-Unis. Il a nommé ce minéral moissanite. D'autre part, Edward Goodrich Acheson (1894) a créé une méthode pour synthétiser du carbure de silicium, en faisant réagir du sable ou du quartz de haute pureté avec du coke de pétrole..
Goodrich a nommé le produit obtenu carborundum (ou carborundium) et a fondé une entreprise pour produire des abrasifs.
Index des articles
- 1 Structure chimique
- 2 propriétés
- 2.1 Propriétés générales
- 2.2 Propriétés thermiques
- 2.3 Propriétés mécaniques
- 2.4 Propriétés électriques
- 3 utilisations
- 3.1 En tant qu'abrasif
- 3.2 Sous forme de céramique structurée
- 3.3 Autres utilisations
- 4 Références
Structure chimique
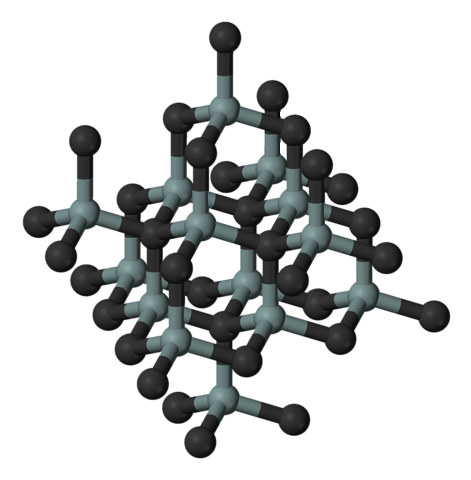
L'image ci-dessus illustre la structure cubique et cristalline du carbure de silicium. Cette disposition est la même que celle du diamant, malgré les différences de rayons atomiques entre C et Si..
Toutes les liaisons sont fortement covalentes et directionnelles, contrairement aux solides ioniques et à leurs interactions électrostatiques.
SiC forme des tétraèdres moléculaires; c'est-à-dire que tous les atomes sont liés à quatre autres. Ces unités tétraédriques sont reliées entre elles par des liaisons covalentes, adoptant des structures cristallines en couches..
En outre, ces couches ont leurs propres arrangements cristallins, qui sont de trois types: A, B et C.
C'est-à-dire qu'une couche A est différente de B, et cette dernière de C. Ainsi, le cristal de SiC consiste en l'empilement d'une séquence de couches, le phénomène connu sous le nom de polytypisme se produisant..
Par exemple, le polytype cubique (similaire à celui du diamant) est constitué d'un empilement de couches ABC et a donc une structure cristalline 3C..
D'autres empilements de ces couches génèrent également d'autres structures, entre ces polytypes rhomboédriques et hexagonaux. En fait, les structures cristallines du SiC finissent par être un "trouble cristallin".
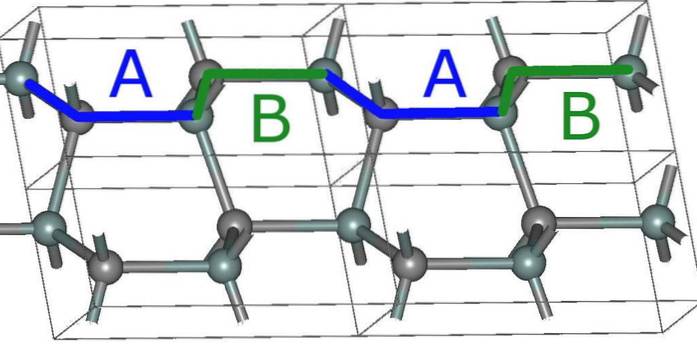
La structure hexagonale la plus simple pour SiC, la 2H (image du haut), est formée à la suite de l'empilement des couches avec la séquence ABABA ... Après toutes les deux couches, la séquence se répète, et c'est de là que vient le nombre 2.
Propriétés
Les propriétés générales
Masse molaire
40,11 g / mol
Apparence
Cela varie selon la méthode d'obtention et les matériaux utilisés. Il peut s'agir de cristaux jaunes, verts, bleus noirâtres ou irisés.
Densité
3,16 g / cm3
Point de fusion
2830 ºC.
Indice de réfraction
2,55.
Cristaux
Il y a polymorphisme: cristaux hexagonaux αSiC et cristaux cubiques βSiC.
Dureté
9 à 10 sur l'échelle de Mohs.
Résistance aux agents chimiques
Il résiste à l'action des acides forts et des alcalis. De plus, le carbure de silicium est chimiquement inerte..
Propriétés thermiques
- Conductivité thermique élevée.
- Résiste à des températures élevées.
- Conductivité thermique élevée.
- Faible coefficient de dilatation thermique linéaire, donc il résiste à des températures élevées avec une faible dilatation.
- Résistant aux chocs thermiques.
Propriétés mécaniques
- Haute résistance à la compression.
- Résistant à l'abrasion et à la corrosion.
- C'est un matériau léger de grande solidité et résistance.
- Conserve sa résistance élastique aux températures élevées.
Propriétés électrique
C'est un semi-conducteur qui peut remplir ses fonctions à des températures élevées et des tensions extrêmes, avec une faible dissipation de sa puissance au champ électrique..
Applications
Comme abrasif
- Le carbure de silicium est un semi-conducteur capable de résister à des températures élevées, à des gradients de haute tension ou à un champ électrique 8 fois plus que ce que le silicium peut supporter. Pour cette raison, il est utile dans la construction de diodes, de transiteurs, de suppresseurs et de dispositifs hyperfréquences à haute énergie..
- Des diodes électroluminescentes (LED) et des détecteurs pour les premières radios (1907) ont été fabriqués avec le composé. Actuellement, le carbure de silicium a été remplacé dans la fabrication des ampoules LED par du nitrure de gallium, qui émet une lumière 10 à 100 fois plus brillante..
- Dans les systèmes électriques, le carbure de silicium est utilisé comme paratonnerre dans les systèmes d'alimentation électrique, car ils peuvent réguler sa résistance en régulant la tension à travers lui..
Sous forme de céramique structurée
- Dans un procédé appelé frittage, les particules de carbure de silicium - ainsi que celles des compagnons - sont chauffées à une température inférieure à la température de fusion de ce mélange. Ainsi, il augmente la résistance et la résistance de l'objet en céramique, grâce à la formation de liaisons fortes entre les particules..
- Les céramiques structurales en carbure de silicium ont eu une vaste gamme d'applications. Ils sont utilisés dans les freins à disque et les embrayages de véhicules automobiles, dans les filtres à particules diesel et comme additif dans les huiles pour réduire les frottements.
- Les utilisations des céramiques structurales en carbure de silicium se sont généralisées dans les pièces exposées à des températures élevées. C'est par exemple le cas de la gorge des injecteurs de fusée et des rouleaux des fours..
- La combinaison d'une conductivité thermique élevée, d'une ténacité et d'une stabilité à haute température permet de fabriquer des composants pour tubes d'échangeurs de chaleur en carbure de silicium..
- La céramique structurelle est utilisée dans les injecteurs de sablage, les joints de pompe à eau automobile, les roulements et les matrices d'extrusion. C'est aussi le matériau des creusets, utilisé dans la fonte des métaux..
- Il fait partie des éléments chauffants utilisés dans la fusion du verre et des métaux non ferreux, ainsi que dans le traitement thermique des métaux.
Autres utilisations
- Il peut être utilisé dans la mesure de la température des gaz. Dans une technique connue sous le nom de pyrométrie, un filament de carbure de silicium est chauffé et émet un rayonnement qui est en corrélation avec la température dans une plage de 800-2500 ºK..
- Il est utilisé dans les centrales nucléaires pour éviter les fuites de matières produites par la fission.
- Dans la production d'acier, il est utilisé comme combustible.
Les références
- Nicholas G. Wright, Alton B. Horsfall. Carbure de silicium: le retour d'un vieil ami. Material Matters Volume 4 Article 2. Extrait le 5 mai 2018 de: sigmaaldrich.com
- John Faithfull. (Février 2010). Cristaux de carborundum. Extrait le 5 mai 2018 de: commons.wikimedia.org
- Charles et Colvard. Polytypisme et Moissanite. Récupéré le 5 mai 2018 de: moissaniteitalia.com
- Scientifique des matériaux. (2014). SiC2HstructureA. [Chiffre]. Extrait le 5 mai 2018 de: commons.wikimedia.org
- Wikipédia. (2018). Carbure de silicium. Extrait le 5 mai 2018 de: en.wikipedia.org
- Navarro SiC. (2018). Carbure de silicium. Récupéré le 5 mai 2018 de: navarrosic.com
- Université de Barcelone. Carbure de silicium, SiC. Récupéré le 5 mai 2018 de: ub.edu
- CarboSystem. (2018). Carbure de silicium. Extrait le 5 mai 2018 de: carbosystem.com



Personne n'a encore commenté ce post.