
Structure de l'acide laurique, propriétés, utilisations, avantages, effets
le l'acide laurique C'est un acide gras saturé à 12 atomes de carbone à chaîne moyenne. Il se compose d'une poudre blanche solide ou blanche brillante, avec une odeur caractéristique d'huile pour bébé. Il est pratiquement insoluble dans l'eau, mais il est très soluble dans les solvants organiques; notamment dans l'éthanol, le méthanol et l'acétone.
C'est l'un des composants des triglycérides. Le lait de coco est très riche en cet acide gras (environ 50% des acides gras). On le trouve également dans l'huile de coco et l'huile de palmiste. Dans le lait maternel, il représente 6,2% des lipides totaux.

L'acide laurique est métabolisé pour donner naissance à la monolaurine, un composé auquel une activité contre les bactéries très négatives, les virus, les champignons et les protozoaires est attribuée..
L'acide laurique s'est avéré utile dans le traitement de l'acné, car il a une activité contre les bactéries Propionibacterium acnes, liés aux processus inflammatoires observés dans le trouble.
De même, il a été utilisé expérimentalement dans des cultures de cellules cancéreuses rectales du côlon, pouvant induire l'apoptose de ces cellules; qui pourrait ouvrir la porte à l'utilisation de l'acide laurique dans une thérapie alternative pour ce type de cancer
En résumé, l'acide laurique présente de nombreux avantages pour la santé, étant également utilisé dans la préparation de cosmétiques, de parfums, de savons, de shampooings, etc..
Index des articles
- 1 Structure de l'acide laurique
- 2 propriétés
- 2.1 Noms chimiques
- 2.2 Formule moléculaire
- 2.3 Poids moléculaire
- 2.4 Description physique
- 2.5 Odeur
- 2.6 Point de fusion
- 2.7 Point d'ébullition
- 2.8 Solubilité dans l'eau
- 2.9 Solubilité dans les solvants organiques
- 2.10 Densité
- 2.11 Pression de vapeur
- 2.12 Viscosité
- 2.13 Chaleur de combustion
- 2.14 Tension superficielle
- 2.15 Indice de réfraction
- 2.16 Constante de dissociation
- 3 utilisations
- 3.1 Industriel
- 3.2 Détermination de la masse molaire
- 3.3 Agriculture
- 4 bienfaits pour la santé
- 4.1 Greffes de pontage vasculaire
- 4.2 Augmente l'action de certains médicaments
- 4.3 Action bactéricide
- 4.4 Traitement du côlon rectal
- 4.5 Combattre les infections et les agents pathogènes
- 4.6 Autres
- 5 effets secondaires
- 6 Références
Structure de l'acide laurique
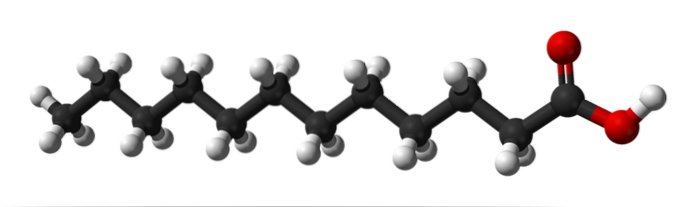
L'image du haut montre la structure moléculaire de l'acide laurique à l'aide d'un modèle de sphères et de barres..
On peut compter que dans sa «queue» de carbone il y a onze atomes de carbone ou sphères noires; il constitue l'extrémité apolaire ou hydrophobe de la structure. Et à sa droite, la tête polaire avec le groupe COOH, avec ses sphères rouges. Il y a douze atomes de carbone en tout.
Le groupe COOH peut donner un ion H+, formant des sels de laurates. Dans ceux-ci, l'hydrogène du groupe OH, situé à l'extrémité droite, est remplacé par des cations métalliques.
La queue apolaire de l'acide laurique est exempte d'insaturations. Que signifie? Manque de doubles liaisons (C = C). Si c'était le cas, il aurait des plis, caractéristiques des graisses insaturées. Tous les carbones sont liés au nombre maximum d'hydrogène autorisé, et c'est pourquoi cette graisse est du type saturé.
Interactions intermoléculaires
La structure en général présente une forme trop évidente: celle d'un zigzag. Non seulement cela, c'est aussi un zigzag flexible, capable d'agencer ses atomes de carbone de manière à ce qu'ils correspondent parfaitement aux espaces vides de la queue d'une molécule voisine..
Une bonne analogie pour comprendre cela est de comparer les interactions entre deux molécules d'acide laurique avec celles de deux chaises pliantes empilées l'une sur l'autre pour former une colonne; Il en va de même avec ces molécules: leur nature saturée leur permet de se regrouper et de se précipiter en une graisse de plus grande insolubilité.
Les queues apolaires interagissent donc au moyen des forces de diffusion de Londres. Pendant ce temps, les têtes polaires forment des liaisons hydrogène entre elles, ce qui renforce encore les liaisons de leurs queues..
Ainsi, les molécules sont couplées de manière ordonnée jusqu'à ce qu'elles forment un cristal blanc à structure triclinique..
Ces cristaux d'acide laurique gras sont peu résistants à la chaleur, puisqu'ils fondent à 43 ° C. L'augmentation de la température désolidarise les queues sous l'effet des vibrations de leurs atomes; ils commencent à glisser les uns sur les autres, donnant ainsi naissance à de l'huile d'acide laurique.
Propriétés
Noms chimiques
Acide laurique, acide n-dodécanoïque, acide dodécylique, acide dodécanoïque, acide volvique et dodécylcarboxylate.
Formule moléculaire
C12H24OU ALORSdeux et CH3(CHdeux)dixCOOH.
Poids moléculaire
200,322 g / mol
Description physique
Blanc uni. Il peut également se présenter sous forme d'aiguilles incolores ou de poudre cristalline blanche..
Odeur
Caractéristique de l'huile pour bébé.
Point de fusion
43,2 ºC (111 ºF).
Point d'ébullition
297,9 ºC
Solubilité dans l'eau
Pratiquement insoluble dans l'eau:
-37 mg / L à 0 ºC
-48,1 mg / L à 50 ºC
-83 mg / L à 100 ºC.
Solubilité dans les solvants organiques
Un gramme d'acide laurique est dissous dans 1 mL d'alcool éthylique et 2,5 mL d'alcool propylique. Il est très soluble dans le benzène et l'éther, mais légèrement soluble dans le chloroforme.
Solubilité dans l'acétone
60,5 g / 100 g à 20 ºC
Solubilité dans le méthanol
120 g / 100 g à 20 ºC.
Densité
-1,007 g / cm3 à 24 ºC
-0,8744 g / cm3 à 41,5 ºC
-0,8679 g / cm3 à 50 ºC.
La pression de vapeur
-2,13 x 10-6 kPa (25 ºC)
-0,42 kPa (150 ºC).
Viscosité
-6,88 cPois (50 ºC)
-5,37 cPois (60 ºC).
Chaleur de combustion
7 413,7 kJ / mol.
Tension superficielle
26,6 mN / m à 70 ºC.
Indice de réfraction
1.4183 à 82 ºC.
Constante de dissociation
pKa = 5,3 à 20 ºC.
Applications
Industriel
L'acide laurique réagit avec l'hydroxyde de sodium pour le saponifier, produisant du laurate de sodium. Les savons à base d'acide laurique sont mousseux et ont la capacité de dissoudre les lipides.
Les acides gras fractionnés, y compris l'acide laurique, sont utilisés dans la fabrication d'esters, d'alcools gras, de peroxydes, de parfums, de finition de surface, de lubrifiants, de cosmétiques, d'aliments pour animaux, de chimie du papier, de plastiques, de détergents, de produits agrochimiques, de résines et de revêtements..
Détermination de la masse molaire
L'acide laurique est utilisé pour déterminer la masse molaire inconnue d'une substance. La raison: il a un point de fusion relativement élevé (43,8 ºC). L'acide laurique et l'autre substance sont fondus, déterminant la diminution du point cryoscopique du mélange et donc la masse molaire de la substance..
agriculture
L'acide laurique est utilisé en agriculture comme herbicide, insecticide, acaricide et régulateur de croissance des plantes. Les mousses, les algues, les lichens, les hépatiques et autres mauvaises herbes sont également utilisés dans les cultures fourragères, les fleurs ornementales et les plantes domestiques..
Avantages pour la santé
Greffes de pontage vasculaire
L'acide laurique se lie au peptide gli-arg-gli-asp-ser (GRGDS), facilitant son incorporation dans la matrice de poly (carbonate-urée) uréthane (PCU), utilisé dans les greffons pour pontage vasculaire.
Augmente l'action de certains médicaments
Il facilite la pénétration transdermique du médicament fenazépam, augmentant l'action anticonvulsivante du médicament trois fois. Il augmente également le passage à travers la peau humide de la caféine neutre et du salicylate de sodium anionique..
Action bactéricide
Dans une enquête, l'action bactéricide de l'acide laurique a été étudiée, à la fois in vivo et in vitro, sur les bactéries Staphylococcus aureus, Staphylococcus epidermis et Propionabacterium acnes, bactéries responsables de l'inflammation vasculaire..
Une dose d'acide laurique 15 fois plus faible était nécessaire, par rapport à la dose de peroxyde de benzoyle (BPO), un médicament habituellement utilisé dans le traitement de l'acné, pour montrer un effet thérapeutique..
Parmi les bactéries étudiées, P. acnes était la plus sensible à l'acide laurique. De plus, l'acide laurique n'a pas montré d'effet cytotoxique sur les sébocytes humains..
Traitement rectal du côlon
L'acide laurique est à l'étude en tant que traitement d'appoint prometteur dans le traitement du cancer rectal du côlon. Notant que l'acide laurique réduit l'utilisation du glutathion (GSH), et produit un stress oxydatif qui induit l'apoptose des cellules cancéreuses rectales du côlon.
Combattre les infections et les agents pathogènes
-L'acide laurique est utilisé pour traiter les infections virales, y compris la grippe et l'herpès génital, causées par le virus de l'herpès simplex (HSV). De plus, l'acide laurique est utilisé pour traiter les verrues génitales causées par le virus du papillome (VPH)..
-Sert de précurseur de la monolaurine, une substance antimicrobienne qui combat les agents pathogènes tels que les bactéries, les virus et les champignons.
-À lui seul ou en association avec des huiles essentielles, il peut lutter contre les agents pathogènes présents dans les aliments. De même, lorsqu'il est donné à des animaux d'élevage, il peut améliorer la qualité de la nourriture qu'ils produisent..
Autres
-Il pourrait être bénéfique dans le traitement de la peau sèche, car il pourrait aider à son hydratation. Cette propriété pourrait être utilisée pour améliorer des maladies telles que le psoriasis.
Il a une propriété antioxydante. Augmente les niveaux de lipoprotéines de haute densité (HDL), qui agit en éliminant le cholestérol déposé dans les vaisseaux sanguins, permettant sa sortie du corps.
-Abaisse la tension artérielle et la fréquence cardiaque. De plus, il réduit le stress oxydatif présent dans le cœur et les reins..
Effets secondaires
L'acide laurique est un acide gras saturé, on pense donc qu'il peut endommager le système cardiovasculaire; car les graisses saturées provoquent un dépôt de cholestérol dans les vaisseaux sanguins.
Cependant, selon une revue de 2016, l'action néfaste de l'acide laurique sur le fonctionnement du système cardiovasculaire n'est pas concluante. Une conclusion similaire a été tirée lors d'un examen effectué en 2003.
Comme l'acide laurique est un acide carboxylique, un ensemble d'effets secondaires non spécifiques peut lui être attribué. Par exemple, la réaction avec le diazo, le dithiocarbamate, l'isocyanate, le mercaptan, les nitrures et les sulfures peut produire des gaz toxiques..
Cependant, ce ne sont pas des effets secondaires spécifiques de l'acide laurique et il n'a pas été démontré qu'il était impliqué dans ces réactions. En général, aucun effet secondaire n'a été trouvé..
Cependant, certains effets nocifs pouvant survenir lors de la manipulation sont connus. Peut être nocif par inhalation, ingestion ou contact direct avec la peau. Sous forme de vapeur, il est irritant pour les yeux, les muqueuses, le nez et les voies respiratoires..
Les références
- Nakatsuji, T., Kao, M. C., Fang, J. Y., Zouboulis, C. C. (2009). Propriété antimicrobienne de l'acide laurique contre Propionibacterium Acnes: son potentiel thérapeutique pour l'acné vulgaire inflammatoire. Journal Investigative Dermatology 129 (10): 2480-2488.
- Fauser, J. K., Matthews, G. S., Cummins, A. et Howarth, G. (2013). Induction de l'apoptose par l'acide gras laurique à chaîne moyenne dans les cellules cancéreuses du côlon en raison de l'induction du stress oxydatif. Chimiothérapie 59 (3): 214-224.
- Superalimentaire. (06 octobre 2017). 25 Aliments et huiles à l'acide laurique: sources élevées à compléter. Récupéré de: superfoodly.com
- Régime de la Toscane. (2019). Acide laurique: structure, propriétés et sources. Récupéré de: tuscany-diet.net
- R. Lomer. (1963). La structure cristalline et moléculaire de l'acide laurique (forme A). Loi sur les cristaux. 16 984.
- Centre national d'information sur la biotechnologie. (2019). L'acide laurique. Base de données PubChem. Récupéré de: pubchem.ncbi.nlm.nih.gov
- WebMD LLC. (2019). L'acide laurique. Récupéré de: webmd.com
- Schaefer Anna. (22 février 2019). Qu'est-ce que l'acide laurique? Récupéré de: healthline.com
- Lama C. Siddhi. (12 avril 2019). Avantages de l'acide laurique pour le corps. Récupéré de: livestrong.com



Personne n'a encore commenté ce post.