
Caractéristiques, fonctions, types, valeurs des cellules NK
le Cellules NK (de l'anglais Natural Kcellules plus malades), cellules tueuses naturelles ou cellules cytocides naturelles, sont un type de lymphocyte effecteur qui participe aux réponses du système immunitaire inné ou non spécifique.
Ces cellules ont été découvertes il y a plus de 40 ans et certains auteurs les décrivent comme des «lymphocytes granulaires» qui, contrairement aux lymphocytes T et B, participent à la réponse immunitaire innée et ne subissent pas de processus de réarrangement génétique dans leurs lignées germinales..
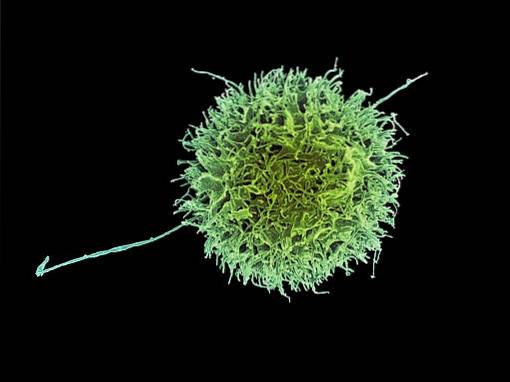
Comme elles n'expriment pas les marqueurs communs pour les deux autres classes de lymphocytes, les cellules NK étaient initialement appelées «cellules nulles». Cependant, d'autres études ont montré qu'il s'agissait de lymphocytes avec de gros granulocytes..
Ces cellules sont capables de contrôler différents types de tumeurs et d'infections microbiennes en limitant leur propagation et les lésions tissulaires. De plus, ils peuvent lyser différents types de cellules sans stimulation antigénique définie..
Les cellules NK sont des cellules extrêmement importantes dans la première ligne de défense contre les agents pathogènes, un fait qui a été démontré par des études dans lesquelles des êtres humains déficients en cellules NK peuvent souffrir d'infections mortelles pendant l'enfance..
Index des articles
- 1 Caractéristiques des cellules NK
- 1.1 Composants cytosoliques
- 2 fonctions
- 3 types
- 3.1 Chez les rongeurs
- 3.2 Chez l'homme
- 4 Valeurs normales
- 5 Activation et maturation
- 5.1 Processus d'activation
- 6 Mécanisme d'action
- 6.1 Distinction entre les cellules saines et infectées
- 7 signets
- 7.1 CD7, CD2 et CD5
- 7.2 CD11b
- 7,3 CD16
- 7,4 CD27
- 7,5 CD56
- 8 Références
Caractéristiques de cellules NK

Les cellules NK se trouvent dans une proportion plus faible que l'une ou l'autre des deux autres classes de lymphocytes (elles constituent 2 à 10% des lymphocytes circulants) et, comme elles appartiennent au système de défense inné, on pense qu'elles ont été parmi les premiers éléments cellulaires impliqués dans la protection des organismes multicellulaires.
Comme les lymphocytes T et les lymphocytes B, les cellules NK font partie du système hématopoïétique des mammifères et sont dérivées de cellules hématopoïétiques progénitrices qui expriment des marqueurs membranaires CD34 +, également appelées cellules HPC..
Alors que les cellules T sont connues pour mûrir dans le thymus et les cellules B pour mûrir dans la moelle osseuse, les tentatives pour déterminer la voie de développement complète des NK à partir de précurseurs de HPC n'ont pas été entièrement couronnées de succès; connu uniquement pour être indépendant du thymus.
Les cellules NK expriment des molécules d'adhésion sur leur surface membranaire appelées CD2, LFA-1, NCAM ou CD56. Ils expriment également des récepteurs de faible affinité à la portion constante (Fc) de l'immunoglobuline IgG qui sont collectivement appelés FcγRIIIA ou CD16..
Composants cytosoliques
L'intérieur d'une cellule cytocide naturelle est rempli de gros granules cytosoliques chargés de perforine, de granzymes et de protéoglycanes..
Les perforines sont des protéines porogènes qui «transpercent» la membrane plasmique des cellules attaquées par les NK. Les granzymes, en revanche, sont des sérine protéases qui pénètrent dans les cellules à travers les pores formés par les perforines et dégradent les protéines intracellulaires..
L'action combinée des perforines et des granzymes se traduit par l'arrêt de la production de protéines virales ou bactériennes et par l'apoptose ou la mort cellulaire programmée de la cellule infectée.
Caractéristiques
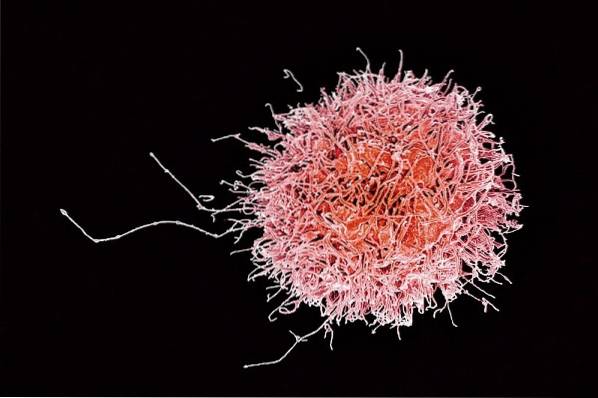
Les cellules tueuses naturelles fonctionnent dans l'élimination des cellules «cibles» ou «cibles» de manière naturelle, c'est-à-dire spontanément et sans grande spécificité, puisqu'elles ne nécessitent aucun type d'amorçage antigénique..
L'une des fonctions les plus importantes de ce groupe de cellules est sa capacité à tuer les cellules tumorales, en particulier celles appartenant à des lignées hématopoïétiques, ainsi que les cellules envahies par différents types de virus et / ou de bactéries..
Son activité est fortement stimulée par des facteurs tels que les interférons IFN-α et β, ainsi que par l'interleukine IL-12..
Grâce au fait que ces cellules produisent des cytokines importantes pour le système immunitaire, les NK participent à la régulation immunitaire, à la fois dans les systèmes innés et adaptatifs ou spécifiques..
Par exemple, la production d'interféron gamma (IFN-γ) dans les cellules NK peut perturber la participation des macrophages dans l'immunité innée, car cette molécule interfère avec les activités phagocytaires et microbicides.
Dans le même temps, l'IFN-γ produit par des cytocides naturels peut modifier l'engagement de populations entières de lymphocytes T auxiliaires, puisque l'IFN-γ inhibe également l'expansion et le développement d'une population par rapport à une autre..
Les cellules NK représentent la première ligne de défense lors d'infections virales, car elles contrôlent la réplication des virus tandis que les cellules T cytotoxiques sont activées, prolifèrent et se différencient, ce qui peut prendre plus de 6 jours..
Les types
Les populations de cellules NK sont assez hétérogènes, à la fois phénotypiquement, fonctionnellement et anatomiquement. De plus, ses caractéristiques dépendent du type d'organisme étudié..
Chez les rongeurs
Dans le modèle murin (souris), trois ensembles différents de cellules cytocides naturelles ont été décrits qui diffèrent les uns des autres par l'expression des marqueurs CD11b et CD27. En ce sens, il existe des cellules CD11bdullCD27 +, CD11b + CD27 + et CD11b + CD27dull.
L'exposant "terne" se réfère à "éteint" ou "inactif" et est utilisé, dans ce cas, pour décrire son état à la surface des cellules murines..
Les cellules CD11bdullCD27 + se différencient d'un double précurseur de type positif (CD11b + CD27 +) qui, à son tour, donne naissance au type plus mature de cellules NK chez les rongeurs: CD11b + CD27dull.
Les lignées doubles positives et les lignées mates CD11b + CD27 sont caractérisées en éliminant leurs cellules cibles et en sécrétant une cytokine connue sous le nom d'interféron (INF-γ). Cependant, ces derniers sont dans quelque chose appelé «sénescence réplicative».
Les trois types de cellules NK sont répartis dans différents tissus. Les cellules CD11bdullCD27 + se trouvent principalement dans les ganglions lymphatiques et la moelle osseuse. Les cellules ternes CD11b + CD27 sont abondantes dans le sang, la rate, les poumons et le foie; pendant ce temps, les cellules doubles positives ont une distribution plus homogène ou systémique.
Chez les humains
Les cellules NK chez l'homme sont également classées en fonction des marqueurs de surface qu'elles expriment, mais dans ce cas elles se différencient par la présence des marqueurs CD56dim et CD56bright. Les exposants «faible» et «clair» se réfèrent respectivement à «sombre» et «clair»..
Les différences entre ces cellules résident dans les propriétés de «recherche de cible» de chacune, qui sont données par la présence de l'un ou l'autre marqueur..
Dans le sang périphérique et la rate des humains, le principal type de cellule NK est connu sous le nom de CD56dimCD16 +, qui exprime généralement la protéine porphyrine et est cytotoxique. Ils produisent également de l'IFN-γ à la suite de l'interaction avec les cellules tumorales dans des conditions in vitro.
Les cellules CD56brightCD16- se trouvent dans les ganglions lymphatiques et les amygdales, qui, au lieu de produire de la porphyrine, sécrètent la cytokine IFN-γ en réponse à la stimulation par les interleukines IL-12, IL-15 et IL-18.
Chez les humains et les rongeurs, on pense que les amygdales et autres organes lymphoïdes secondaires sont les sites de production et de maturation de la plupart des cellules NK..
Certaines études suggèrent qu'il existe une certaine similitude entre les cellules CD56bright humaines et les cellules CD11dull de rongeur en termes de localisation anatomique, de caractéristiques phénotypiques, de teneur en perforine cytosolique, de potentiel prolifératif et d'expression de surface de l'interleukine IL-7R..
Valeurs normales
Ceux-ci ont une demi-vie assez courte (environ 2 semaines) et on pense que chez un être humain adulte, il y a environ 2 billions de cellules en circulation. Ils sont abondants dans le sang, la rate et d'autres tissus lymphoïdes et non lymphoïdes.
Des études montrent que la concentration normale chez les hommes et les femmes adultes est d'environ 200 et 600 cellules par microlitre de sang testé..
Activation et maturation
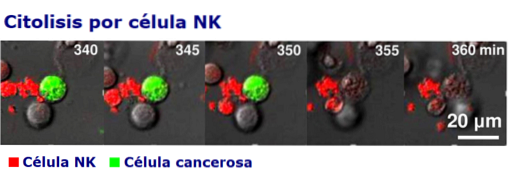
L'intensité et la qualité des réponses cytotoxiques des cellules NK dépendent du microenvironnement généré par les cytokines et de l'interaction avec d'autres cellules du système immunitaire, en particulier avec les cellules T, les cellules dendritiques et les macrophages..
Parmi les cytokines activatrices des cellules NK, on trouve les interleukines, spécifiquement IL-12, IL-18 et IL-15; ainsi que l'interféron de type I (IFN-I). L'interféron et les interleukines sont de puissants activateurs de la fonction effectrice de NK.
L'interleukine IL-2 est également impliquée dans la promotion de la prolifération, de la cytotoxicité et de la sécrétion de cytokines par les cellules NK..
L'IL-15 est cruciale pour la différenciation des NK, tandis que l'IL-2 et l'IL-18 sont essentielles pour la maturation ultérieure de ces cellules..
Processus d'activation
Les cellules cytocides naturelles sont activées grâce à la reconnaissance de leurs propres molécules (un processus connu en anglais sous le nom de «reconnaissance des molécules de soi”) Qui sont exprimées de manière constitutive dans des conditions d’état stationnaire.
Dans leurs membranes, ces cellules expriment différents membres d'une famille de protéines de surface qui contiennent deux ou trois domaines de type immunoglobuline dans leurs parties extracellulaires et des motifs similaires aux domaines d'activation des immunorécepteurs via la tyrosine dans leur région intracellulaire..
Chaque cellule NK peut exprimer une ou plusieurs de ces protéines réceptrices et chaque récepteur est capable de reconnaître une forme spécifique d'une molécule du complexe majeur d'histocompatibilité de classe I (CMH-I)..
La reconnaissance entre cette molécule et le récepteur à la surface des cellules cytocides naturelles conduit à la formation d'un complexe avec d'abondants peptides dérivés de protéines «auto»..
Les récepteurs sont principalement des protéines inhibitrices qui activent une tyrosine phosphatase qui empêche la cellule d'émettre des réponses normales.
Mécanisme d'action
L'élimination ou la mort médiée par les cellules tueuses naturelles est similaire à celle qui se produit pendant l'action cytolytique des lymphocytes T CD8 (cytotoxiques), bien que la différence soit que les NK sont cytotoxiques constitutives, c'est-à-dire qu'elles n'ont pas besoin d'être activées avant.
Les NK actifs expriment le ligand FasL, c'est pourquoi ils induisent relativement facilement la mort des cellules cibles qui expriment la protéine Fas à leur surface..
Après la formation du FasL / Fas complet, un processus connu sous le nom de "dégranulation" se produit, qui se termine par la libération de porphyrine et de granzymes au niveau des sites de contact intercellulaire..

Malgré les similitudes susmentionnées, les NK diffèrent des mécanismes à médiation par les lymphocytes T cytotoxiques en ce que la reconnaissance de leurs cellules cibles ne dépend pas des protéines du complexe majeur d'histocompatibilité..
Une autre différence est que les cellules NK n'ont pas de système de «mémoire immunitaire», ce qui est démontré par le fait que leur activité n'augmente pas après une seconde exposition à leurs cellules cibles..
Distinction entre les cellules saines et infectées
Les cytocides naturels font la distinction entre une cellule saine et une autre infectée ou tumorale (cancéreuse) grâce à un équilibre de signaux d'activation et d'inhibition, qui sont reconnus par des récepteurs de surface spécifiques.
Ces récepteurs sont de deux types: de type lectine (protéines qui se lient aux glucides et autres protéines) et de type immunoglobuline (similaire à la région constante des immunoglobulines).
Dans ce dernier groupe, les récepteurs des immunoglobulines des cellules tueuses ou KIR sont reconnus. récepteurs de type immunoglobuline à cellules tueuses), capable de reconnaître et de se lier à des formes spécifiques des protéines du complexe majeur d'histocompatibilité de classe I (HLA-B ou HLA-C).
Il est important de noter que les NK "n'attaquent" pas les cellules qui expriment des niveaux normaux de molécules du CMH de classe I, mais ils tuent les cellules qui expriment des molécules étrangères de ce type ou celles qui n'ont pas lesdits marqueurs (ce qui est typique des cellules tumorales et infectées par des virus).
Marqueurs
Les NK expriment certains marqueurs membranaires communs pour les monocytes et les granulocytes, et d'autres typiques pour les lymphocytes T..
D'autre part, les cytocides naturels expriment différents groupes de marqueurs de surface, mais on ne sait pas encore avec certitude si l'hétérogénéité indique des sous-populations cellulaires ou des stades lors de leur activation ou de leur maturation..
Quelques exemples de marqueurs de cellules NK sont:
CD7, CD2 et CD5
Les cellules NK sont dérivées du même parent qui donne naissance aux cellules T. Cette cellule mère exprime généralement les marqueurs CD7, CD2 et parfois CD5..
CD2 est une protéine de poids moléculaire de 50 kDa qui est également présente dans les cellules T. Elle est connue comme une molécule d'adhésion de surface et participe à l'activation des cellules T..
Le CD5 est normalement présent sur les lymphocytes T et certaines sous-populations de lymphocytes B. C'est un marqueur de 67 kDa et a également des fonctions adhésives..
Le marqueur CD7 est typique des cellules souches hématopoïétiques et a également été trouvé dans certaines sous-populations de cellules T. Il a un poids moléculaire de 40 kDa et fonctionne dans la transduction du signal..
CD11b
Ce récepteur est partagé entre les NK, les monocytes et les granulocytes. Il a un poids moléculaire de 165 kDa et est capable de s'associer avec d'autres marqueurs de surface. Ses principales fonctions sont adhésives, notamment lors des processus de phagocytose ou "opsonisation"..
CD16
C'est un récepteur de 50 à 70 kDa qui est lié à une molécule transmembranaire de phosphatidyl inositol. Participe à l'activation des cellules tueuses naturelles et se retrouve également dans les granulocytes et les macrophages.
Il fonctionne également comme un récepteur pour la région constante de la chaîne gamma de certains anticorps..
CD27
Il se trouve sur la plupart des lymphocytes T et est un homodimère de chaîne peptidique de 55 kDa. Il semble être un membre de la famille des récepteurs du facteur de nécrose tumorale (TNF-R) et est également impliqué dans la co-stimulation des cellules T..
CD56
Ce récepteur est unique aux cellules NK et est composé de chaînes de 135 et 220 kDa. Participe à l'adhésion «homotypique» de ces cellules.
Les références
- Abbas, A., Lichtman, A. et Pober, J. (1999). Immunologie cellulaire et moléculaire (3e éd.). Madrid: McGraw-Hill.
- Burmester, G., et Pezzutto, A. (2003). Atlas des couleurs d'immunologie Avec les contributions de. New York, États-Unis: Thieme.
- Caligiuri, M. A. (2008). Cellules tueuses naturelles humaines. Du sang, 112, 461-469.
- Kindt, T., Goldsby, R. et Osborne, B. (2007). Immunologie de Kuby (6e éd.). Mexique D.F.: McGraw-Hill Interamericana de España.
- Mandal, A. et Viswanathan, C. (2015). Cellules tueuses naturelles: dans la santé et la maladie. Hématol Oncol Stem Cell Ther, 1-9.
- Vivier, E., Tomasello, E., Baratin, M., Walzer, T., et Ugolini, S. (2008). Fonctions des cellules tueuses naturelles. Immunologie de la nature, 9(5), 503-510.
- Vivier, E., Zitvogel, L., Lanier, L. L., Yokoyama, W. M. et Ugolini, S. (2011). Immunité innée ou adaptative? L'exemple des cellules tueuses naturelles. La science, 331, 44-49.


Personne n'a encore commenté ce post.