
Morphologie du diphyllobothrium latum, cycle de vie, symptômes
le Diphyllobothrium latum c'est un parasite plat de la classe des cestodes qui peut provoquer des infections chez l'homme. La maladie qu'elle produit reçoit plusieurs noms: botryocephalus, diphyllobothriasis ou botryocephalus, mais tous renvoient à la même maladie parasitaire intestinale.
L'infection par ce ver plat se produit lors de la consommation de poisson cru ou mal cuit. Cette caractéristique limitait la pathologie aux régions avec des habitudes culinaires comprenant du poisson cru, telles que l'Asie, l'Arctique et l'Amérique, mais la mondialisation des sushis et des ceviches en tant que plats courants a propagé le parasite dans le monde entier..
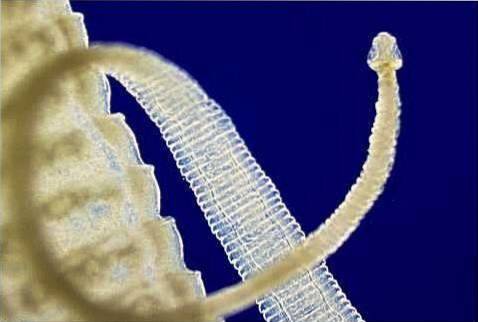
Ces parasites ont une morphologie et un cycle de vie vraiment intéressants. La forme d'infection chez l'homme - leur hôte principal - et chez d'autres mammifères et oiseaux se produit par voie orale, bien que l'atteinte de ce point soit un processus long et complexe avec de nombreux bords et variables.
Les symptômes qu'il produit sont très non spécifiques, principalement liés au tractus gastro-intestinal. Atteindre le diagnostic n'est pas si simple car cette possibilité n'est généralement pas envisagée et elle est souvent réalisée grâce à des découvertes fortuites. Le traitement peut être délicat, mais presque toujours efficace.
Index des articles
- 1 Morphologie
- 2 Cycle de vie
- 2.1 Œuf et foyer
- 2.2 Premier hôte
- 2.3 Deuxième invité
- 2.4 Hôte définitif
- 3 Symptômes qu'il produit
- 4 Traitement
- 4.1 Antiparasitaires
- 4.2 Autres traitements
- 5 Références
Morphologie
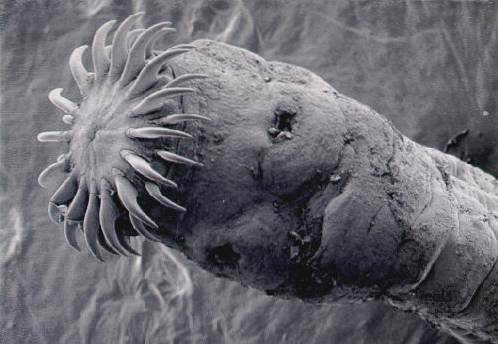
D'un point de vue taxinomique, comme tout membre du phylum flatworm et de la classe cestoda, le Diphyllobothrium latum c'est un ver plat et effilé. Il a un scolex (tête) plus allongé que la plupart des autres membres de sa classe et a des disques d'aspiration au lieu des ventouses habituelles..
Ces parasites ont une zone de prolifération ou un cou juste après le scolex et le reste du corps est constitué de nombreux segments ou proglottis, chacun avec son propre ensemble génital des deux sexes; c'est-à-dire qu'ils sont hermaphrodites. Certains auteurs ont décrit des spécimens avec jusqu'à 4000 segments dans leur extension.
le Diphyllobothrium latum c'est l'un des parasites les plus longs pouvant affecter l'homme: ils peuvent se développer dans l'intestin de 2 à 15 mètres.
Sa longueur maximale atteinte a été de 25 mètres. Le taux de croissance peut atteindre 22 cm par jour (soit près de 1 cm par heure) et ils survivent jusqu'à 25 ans à l'intérieur du corps.
Cycle biologique
Le développement de ces parasites implique jusqu'à deux hôtes intermédiaires et plusieurs stades d'évolution avant d'atteindre l'hôte définitif: l'homme..
Oeuf et coeur
Les œufs qui voyagent dans les excréments humains ne sont pas embryonnés et ont un opercule dans leur partie la plus étroite. Lorsque les matières fécales atteignent l'eau, elles deviennent des larves de premier stade (oncosphère), qui sont recouvertes d'une enveloppe externe ciliée, formant ainsi un coracidium qui s'ouvre au contact de l'eau, devenant embryonnaire.
Premier invité
Le cœur mobile nage dans l'eau, attirant de potentiels premiers hôtes intermédiaires. Ces hôtes initiaux sont des crustacés de la sous-classe des copépodes, qui font partie du plancton dans la plupart des plans d'eau de la planète (océans, mers, rivières, lacs, entre autres).
Les coracidies pénètrent dans les parois intestinales des copépodes et se transforment en procercoïdes, dépourvus de scolex et de organes génitaux, mais ayant un appendice postérieur contenant des crochets embryonnaires.
Deuxième invité
Les copépodes infectés par les procerchoïdes sont ingérés par les poissons d'eau douce ou d'eau salée; le saumon a une vraie prédilection pour ces crustacés.
Une fois à l'intérieur, les procercoïdes se déplacent vers les tissus musculaires, les organes et la cavité abdominale du poisson et là, ils deviennent des plérocercoïdes..
Ces plérocercoïdes peuvent être trouvés sans capsules à l'intérieur du poisson, bien qu'entourés d'un tissu conjonctif kystique. Certains sont automatiquement encapsulés en étant situés dans les muscles du poisson, c'est la partie la plus ingérée par les hôtes finaux du parasite..
Hôte définitif
Les humains, ainsi que certains mammifères ou poissons-oiseaux, sont les hôtes définitifs. La chair de poisson contaminée est consommée par l'hôte et les plérocercoïdes se transforment rapidement en vers adultes dans l'intestin. Là, ils pondent leurs premiers œufs 2 à 6 semaines après l'infection et entament un nouveau cycle biologique..
le Diphyllobothrium latum, comme la plupart des membres de son espèce, il a une faible spécificité d'hôte. Cela signifie que les humains peuvent être infectés par des espèces qui affectent normalement d'autres mammifères ou oiseaux et vice versa..
Symptômes qu'il produit
Malgré la grande taille de ces parasites et les grandes surfaces qu'ils occupent dans le tractus gastro-intestinal de l'hôte, de nombreuses infections sont asymptomatiques. Environ 20% des patients présentent des symptômes non spécifiques tels que des douleurs ou malaises abdominaux, de la diarrhée et de la constipation..
D'autres symptômes peuvent être de la fatigue, des maux de tête, des réactions allergiques et un mal de langue en mangeant. Des infestations massives peuvent provoquer une occlusion intestinale, une cholangite et une cholécystite, en particulier en raison de petits segments du parasite qui se répandent et migrent dans le canal cholédoque et la vésicule biliaire..
Infection prolongée ou sévère par Diphyllobothrium latum il peut provoquer une anémie mégaloblastique due à une dissociation parasitaire du facteur intrinsèque vitamine B12 dans la lumière intestinale, rendant la vitamine indisponible pour l'hôte. Environ 80% de l'apport en vitamine B12 est absorbé par le ver.
Traitement
Antiparasitaires
Les vers adultes de Diphyllobothrium latum sont facilement traitables avec le praziquantel, un anthelminthique qui affecte le calcium dans le parasite, le paralyse et l'empêche de se fixer aux parois de l'intestin.
Ce médicament modifie également l'absorption de l'adénosine, de sorte que le ver ne peut pas synthétiser les purines, étant incapable de se développer et de se reproduire.
Une dose unique de 25 mg / kg de poids corporel s'est avérée très efficace contre Diphyllobothrium latum. Un autre anthelminthique, le niclosamide, est également efficace contre ce parasite dans sa dose unique habituelle de 2 grammes par voie orale, qui peut être administrée aux patients âgés de plus de 6 ans..
Les effets indésirables de ces deux médicaments ne sont pas très graves et peuvent être traités sans complications majeures. Les plus importants sont: malaise général, étourdissements, douleurs abdominales avec ou sans nausées, fièvre et urticaire. Cependant, tous ces symptômes sont causés par l'infection elle-même, il est donc difficile de les distinguer..
Autres traitements
L'administration de vitamine B12 est nécessaire chez les patients atteints d'anémie mégaloblastique. D'autres mesures de soutien telles que le soutien nutritionnel et les recommandations diététiques sont les bienvenues; le traitement symptomatique est permanent avec des antipyrétiques, des anti-inflammatoires et des protecteurs gastriques.
Des mesures préventives sont également essentielles. Les stations d'épuration et l'utilisation de toilettes et d'installations sanitaires adéquates représentent les mesures sanitaires les plus efficaces pour éviter la contamination de l'eau..
La meilleure thérapie prophylactique est d'éviter de manger du poisson cru, fumé ou mariné. Une autre alternative est de congeler le poisson.
Certains auteurs suggèrent de garder le poisson pendant 24 à 48 heures à -18 ° C, et d'autres plus stricts recommandent -20 ° C pendant 7 jours ou -35 ° C pendant 15 heures pour tuer les parasites..
Les références
- Scholz, Tomás et collaborateurs (2009). Mise à jour sur le ténia humain large (genre Diphyllobothrium), y compris la pertinence clinique. Examens en microbiologie clinique, 22 (1): 146-160.
- Guttowa A. et Moskwa, B. (2005). L'histoire de l'exploration du cycle de vie du Diphyllobothrium latum. Wiadomosci parazytologiczne, 51 (4): 359-364.
- Von Bonsdorff, B. et Bylund, G. (1982). L'écologie du Diphyllobothrium latum. Écologie de la maladie, 1 (1): 21-26.
- Rosas, Reinaldo et Weitzel, Thomas (2014). Diphyllobothrium latum. Journal chilien d'infectologie, 31 (2).
- Escobedo, Angel (2015). Diphyllobothrium. Microbiologie médicale et parasitologie, première édition, chapitre 117, 361-364.
- Wikipédia (2018). Diphyllobothrium latum. Récupéré de: es.wikipedia.org



Personne n'a encore commenté ce post.