
Liaison phosphodiester comment elle est formée, fonction et exemples
Les liaisons phosphodiester sont les liaisons covalentes qui se produisent entre deux des atomes d'oxygène d'un groupe phosphate et les groupes hydroxyle de deux autres molécules différentes. Dans ce type de liaison, le groupe phosphate agit comme un «pont» de liaison stable entre les deux molécules à travers leurs atomes d'oxygène..
Le rôle fondamental des liaisons phosphodiester dans la nature est la formation de chaînes d'acide nucléique, à la fois ADN et ARN. Avec les sucres pentoses (désoxyribose ou ribose, selon le cas), les groupes phosphate font partie de la structure de support de ces biomolécules importantes..
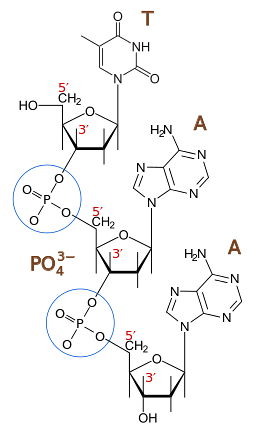
Les chaînes nucléotidiques d'ADN ou d'ARN, comme les protéines, peuvent prendre différentes conformations tridimensionnelles qui sont stabilisées par des liaisons non covalentes, telles que des liaisons hydrogène entre des bases complémentaires..
Cependant, la structure primaire est donnée par la séquence linéaire de nucléotides liés de manière covalente via des liaisons phosphodiester..
Index des articles
- 1 Comment se forme une liaison phosphodiester?
- 1.1 Enzymes impliquées
- 2 Fonction et exemples
- 3 Références
Comment se forme une liaison phosphodiester?
Comme les liaisons peptidiques dans les protéines et les liaisons glycosidiques entre les monosaccharides, les liaisons phosphodiester résultent de réactions de déshydratation dans lesquelles une molécule d'eau est perdue. Voici le schéma général de l'une de ces réactions de déshydratation:
H-X1-OH + H-Xdeux-OH → H-X1-Xdeux-OH + HdeuxOU ALORS
Les ions phosphate correspondent à la base conjuguée complètement déprotonée de l'acide phosphorique et sont appelés phosphates inorganiques, en abrégé Pi. Lorsque deux groupes phosphate sont liés ensemble, une liaison phosphate anhydre est formée et une molécule connue sous le nom de pyrophosphate inorganique ou PPi est obtenue..
Lorsqu'un ion phosphate est attaché à un atome de carbone dans une molécule organique, la liaison chimique est appelée un ester phosphate et l'espèce résultante est un monophosphate organique. Si la molécule organique se lie à plus d'un groupe phosphate, des diphosphates ou triphosphates organiques se forment.
Lorsqu'une seule molécule de phosphate inorganique est attachée à deux groupes organiques, une liaison phosphodiester ou "phosphate diester" est utilisée. Il est important de ne pas confondre les liaisons phosphodiester avec les liaisons phosphoanhydro à haute énergie entre les groupes phosphate de molécules comme l'ATP, par exemple..
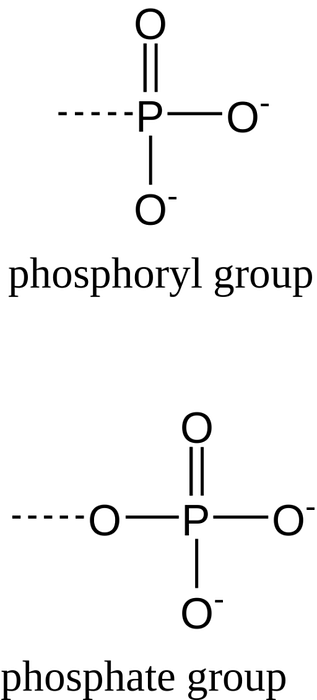
Les liaisons phosphodiester entre nucléotides adjacents consistent en deux liaisons phosphoester qui se produisent entre l'hydroxyle à la position 5 'd'un nucléotide et l'hydroxyle à la position 3' du nucléotide suivant dans un brin d'ADN ou d'ARN.
Selon les conditions de l'environnement, ces liaisons peuvent être hydrolysées à la fois enzymatiquement et non enzymatiquement..
Enzymes impliquées
La formation et la rupture des liaisons chimiques sont cruciales pour tous les processus vitaux tels que nous les connaissons, et le cas des liaisons phosphodiester ne fait pas exception..
Parmi les enzymes les plus importantes qui peuvent former ces liaisons, on trouve les ADN ou ARN polymérases et les ribozymes. Les enzymes phosphodiestérases sont capables de les hydrolyser par voie enzymatique.
Au cours de la réplication, un processus crucial pour la prolifération cellulaire, dans chaque cycle de réaction un dNTP (désoxynucléotide triphosphate) complémentaire de la base de matrice est incorporé dans l'ADN par une réaction de transfert de nucléotides..
La polymérase est responsable de la formation d'une nouvelle liaison entre le 3'-OH du brin matrice et l'α-phosphate du dNTP, grâce à l'énergie libérée par la rupture des liaisons entre les phosphates α et β du dNTP, qui sont liés par des liaisons phosphoanhydro.
Le résultat est l'extension de la chaîne par un nucléotide et la libération d'une molécule de pyrophosphate (PPi) s. Il a été déterminé que ces réactions méritent deux ions magnésium divalents (Mgdeux+), dont la présence permet la stabilisation électrostatique du nucléophile OH- pour obtenir l'approximation du site actif de l'enzyme.
le paquetà d'une liaison phosphodiester est proche de 0, donc dans une solution aqueuse ces liaisons sont complètement ionisées, chargées négativement.
Cela donne aux molécules d'acide nucléique une charge négative, qui est neutralisée grâce à des interactions ioniques avec les charges positives des résidus d'acides aminés protéiques, une liaison électrostatique avec des ions métalliques ou une association avec des polyamines..
Dans une solution aqueuse, les liaisons phosphodiester dans les molécules d'ADN sont beaucoup plus stables que dans les molécules d'ARN. En solution alcaline, ces liaisons dans les molécules d'ARN sont clivées par déplacement intramoléculaire du nucléoside à l'extrémité 5 'par un oxyanion 2'.
Fonction et exemples
Comme mentionné, le rôle le plus important de ces liaisons est leur participation à la formation du squelette des molécules d'acide nucléique, qui sont l'une des molécules les plus importantes du monde cellulaire..
L'activité des enzymes topoisomérases, qui participent activement à la réplication de l'ADN et à la synthèse des protéines, dépend de l'interaction des liaisons phosphodiester à l'extrémité 5 'de l'ADN avec la chaîne latérale des résidus tyrosine dans le site actif de ces enzymes.
Les molécules qui participent en tant que seconds messagers, comme l'adénosine monophosphate cyclique (AMPc) ou la guanosine triphosphate cyclique (cGTP), possèdent des liaisons phosphodiester qui sont hydrolysées par des enzymes spécifiques appelées phosphodiestérases, dont la participation est de la plus haute importance pour de nombreux processus de signalisation mobiles.
Les glycérophospholipides, composants fondamentaux des membranes biologiques, sont constitués d'une molécule de glycérol qui se lie par des liaisons phosphodiester aux groupes polaires «tête» qui constituent la région hydrophile de la molécule..
Les références
- Fothergill, M., Goodman, M. F., Petruska, J., et Warshel, A. (1995). Analyse structure-énergie du rôle des ions métalliques dans l'hydrolyse des liaisons phosphodiester par l'ADN polymérase I. Journal de l'American Chemical Society, 117(47), 11619-11627.
- Lodish, H., Berk, A., Kaiser, C. A., Krieger, M., Bretscher, A., Ploegh, H., Martin, K. (2003). Biologie cellulaire moléculaire (5e éd.). Freeman, W. H. & Company.
- Nakamura, T., Zhao, Y., Yamagata, Y., Hua, Y. J., et Yang, W. (2012). Regarder l'ADN polymérase η créer une liaison phosphodiester. Nature, 487(7406), 196-201.
- Nelson, D. L. et Cox, M. M. (2009). Principes de biochimie de Lehninger. Éditions Omega (5e éd.)
- Oivanen, M., Kuusela, S., et Lönnberg, H. (1998). Cinétique et mécanismes de clivage et d'isomérisation des liaisons phosphodiester de l'ARN par les acides et bases bronstés. Avis sur les produits chimiques, 98(3), 961-990.
- Pradeepkumar, P. I., Höbartner, C., Baum, D. et Silverman, S. (2008). Formation catalysée par l'ADN de liaisons nucléopeptidiques. Édition internationale d'Angewandte Chemie, 47(9), 1753-1757.
- Soderberg, T. (2010). Chimie organique avec un accent biologique Volume II (Vol. II). Minnesota: Université du Minnesota Morris Digital Well. Récupéré de www.digitalcommons.morris.umn.edu


Personne n'a encore commenté ce post.