
Structure, biosynthèse et fonctions de la phosphatidyléthanolamine
La phosphatidyléthanolamine (PE) est un glycérophospholipide abondant dans les membranes plasmiques des organismes procaryotes. Au contraire, dans les membranes cellulaires eucaryotes, c'est le deuxième glycérophospholipide le plus abondant à l'intérieur de la membrane plasmique après la phosphatidylcholine..
Malgré l'abondance de la phosphatidyléthanolamine, son abondance dépend non seulement du type cellulaire mais aussi du compartiment et du moment du cycle de vie cellulaire spécifique considéré..
Les membranes biologiques sont des barrières qui définissent les organismes cellulaires. Non seulement ils ont des fonctions de protection et d'isolement, mais ils sont également essentiels à l'établissement de protéines qui nécessitent un environnement hydrophobe pour leur fonctionnement optimal..
Les eucaryotes et les procaryotes ont des membranes composées principalement de glycérophospholipides et, dans une moindre mesure, de sphingolipides et de stérols..
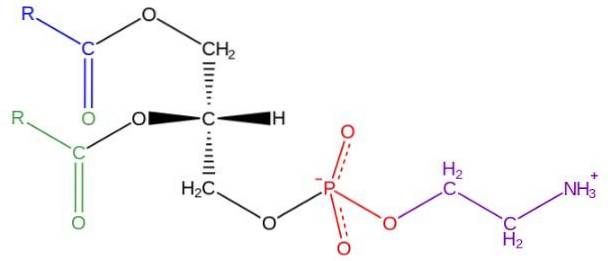
Les glycérophospholipides sont des molécules amphipathiques structurées sur un squelette L-glycérol qui est estérifié aux positions sn-1 et sn-2 par deux acides gras de longueur et de degré de saturation variables. Dans l'hydroxyle de la position sn-3, il est estérifié par un groupe phosphate, auquel à son tour différents types de molécules peuvent être attachés qui donnent naissance aux différentes classes de glycérophospholipides.
Dans le monde cellulaire, il existe une grande variété de glycérophospholipides, cependant, les plus abondants sont la phosphatidylcholine (PC), la phosphatidyléthanolamine (PE), la phosphatidylsérine (PS), le phosphatidylinositol (PI), l'acide phosphatidique (PA), la phosphatidylglycérol (PG) et la cardiolipine. (CL).
Index des articles
- 1 Structure
- 2 Biosynthèse
- 2.1 Route Kennedy
- 2.2 Chemin PSD
- 3 fonctions
- 4 Références
Structure
La structure de la phosphatidyléthanolamine a été découverte par Baer et al.En 1952. Comme cela a été déterminé expérimentalement pour tous les glycérophospholipides, la phosphatidyléthanolamine est formée par une molécule de glycérol estérifiée aux positions sn-1 et sn-2 avec des chaînes acides grasses entre 16 et 20 atomes de carbone.
Les acides gras estérifiés dans l'hydroxyle sn-1 sont généralement saturés (sans doubles liaisons) avec des longueurs maximales de 18 atomes de carbone, tandis que les chaînes liées en position sn-2 sont plus longues et avec une ou plusieurs insaturations (doubles liaisons).
Le degré de saturation de ces chaînes contribue à l'élasticité de la membrane, ce qui a une grande influence sur l'insertion et la séquestration des protéines dans la bicouche..
La phosphatidyléthanolamine est considérée comme un glycérophospholipide non lamellaire, car elle a une forme géométrique conique. Cette forme est donnée par la petite taille de son groupement polaire ou «tête», par rapport à celle des chaînes d'acides gras qui composent les «queues» hydrophobes.
Le groupe «tête» ou groupe polaire de la phosphatidyléthanolamine a un caractère zwitterionique, c'est-à-dire qu'il a des groupes qui peuvent être chargés positivement et négativement dans certaines conditions de pH..
Cette caractéristique lui permet de se lier à l'hydrogène avec un grand nombre de résidus d'acides aminés et sa distribution de charge est un déterminant essentiel pour la topologie de domaine de nombreuses protéines membranaires intégrales..
Biosynthèse
Dans les cellules eucaryotes, la synthèse des lipides structuraux est géographiquement limitée, le principal site de biosynthèse étant le réticulum endoplasmique (RE) et dans une moindre mesure l'appareil de Golgi..
Il existe quatre voies biosynthétiques indépendantes pour la production de phosphatidyléthanolamine: (1) la voie CDP-éthanolamine, également connue sous le nom de voie Kennedy; (2) la voie PSD pour la décarboxylation de la phosphatidylsérine (PS); (3) acylation du lyso-PE et (4) réactions de changement de base du groupe polaire d'autres glycérophospholipides.
Route Kennedy
La biosynthèse de la phosphatidyléthanolamine par cette voie est limitée à l'ER et il a été démontré que dans les cellules hépatiques de hamster, c'est la principale voie de production. Il se compose de trois étapes enzymatiques consécutives catalysées par trois enzymes différentes.
Dans un premier temps, la phosphoéthanolamine et l'ADP sont produits grâce à l'action de l'éthanolamine kinase, qui catalyse la phosphorylation ATP-dépendante de l'éthanolamine..
Contrairement aux plantes, ni les mammifères ni les levures ne sont capables de produire ce substrat, il doit donc être consommé dans l'alimentation ou obtenu à partir de la dégradation de molécules préexistantes de phosphatidyléthanolamine ou de sphingosine..
La phosphoéthanolamine est utilisée par le CTP: phosphoéthanolamine cytidyltransférase (ET) pour former le composé à haute énergie CDP: éthanolamine et un phosphate inorganique.
La 1,2-diacylglycérol éthanolamine phosphotransférase (ETP) utilise l'énergie contenue dans la liaison CDP-éthanolamine pour lier de manière covalente l'éthanolamine à une molécule de diacylglycérol insérée dans la membrane, donnant naissance à la phosphatidyléthanolamine..
Route PSD
Cette voie fonctionne à la fois chez les procaryotes et chez les levures et les mammifères. Chez les bactéries, il se produit dans la membrane plasmique, mais chez les eucaryotes, il se produit dans une zone du réticulum endoplasmique qui est étroitement liée à la membrane mitochondriale.
Chez les mammifères, la voie est catalysée par une seule enzyme, la phosphatidylsérine décarboxylase (PSD1p), qui est intégrée dans la membrane mitochondriale, dont le gène est codé par le noyau. La réaction implique la décarboxylation du PS en phosphatidyléthanolamine.
Les deux voies restantes (acylation PE-lyso et échange de calcium dépendant du groupe polaire) se produisent dans le réticulum endoplasmique, mais ne contribuent pas de manière significative à la production totale de phosphatidyléthanolamine dans les cellules eucaryotes..
Caractéristiques
Les glycérophospholipides ont trois fonctions principales dans la cellule, parmi lesquelles se distinguent les fonctions structurelles, le stockage d'énergie et la signalisation cellulaire..
La phosphatidyléthanolamine est associée à l'ancrage, à la stabilisation et au repliement de plusieurs protéines membranaires, ainsi qu'aux changements conformationnels nécessaires au fonctionnement de nombreuses enzymes.
Il existe des preuves expérimentales qui proposent la phosphatidyléthanolamine comme glycérophospholipide crucial au stade avancé de la télophase, lors de la formation de l'anneau contractile et de l'établissement du fragmoplaste qui permet la division de la membrane des deux cellules filles..
Il joue également un rôle important dans tous les processus de fusion et de fission (union et séparation) des membranes à la fois du réticulum endoplasmique et de l'appareil de Golgi..
Chez E. coli, il a été montré que la phosphatidyléthanolamine est nécessaire au repliement et au fonctionnement correct de l'enzyme lactose permease, c'est pourquoi il a été suggéré qu'elle joue un rôle de «chaperon» moléculaire.
La phosphatidyléthanolamine est le principal donneur de la molécule d'éthanolamine nécessaire à la modification post-traductionnelle de nombreuses protéines, telles que les ancres GPI.
Ce glycérophospholipide est le précurseur de nombreuses molécules à activité enzymatique. De plus, les molécules dérivées de son métabolisme, ainsi que le diacylglycérol, l'acide phosphatidique et certains acides gras, peuvent jouer le rôle de seconds messagers. De plus, c'est un substrat important pour la production de phosphatidylcholine..
Les références
- Brouwers, J. F. H. M., Vernooij, E. A. A. M., Tielens, A. G. M., et van Golde, L. M. G. (1999). Séparation et identification rapides des espèces moléculaires de la phosphatidyléthanolamine. Journal of Lipid Research, 40 (1), 164-169. Récupéré de jlr.org
- Calzada, E., McCaffery, J. M. et Claypool, S. M. (2018). La phosphatidyléthanolamine produite dans la membrane mitochondriale interne est essentielle à la fonction du complexe 3 du cytochrome bc1 de levure. BioRxiv, 1, 46.
- Calzada, E., Onguka, O., et Claypool, S. M. (2016). Métabolisme de la phosphatidyléthanolamine dans la santé et la maladie. Revue internationale de biologie cellulaire et moléculaire (Vol. 321). Elsevier Inc.
- Gibellini, F. et Smith, T. K. (2010). La synthèse de la voie Kennedy-de novo de la phosphatidyléthanolamine et de la phosphatidylcholine. IUBMB Life, 62 (6), 414-428.
- Harayama, T., et Riezman, H. (2018). Comprendre la diversité de la composition lipidique membranaire. Nature Reviews Biologie cellulaire moléculaire, 19 (5), 281-296.
- Luckey, M. (2008). Biologie structurale membranaire: avec fondements biochimiques et biophysiques. Presse universitaire de Cambrudge. Récupéré de cambrudge.org
- Seddon, J. M., Cevc, G., Kaye, R. D., et Marsh, D. (1984). Etude par diffraction des rayons X du polymorphisme des diacyl- et dialkylphosphatidyléthanolamines hydratées. Biochimie, 23 (12), 2634-2644.
- Sendecki, A. M., Poyton, M. F., Baxter, A. J., Yang, T., et Cremer, P. S. (2017). Bicouches lipidiques prises en charge avec la phosphatidyléthanolamine comme composant principal. Langmuir, 33 (46), 13423-13429.
- van Meer, G., Voelker, D. R. et Feignenson, G. W. (2008). Lipides membranaires: où ils se trouvent et comment ils se comportent. Avis sur la nature, 9, 112-124.
- Vance, J. E. (2003). Biologie moléculaire et cellulaire du métabolisme de la phosphatidylsérine et de la phosphatidyléthanolamine. Dans K. Moldave (Ed.), Progress Nucleic Acid Research and Molecular Biology (pp. 69-111). Presse académique.
- Vance, J. E. (2008). Phosphatidylsérine et phosphatidyléthanolamine dans les cellules de mammifères: deux aminophospholipides métaboliquement apparentés. Journal of Lipid Research, 49 (7), 1377-1387.
- Vance, J. E. et Tasseva, G. (2013). Formation et fonction de la phosphatidylsérine et de la phosphatidyléthanolamine dans les cellules de mammifères. Biochimica et Biophysica Acta - Biologie moléculaire et cellulaire des lipides, 1831 (3), 543-554.
- Watkins, S. M., Zhu, X. et Zeisel, S. H. (2003). L'activité de la phosphatidyléthanolamine-N-méthyltransférase et la choline alimentaire régulent le flux lipidique hépatique et plasmatique et le métabolisme des acides gras essentiels chez la souris. Le Journal de la nutrition, 133 (11), 3386-3391.



Personne n'a encore commenté ce post.