
Processus hémostatique d'hémostase, primaire et secondaire
La hémostase Il s'agit d'un ensemble de processus physiologiques qui vise à arrêter le saignement en cas de lésion d'un vaisseau sanguin. Ce mécanisme comprend la formation d'un bouchon ou d'un caillot qui arrête le saignement, puis tous les mécanismes de réparation des dommages..
Le but de l'hémostase est de garder intact le système cardiovasculaire, qui est un système de circulation fermé. Le système hémostatique fonctionne donc comme un plombier dans un système de canalisation d'eau, colmatant les fuites ou les fuites, puis les réparant pour restaurer la structure endommagée..
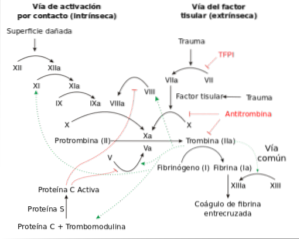
Comme le processus hémostatique est assez complexe et implique la participation de nombreux mécanismes physiologiques différents, il a été divisé en deux processus afin de faciliter son étude. Ainsi, on parle d'hémostase primaire et d'hémostase secondaire..
L'hémostase primaire concerne l'étude initiale du processus hémostatique, c'est-à-dire la formation du bouchon plaquettaire. L'hémostase secondaire prend en charge le processus de coagulation lui-même.
Il y a deux mille ans, le philosophe grec Platon décrivait que «le sang, lorsqu'il quittait le corps, formait des fibres». Platon a été le premier à utiliser le terme "Fibrine"En référence au sang.
Cette description a ensuite été acceptée par de nombreux autres philosophes, mais ce n'est qu'à la fin des années 1800 et au début des années 1900 que les plaquettes ont été découvertes et que le premier modèle du mécanisme de coagulation a été créé..
Index des articles
- 1 Processus hémostatique
- 2 Hémostase primaire
- 2.1 Vasoconstriction
- 2.2 Formation du bouchon plaquettaire
- 3 Hémostase secondaire
- 3.1 Formation de caillots
- 3.2 Rétraction du caillot
- 3.3 Lyse des caillots
- 4 Références
Processus hémostatique
Lorsqu'un vaisseau sanguin est endommagé, trois processus sont activés séquentiellement. Premièrement, une vasoconstriction locale se produit, c'est-à-dire que le muscle lisse de la paroi vasculaire se contracte, réduisant le diamètre du vaisseau pour réduire la perte de sang.
Parfois, lorsque les vaisseaux sont très petits, la constriction est si efficace qu'elle obstrue la lumière du tube et arrête d'elle-même le saignement..
Une lésion de l'endothélium vasculaire favorise l'adhésion des plaquettes au site de la lésion et cette adhésion plaquettaire favorise l'agrégation d'un plus grand nombre de plaquettes qui finissent par occlure le site de la lésion ou, dans les petits vaisseaux, peuvent obstruer le vaisseau et arrêter la circulation sanguine dans le vaisseau. navire affecté.
Ce processus est auto-limité, de sorte que le bouchon plaquettaire ne se propage pas dans tout le vaisseau, et constitue le deuxième processus.
Le caillot sanguin est alors formé par l'activation séquentielle d'une série d'enzymes du système de coagulation qui circulent dans le sang sous leur forme inactive. Ces processus arrêtent le saignement, mais la circulation doit être rétablie (troisième processus).
Par conséquent, une fois l'objectif initial atteint, qui est d'éviter les fuites, les parois du vaisseau sont réparées et maintenant le caillot formé est lissé ou détruit (fibrinolyse) et le sang circule à nouveau normalement à travers tout le vaisseau parfaitement reconstitué..
L'ensemble de ce processus hémostatique complexe est rigoureusement régulé, de sorte que ses effets sont limités à la zone lésée et que les dommages sont rapidement contenus. Les altérations de l'équilibre physiologique ou de la régulation de l'hémostase donnent lieu à des états pathologiques accompagnés de thrombose ou d'hémorragie.
Hémostase primaire
L'hémostase primaire fait référence à tous les processus qui permettent au bouchon plaquettaire de se former. Cela implique l'adhésion, l'activation, la sécrétion et l'agrégation des plaquettes..
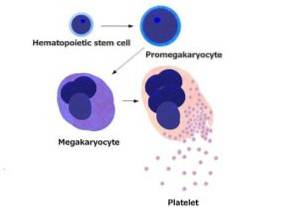
Les plaquettes sont de petits fragments cellulaires sans noyau de 1 à 4 microns de diamètre. Ceux-ci sont formés par le fractionnement de cellules produites par la moelle osseuse qui sont appelées mégacaryocytes. Les plaquettes ont une demi-vie de 8 à 12 jours et sont des structures très actives.
Vasoconstriction
Dans le processus d'hémostase, la première chose qui se produit est une vasoconstriction due à la contraction du muscle lisse de la paroi vasculaire dans la zone de la blessure. Cette contraction est produite par effet mécanique direct de l'élément qui a blessé le vaisseau et / ou par activation des fibres nerveuses périvasculaires.
Formation de bouchon plaquettaire
Lorsqu'un vaisseau sanguin est blessé, le collagène situé juste en dessous de l'endothélium est exposé et les plaquettes y adhèrent et s'activent. Lorsqu'il est activé, les plaquettes attachées libèrent adénosine diphosphate (ADP) et thromboxane Adeux. Ces substances induisent à leur tour l'adhésion et l'activation de plus de plaquettes.
L'adhésion et l'agrégation peuvent se poursuivre jusqu'à ce que l'un des vaisseaux blessés de petit calibre soit complètement obstrué. Initialement, le bouchon plaquettaire est lâche, puis lors du processus de coagulation suivant, les brins de fibrine le transformeront en un bouchon rigide.
Dans les zones adjacentes à la lésion vasculaire, les cellules endothéliales commencent à sécréter prostafiline, qui est une substance ayant des effets antiplaquettaires, c'est-à-dire qu'elle empêche les plaquettes d'adhérer.
La sécrétion de prostafiline par l'endothélium vasculaire dans les zones saines périphériques à la lésion, il délimite l'extension, le long du vaisseau, du bouchon plaquettaire et le confine à la zone lésée.
Les plaquettes activées sécrètent également sérotonine, une substance capable d'améliorer la vasoconstriction. De plus, ils sécrètent thromboplastine, qui est une substance qui active une partie de la cascade de coagulation, comme cela sera décrit plus loin.
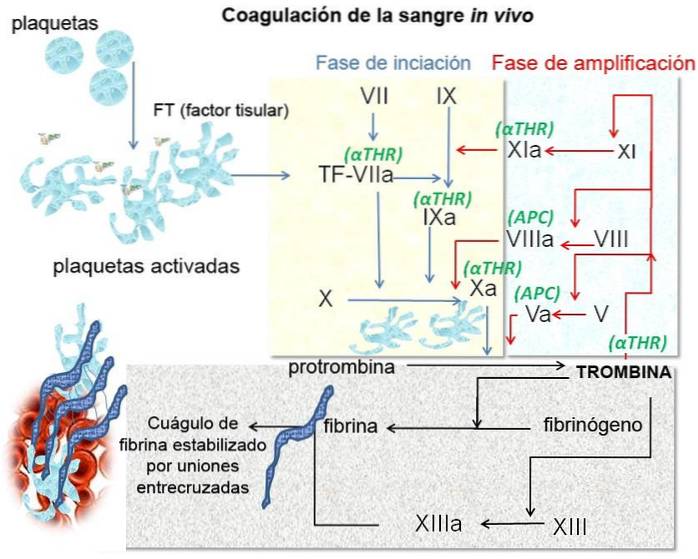
Par le Dr Graham Beards (et) [CC BY-SA 4.0 (https://creativecommons.org/licenses/by-sa/4.0)], via Wikimedia Commons
D'autres substances sécrétées par les plaquettes sont des protéines appelées «facteur de stabilisation de la fibrine» et «facteur de croissance». Le facteur de croissance induit la croissance des cellules endothéliales, des fibroblastes et des cellules musculaires lisses du vaisseau lésé.
L'effet final de la croissance des structures de la paroi vasculaire induite par les facteurs de croissance libérés par les plaquettes est d'initier la réparation de la lésion vasculaire..
Hémostase secondaire
L'hémostase secondaire fait référence au processus de coagulation lui-même. C'est un processus enzymatique qui implique une cascade de réactions par lesquelles le fibrinogène soluble est converti en fibrine, une substance insoluble qui polymérise et réticule pour former un caillot stable..
Dans les lésions vasculaires étendues, le caillot commence à apparaître environ 15 à 20 secondes après la blessure. En revanche, dans les blessures mineures, cela apparaît 1 à 2 minutes plus tard.
Trois types de substances sont responsables du démarrage de cette cascade enzymatique.
1- Activation des substances de la paroi vasculaire lésée.
2- Substances produites par les plaquettes.
3- Protéines sanguines qui adhèrent à la paroi vasculaire lésée.
Plus de 50 substances liées aux processus de coagulation sanguine ont été trouvées. Ceux-ci peuvent être classés en ceux qui favorisent la coagulation, appelés procoagulants, et ceux qui inhibent la coagulation, appelés anticoagulants..
L'équilibre entre l'activité de ces deux groupes de substances sera responsable de la coagulation ou non du sang. Normalement, les anticoagulants prédominent, à l'exception de la zone où survient un traumatisme vasculaire dans lequel l'activité des substances procoagulantes prédomine.
Formation d'un caillot
La cascade d'activation enzymatique finit par activer un groupe de substances appelées collectivement activateur de prothrombine. Ces activateurs de prothrombine catalysent la transformation de la prothrombine en thrombine, et cette dernière agit comme une enzyme qui convertit le fibrinogène en fibrine..
La fibrine est une protéine fibreuse qui polymérise et forme un réseau dans lequel elle emprisonne les plaquettes, les cellules sanguines et le plasma. Ces fibres de fibrine adhèrent en outre à la surface lésée du vaisseau. Voici comment se forme le caillot.
Rétraction du caillot
Une fois formé, le caillot commence à se rétracter et élimine tout le sérum qui se trouvait à l'intérieur. Le liquide pressé est du sérum et non du plasma, car il ne contient pas de facteurs de coagulation ou de fibrinogène..
Les plaquettes sont essentielles à la rétraction du caillot. Ceux-ci produisent le facteur de stabilisation fibrine, qui est une substance procoagulante. De plus, ils contribuent directement au processus de rétraction en activant leurs propres protéines contractiles (myosine)..
Lyse des caillots
Une protéine plasmatique appelée plasminogène, également appelée profibrinolysine, est piégée dans le caillot avec d'autres protéines plasmatiques. Les tissus vasculaires blessés et l'endothélium libèrent un puissant activateur du plasminogène appelé activateur tissulaire du plasminogène (t-PA).
La libération de t-PA est lente et s'achève en quelques jours après la formation du caillot et l'arrêt du saignement. Le T-PA active le plasminogène et le convertit en plasmine, une enzyme protéolytique qui digère les fibres de fibrine et une grande partie des facteurs de coagulation confinés dans le caillot.
Ainsi, la plasmine élimine le caillot une fois le vaisseau réparé. Si le caillot se trouvait dans un petit vaisseau obstruant la circulation sanguine, l'effet de la plasmine redirige le vaisseau et l'écoulement est rétabli. Ainsi conclut le processus hémostatique.
Les références
- Best et Taylor's Physiological Basis of Medical Practice, 12e éd. (1998) William et Wilkins.
- Ganong, W. F. et Barrett, K. E. (2012). Examen de la physiologie médicale par Ganong. McGraw-Hill Médical.
- Guyton AC, Hall JE: Les compartiments des fluides corporels: Fluides extracellulaires et intracellulaires; Œdème, dans Manuel de physiologie médicale, 13e éd., AC Guyton, JE Hall (éd.). Philadelphie, Elsevier Inc., 2016.
- Smyth, S. S., McEver, R. P., Weyrich, A. S., Morrell, C. N., Hoffman, M. R., Arepally, G. M.,… et 2009 Participants au colloque sur les plaquettes. (2009). Fonctions plaquettaires au-delà de l'hémostase. Journal de la thrombose et de l'hémostase, 7(11), 1759-1766.
- Versteeg, H. H., Heemskerk, J. W., Levi, M., et Reitsma, P. H. (2013). Nouveaux fondamentaux de l'hémostase. Examens physiologiques, 93(1), 327-358.



Personne n'a encore commenté ce post.