
Applications d'héritage mitochondrial, pathologies, préventions

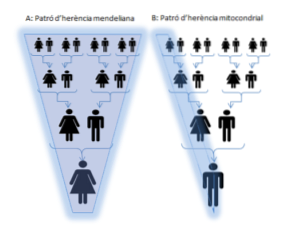
La héritage mitochondrial C'est la transmission de l'ADN mitochondrial à travers des organites appelées «mitochondries» et se produit des parents à leurs descendants. En règle générale, l'hérédité se produit uniquement à partir des mitochondries maternelles, de manière «matrilinéaire»..
Cependant, Shiyu Luo et ses collègues ont publié un article en janvier 2019 dans lequel ils ont trouvé des preuves que, en de rares occasions, l'ADN mitochondrial peut être hérité des deux parents..
La plupart du matériel génétique des cellules eucaryotes se trouve dans le noyau cellulaire. Cependant, une petite partie de l'ADN se trouve à l'intérieur des mitochondries..
Le matériel génétique à l'intérieur de cet organite est connu sous le nom d'ADN mitochondrial, qui est organisé en un chromosome circulaire, qui chez les mammifères a une longueur comprise entre 16 000 et 16 800 paires de bases..
On a observé que des mutations dans l'ADN mitochondrial provoquaient des maladies graves chez les individus et, dans la plupart des cas, les maladies ne sont héritées que de la mère à l'enfant, lorsque les mitochondries maternelles ont des mutations dans leur ADN..
Toutes les mitochondries des descendants proviennent d'un petit groupe de mitochondries présentes dans l'ovule au moment de la formation du zygote (fusion de l'ovule et du sperme) donc, dans la plupart des cas, les mitochondries du fœtus ne sont héritées que de sa mère.
Index des articles
- 1 Fusion de gamètes et transfert de mitochondries
- 2 Héritage biparental
- 3 applications
- 4 Pathologies et préventions
- 5 Références
Fusion de gamètes et transfert de mitochondries
Au moment de la fécondation de l'ovule (gamète femelle), le sperme ou le gamète mâle apporte quelques mitochondries à l'embryon en développement.
Cette contribution se produit au moment du contact du sperme avec la membrane plasmique de l'ovule, puisque les deux membranes fusionnent et le sperme pénètre dans le cytoplasme de l'ovule, y vidant son contenu interne..
Dans la plupart des taxons du règne animal, il existe une «tendance» à l'hérédité sous une forme clonale ou uniparentale de mitochondries et d'ADN mitochondrial (presque toujours par rapport aux mères). Dans certaines familles d'animaux, il existe des mécanismes de destruction des mitochondries paternelles transmises par les spermatozoïdes.
L'ovule chez les mammifères a des centaines de mitochondries, qui représentent environ 1/3 de l'ADN total de ces cellules sexuelles; tandis que le sperme n'en a que quelques-uns dans une région intermédiaire entre le flagelle et la tête.
Les œufs humains contiennent plus de 100 000 copies d'ADN mitochondrial; pendant ce temps, le sperme n'en a qu'environ 100, mais la quantité varie en fonction de l'espèce en question.
Cela rend évident que la grande majorité des mitochondries dans les cellules des descendants sont de transmission maternelle. Par conséquent, si les mitochondries des ovules présentent des mutations nocives ou délétères, ces mutations seront transmises à leurs descendants..
Héritage biparental
Le scientifique Hutchinson, en 1974, a été l'un des premiers à affirmer que l'hérédité des mitochondries se faisait de manière strictement maternelle (matrilinéaire). Cependant, au début du 20e siècle, White et ses collègues ont observé que chez certaines moules, l'hérédité mitochondriale n'était pas strictement maternelle..
Plus tard, en 2008, cette observation chez les moules a été désignée comme un type d '«hétéroplasmie», qui désigne la «fuite» de mitochondries et d'ADN mitochondrial paternel dans la progéniture..
De nombreuses autres observations ont identifié la présence de mitochondries paternelles et d'ADN mitochondrial chez les moules comme étant naturelles..
Shiyu Luo et ses collègues ont identifié trois personnes de trois familles humaines présentant une hétéroplasmie mitochondriale inhabituelle de l'ADN. Ces hétéroplasmies ne pouvaient pas être expliquées par la descente de l'ADN mitochondrial maternel, de sorte que ces auteurs ont effectué un séquençage de nouvelle génération de l'ADN mitochondrial des deux parents et des deux grands-parents des trois personnes..
De cette façon, l'hétéroplasmie inhabituelle a été identifiée comme un produit de la contribution de l'ADN mitochondrial des deux grands-parents, la grand-mère et le grand-père. En outre, les auteurs ont identifié deux autres familles non apparentées présentant une transmission mitochondriale biparentale..
Cette recherche était le premier rapport sur l'hérédité mitochondriale de manière biparentale chez l'homme..
Luo et al suggèrent que l'hétéroplasmie due à la transmission de l'ADN mitochondrial paternel est omise dans les diagnostics lorsqu'elle ne cause aucune maladie chez les individus qui la portent..
Applications
El ADN mitocondrial fue introducido en la genética de poblaciones, en la filogenia y en los estudios evolutivos por el doctor John C. Avise en 1979 y en la actualidad esta es una de las herramientas más poderosas para el estudio de la genética de poblaciones de todos les êtres vivants.
En retraçant la généalogie de l'ADN mitochondrial des humains, une immense quantité d'études génétiques a été menée pour tenter de déterminer avec précision l'origine de l'humanité..
Même, sur la base de l'ADN mitochondrial maternel, il a été déterminé que toutes les personnes dans le monde peuvent être classées dans environ 40 groupes différents d'haplotypes mitochondriaux, étroitement liés à différentes zones géographiques du monde..
De nombreuses maisons commerciales telles que "Oxford Ancestor" proposent de retracer tous les ancêtres des personnes en utilisant l'héritage de l'ADN mitochondrial..
Le fondateur d'Oxford Ancestor, Bryan Sykes, a utilisé l'ADN mitochondrial pour classer tous les Européens en clans fondés par les «Sept Filles d'Eve». C'est le titre que Sykes a attribué à un livre qu'il a écrit en essayant de retracer l'origine de tous les Européens.
Dans son livre, Bryan Sykes suit l'héritage mitochondrial de tous les citoyens européens à travers le séquençage de l'ADN mitochondrial de milliers de personnes, localisant l'origine de tous les Européens chez sept femmes qui existaient avant la dernière période glaciaire, il y a 45000 ans..
Pathologies et préventions
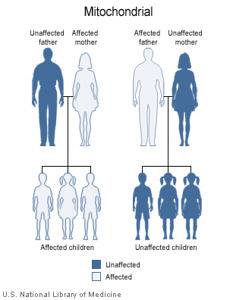
Des mutations nocives dans les gènes de l'ADN mitochondrial provoquent de multiples maladies au niveau systémique. Ces mutations peuvent être transmises par héritage mitochondrial par la mère et, rarement, par le père..
Une mutation dans l'ADN mitochondrial peut causer des problèmes en raison de l'absence ou de l'endommagement des enzymes impliquées dans la respiration cellulaire. Ces dommages entraînent une réduction de l'approvisionnement en ATP des cellules, entraînant un dysfonctionnement des systèmes du corps..
Cependant, à de nombreuses occasions, les gens héritent de divers types de mitochondries de leur mère, certaines fonctionnelles et d'autres défectueuses; par conséquent, les mitochondries avec des gènes fonctionnels peuvent compenser le dysfonctionnement des mitochondries défectueuses.
Actuellement, des recherches sont en cours pour transférer des noyaux cellulaires qui peuvent permettre aux femmes qui souffrent de maladies dues à des mutations nocives dans les mitochondries d'avoir des enfants en bonne santé..
La méthode de transfert de noyaux consiste à extraire le noyau cellulaire de l'ovule de la mère avec les mitochondries affectées et à l'insérer dans des ovules donnés normaux, à partir desquels le noyau cellulaire a été préalablement extrait..
Par la suite, l'ovule peut être fécondé par le sperme du partenaire du patient dans un in vitro. Cette technique a suscité la controverse car les fœtus conçus auraient l'ADN de trois parents différents.
Les références
- Adam, M. P., Ardinger, H. H., Pagon, R. A., Wallace, S. E., Bean, L. J. H., Stephens, K., & Amemiya, A. Aperçu des troubles mitochondriaux-GeneReviews®.
- Aiello, L. B. et Chiatti, B. D. (2017). Primer in genetics and genomics, article 4-Inheritance patterns. Recherche biologique pour les soins infirmiers, 19 (4), 465-472.
- Avise, J. C., Giblin-Davidson, C., Laerm, J., Patton, J. C., et Lansman, R. A. (1979). Clones d'ADN mitochondrial et phylogénie matriarcale au sein et parmi les populations géographiques du gopher de poche, Geomys pinetis. Actes de l'Académie nationale des sciences, 76 (12), 6694-6698.
- Hadjivasiliou, Z., Lane, N., Seymour, R. M. et Pomiankowski, A. (2013). Dynamique de l'hérédité mitochondriale dans l'évolution des types d'accouplement binaires et des deux sexes. Actes de la Royal Society B: Biological Sciences, 280 (1769), 20131920.
- HUTCHISON III, C.A., Newbold, J. E., Potter, S. S., et Edgell, M. H. (1974). Héritage maternel de l'ADN mitochondrial de mammifères. Nature, 251 (5475), 536.
- McWilliams, T. G., et Suomalainen, A. (2019). Le destin des mitochondries d'un père. Nature, 565 (7739), 296-297.
- Sutovsky, P. (2019). Base cellulaire et moléculaire de l'héritage mitochondrial. Springer.



Personne n'a encore commenté ce post.