
Physiologie de l'inotropisme, évaluation, altérations
le inotropisme est un terme médical qui fait référence à la capacité de la pompe cardiaque à se contracter. Il forme, avec le chronotropisme, le dromotropisme et le bathmotropisme, les 4 propriétés fondamentales du cœur d'un point de vue fonctionnel.
L'origine étymologique du mot a 3 composantes du grec ancien. jenous, qui signifie "nerf" ou "fibre"; Tropos, qui signifie "changer", "tourner" ou "tourner" et enfin -isme, un suffixe formant un nom largement utilisé dans les langues avec des racines latines. Cela traduirait littéralement «changement dans les fibres» qui a été adapté à la «contraction».

Bien que l'utilisation du terme soit réservée presque exclusivement au cœur, rien dans la littérature médicale ne le confirme. L'inotropisme pouvait être appliqué à n'importe quel muscle du corps et en fait c'était le cas dans les publications classiques, mais les auteurs actuels ont arrêté de le faire. L'inotropisme hors du cœur n'est pas compris aujourd'hui.
L'inotropisme, comme toute autre propriété du cœur, peut être altéré. Bien qu'ils ne soient pas toujours symptomatiques, si le patient qui en souffre présente des signes d'insuffisance cardiaque, il doit recevoir un traitement, qui visera presque toujours à améliorer ou à augmenter la capacité contractile du cœur..
Index des articles
- 1 Physiologie
- 1.1 Calcium
- 1.2 Fibre myocardique
- 1.3 Valves auriculo-ventriculaires
- 2 Évaluation de l'inotropisme
- 3 Altérations de l'inotropisme
- 3.1 Médicaments
- 4 Références
Physiologie
Lors de la contraction du cœur, toutes les fibres musculaires doivent être activées et les seuls mécanismes qui peuvent modifier la génération de force sont les changements de longueur ou de précharge des fibres (activation en fonction de la longueur) et les changements d'inotropisme (activation indépendante de la longueur).
La contraction des fibres musculaires cardiaques dépend essentiellement de la disponibilité intracellulaire des ions calcium. Il existe d'autres mécanismes de régulation de l'inotropisme cardiaque, qui seront évoqués plus loin, mais c'est la concentration en calcium qui est la plus importante dans un cadre non pathologique..
Calcium
La plupart des voies de régulation de l'inotropisme impliquent définitivement le calcium. Ce cation peut modifier positivement la contraction cardiaque de trois manières fondamentales:
- Augmenter son débit pendant le potentiel d'action (principalement pendant la phase 2 du potentiel d'action).
- Augmentation de sa libération par le réticulum sacroplasmique (principal stock de calcium intracellulaire).
- Sensibiliser à la troponine-C.
Ces trois effets du calcium favorisent la contractilité cardiaque, mais limitent également sa durée. En fermant les canaux calciques du cytoplasme cellulaire et du réticulum sarcoplasmique, grâce à l'activation des canaux potassiques, le potentiel d'action cesse soudainement et le calcium intracellulaire est éliminé en peu de temps.
Ce processus est répété cycliquement à chaque battement de cœur. Cet afflux et cette sortie constants de calcium, avec l'activation des canaux sodium et potassium, assurent une contraction cardiaque efficace..
Fibre myocardique
L'intégrité de la fibre myocardique est un autre des éléments fondamentaux dont dépend l'inotropisme. S'il y a des dommages aux fibres musculaires du cœur qui compromettent la précharge, la quantité de calcium disponible n'aura pas d'importance, le battement ne sera jamais complètement efficace et il y aura des altérations de la fonction de la pompe..
La précharge dépend de la longueur et de la tension de la fibre cardiaque. Ce phénomène est régi par la loi Frank-Starling qui se lit comme suit: "L'énergie de contraction du ventricule dépend de la longueur initiale des fibres myocardiques ". Cela signifie que plus la fibre myocardique est étirée en fin de diastole, plus la force de contraction est grande..
En bref, la fibre myocardique se comporte comme un ressort. Plus le ressort ou la fibre myocardique est étiré au fur et à mesure que le cœur se remplit de sang, plus la force se libère lorsque le ressort est relâché, c'est-à-dire la contraction. Mais si le ressort est cassé ou si la fibre est endommagée, l'énergie sera insuffisante pour générer un rythme cardiaque efficace..
Valves auriculo-ventriculaires
Bien qu'elles jouent un rôle mineur, l'intégrité des valves auriculo-ventriculaires est très importante pour obtenir une contraction adéquate du cœur..
Leur fermeture lors de la première phase de systole provoque l'augmentation de la pression intraventriculaire nécessaire pour distendre la fibre cardiaque et produire une contraction correcte..
Cela signifie que si les valves sont endommagées ou malades, le ventricule ne se remplit pas correctement en raison d'un retour pathologique du sang vers les oreillettes, la fibre cardiaque n'est pas distendue et l'énergie libérée ne déclenche pas la force contractile nécessaire à un rythme cardiaque normal..
Évaluation de l'inotropisme
Bien qu'il n'existe actuellement aucune méthode spécifique pour calculer l'inotropisme, il existe des moyens indirects de le faire. La la fraction d'éjection, mesurée par échocardiographie ou cathétérisme, c'est une bonne technique pour déduire cliniquement la qualité de la contraction cardiaque.
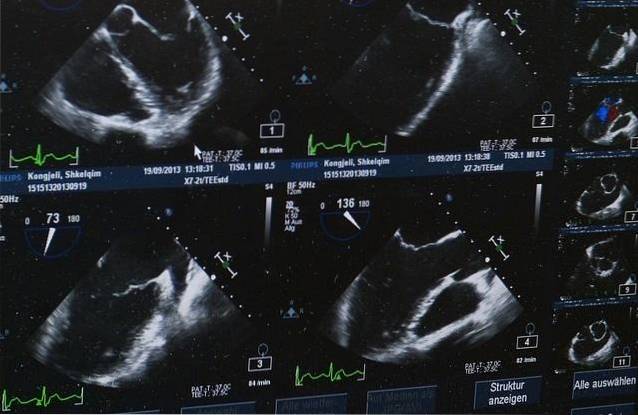
L'utilité de l'échocardiographie est un peu plus large. Il permet d'estimer (sans certitude absolue) la pression de raccourcissement et l'augmentation de la pression / du temps, deux paramètres complexes mais précieux pour évaluer la contractilité du cœur..
L'activité des valves auriculo-ventriculaires peut également être évaluée par échocardiographie..
Altérations de l'inotropisme
Tout changement pathologique de l'inotropisme peut entraîner une insuffisance cardiaque. Il en va de même pour les trois autres propriétés fonctionnelles de base du cœur..
Par conséquent, face à tout tableau clinique compatible avec ladite maladie, une évaluation globale doit être réalisée pour déterminer le niveau d'échec..
Compte tenu de la physiologie de l'inotropisme, les troubles calciques sont parmi les causes les plus importantes d'anomalie contractile. Des taux de calcium élevés ou faibles peuvent affecter la fonction cardiaque. Des études sur le myocarde chez des patients souffrant d'insuffisance cardiaque ont montré des échecs dans l'utilisation du calcium cytosolique et dans la puissance des myocytes.
Les fibres myocardiques malades modifient également la contractilité du cœur. De nombreuses personnes après un infarctus du myocarde avec des lésions tissulaires importantes souffrent d'insuffisance cardiaque en raison de lésions des fibres musculaires.
Les patients hypertendus chroniques et les patients chagasiques perdent la compliance du muscle cardiaque et donc diminuent la force contractile.
Médicaments
Certains médicaments couramment utilisés peuvent compromettre l'inotropisme cardiaque. Les inhibiteurs calciques, largement utilisés dans le traitement de l'hypertension artérielle, ont un effet inotrope négatif. Le même scénario se produit avec les bêtabloquants et la plupart des antiarythmiques..
Les références
- Serra Simal, Rafael (2011). Contractilité ou inotropisme. Récupéré de: webfisio.es
- Département des sciences physiologiques (2000). Fonction ventriculaire: déterminants de la fonction cardiaque. Université pontificale Javeriana. Récupéré de: med.javeriana.edu.co
- Luna Ortiz, pasteur et collaborateurs (2003). Homéostasie calcique et fonction cardiovasculaire: implications anesthésiques. Journal mexicain d'anesthésiologie, 26 (2): 87-100.
- Torales-Ibañez (2012). Bloqueurs de canaux calciques. Récupéré de: med.unne.edu.ar
- Schaper, W. et al. (1972). Effets des médicaments sur l'inotropisme cardiaque. Àrchives Internationales de Pharmacodynamie et de Thérapie, 196: 79-80.
- Wikipédia (2017). Inotropisme. Récupéré de: es.wikipedia.org


Personne n'a encore commenté ce post.