
Structure du terbutyle, caractéristiques, formation, exemples
le terbutyle ou tertbutyle est un groupe ou substituant alkyle dont la formule est -C (CH3)3 et est dérivé de l'isobutane. Le préfixe tert- provient de tertiaire, car l'atome de carbone central, avec lequel ce groupe est lié à une molécule, est tertiaire (3e); c'est-à-dire qu'il forme des liaisons avec trois autres carbones.
Le terbutyle est peut-être le groupe butyle le plus important, au-dessus de l'isobutyle, n-butyle et sec-butyle. Ce fait est attribué à sa taille volumineuse, ce qui augmente les obstacles stériques qui affectent la manière dont une molécule participe à une réaction chimique..

Dans l'image du haut, le groupe tert-butyle est représenté, lié à une chaîne latérale R. Cette chaîne peut être constituée d'un squelette carboné et aliphatique (bien qu'il puisse également être aromatique, Ar), d'un groupe fonctionnel organique ou d'un hétéroatome.
Le terbutyl ressemble à des pales de ventilateur ou à un pied à trois doigts. Lorsqu'il englobe une grande partie de la structure d'une molécule, comme dans le cas de l'alcool tert-butylique, on dit que le composé en dérive; et si, au contraire, ce n'est qu'une fraction ou un fragment de la molécule, alors on dit que ce n'est rien de plus qu'un substituant.
Index des articles
- 1 Nomenclature et formation
- 2 Structure et caractéristiques
- 3 Exemples de terbutyle
- 3.1 Halogénures
- 3.2 alcool butylique tertiaire
- 3.3 Hypochlorite de terbutyle
- 3.4 Isocyanure de terbutyle
- 3,5 acétate de butyle tertiaire
- 3.6 Diterbutileter
- 3.7 Buprofézine
- 3.8 Avobenzone
- 4 Références
Nomenclature et formation
Au début, il a été précisé quelle est la raison pour laquelle ce groupe est appelé terbutyle. Cependant, c'est le nom commun sous lequel il est connu.
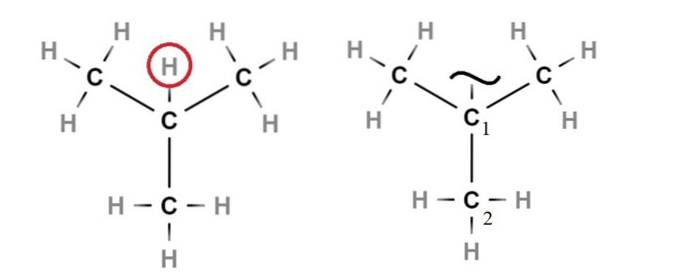
Son nom régi par l'ancienne nomenclature systématique, et actuellement également par la nomenclature IUPAC, est 1,1-diméthyléthyle. À droite de l'image supérieure, nous avons les carbones répertoriés, et on peut voir en effet que deux méthyle sont liés au carbone 1.
Il a également été dit que le terbutyle dérive de l'isobutane, qui est l'isomère structural le plus ramifié et le plus symétrique du butane..
En partant de l'isobutane (à gauche de l'image), le 3ème carbone central doit perdre son seul atome d'hydrogène (dans le cercle rouge), rompant sa liaison C-H pour que le radical terbutyle, · C (CH3)3. Lorsque ce radical parvient à se lier à une molécule ou à une chaîne latérale R (ou Ar), il devient un substituant ou un groupe tert-butyle.
De cette manière, les composés de formule générale RC (CH3)3 ou Rt-Bu.
Structure et caractéristiques
Le groupe tert-butyle est alkyle, ce qui signifie qu'il est dérivé d'un alcane, et qu'il est constitué uniquement de liaisons C-C et C-H. Par conséquent, il est hydrophobe et apolaire. Mais ce ne sont pas ses caractéristiques les plus marquantes. C'est un groupe qui prend trop de place, il est encombrant, et ce n'est pas étonnant puisqu'il comporte trois groupes CH3, grand en soi, lié au même carbone.
Chaque CH3 del -C (CH3)3 tourne, vibre, contribue aux interactions de son environnement moléculaire par les forces de dispersion de Londres. Pas assez avec un, il y a trois CH3 ceux qui tournent comme s'ils étaient les pales d'un ventilateur, l'ensemble du groupe terbutyle étant remarquablement volumineux par rapport aux autres substituants.
En conséquence, une entrave stérique constante apparaît; c'est-à-dire une difficulté spatiale pour deux molécules de se rencontrer et d'interagir efficacement. Le terbutyl affecte les mécanismes et le déroulement d'une réaction chimique, qui cherchera à se dérouler de manière à ce que l'encombrement stérique soit le moins possible.
Par exemple, les atomes proches de -C (CH3)3 ils seront moins sensibles aux réactions de substitution; le CH3 empêchera la molécule ou le groupe qui veut rejoindre la molécule de s'approcher.
En plus de ce qui a déjà été mentionné, le terbutyle a tendance à provoquer une diminution des points de fusion et d'ébullition, reflet d'interactions intermoléculaires plus faibles..
Exemples de terbutyle
Une série d'exemples de composés dans lesquels le tert-butyle est présent sera discutée ci-dessous. Celles-ci sont obtenues simplement en faisant varier les identités de R dans la formule RC (CH3)3.
Les halogénures
En substituant un atome d'halogène à R, on obtient les halogénures de tert-butyle. Ainsi, nous avons leurs fluorures, chlorures, bromures et iodures respectifs:
-FC (CH3)3
-ClC (CH3)3
-BrC (CH3)3
-IC (CH3)3
Parmi ceux-ci, le ClC (CH3)3 et BrC (CH3)3 sont les plus connus, étant des solvants organiques et des précurseurs d'autres composés organiques chlorés et bromés, respectivement.
Alcool butylique tertiaire
Alcool butylique tertiaire, (CH3) COH ou t-BuOH, est un autre des exemples les plus simples dérivés du terbutyle, qui se compose également de l'alcool tertiaire le plus simple de tous. Son point d'ébullition est de 82 ° C, celui de l'alcool isobutylique à 108 ° C. Cela montre comment la présence de ce grand groupe a un impact négatif sur les interactions intermoléculaires..
Hypochlorite de terbutyle
Remplacement de R pour l'hypochlorite, OCl- ou ClO-, nous avons le composé hypochlorite de terbutyle, (CH3)3COCl, dans lequel il se distingue par sa liaison covalente C-OCl.
Isocyanure de terbutyle

En remplaçant maintenant R par isocyanure, NC ou -N≡C, nous avons le composé terbutylisocyanure, (CH3)3CNC ou (CH3)3C-N≡C. Dans l'image ci-dessus, nous pouvons voir sa formule structurelle. Dans celui-ci, le terbutyle se détache à l'œil nu comme un éventail ou une jambe à trois doigts, et peut être confondu avec l'isobutyle (en forme de Y).
Acétate de tert-butyle
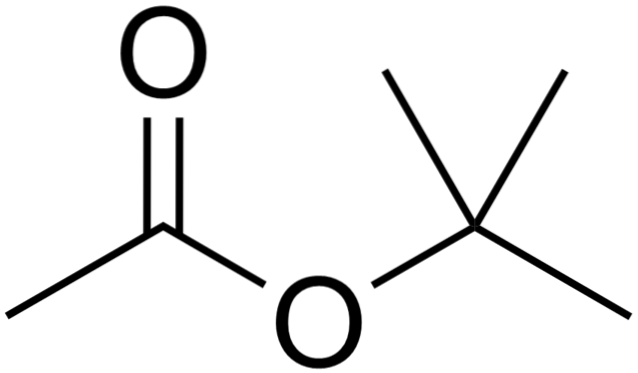
Nous avons également l'acétate de tert-butyle, CH3COOC (CH3)3 (image du haut), que nous obtenons en substituant R au groupe acétate. Le terbutyl commence à perdre sa priorité structurelle car il est lié à un groupe oxygéné.
Diterbutileter

Le diterbutyléther (image du haut) ne peut plus être décrit avec la formule RC (CH3)3, donc le tert-butyle dans ce cas se comporte simplement comme un substituant. La formule de ce composé est (CH3)3COC (CH3)3.
Notez que dans leur structure les deux groupes ou substituants terbutyle ressemblent à deux pattes, où les liaisons O-C sont les pattes de celles-ci; un oxygène avec deux pattes à trois doigts.
Jusqu'à présent, les exemples présentés étaient des composés liquides. Les deux derniers seront solides.
Buprofézine
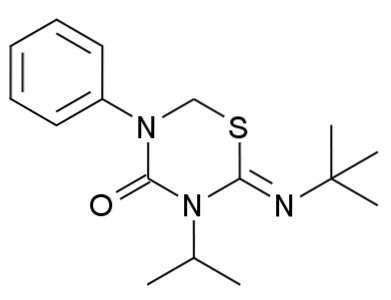
Dans l'image du haut, nous avons la structure de la buprofézine, un insecticide, où à l'extrême droite, nous pouvons voir la «jambe» du terbutyle. En bas, nous avons également le groupe isopropyle.
Avobenzone

Enfin, nous avons l'avobenzone, un ingrédient de la crème solaire en raison de sa grande capacité à absorber les rayons UV. Le terbutyle, encore une fois, est situé à droite de la structure en raison de sa similitude avec celle d'une jambe.
Le terbutyl est un groupe trop courant dans de nombreux composés organiques et pharmaceutiques. Sa présence modifie la manière dont la molécule interagit avec son environnement, car elle est considérablement volumineuse; et par conséquent, repousse sur son passage tout ce qui n'est pas aliphatique ou apolaire, comme les régions polaires des biomolécules..
Les références
- Morrison, R. T. et Boyd, R, N. (1987). Chimie organique. 5e édition. Éditorial Addison-Wesley Interamericana.
- Carey F. (2008). Chimie organique. (Sixième édition). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chimie organique. (10e édition.). Wiley plus.
- Wikipédia. (2020). Groupe Butyl. Récupéré de: en.wikipedia.org
- Steven A. Hardinger. (2017). Glossaire illustré de chimie organique: tert-butyle. Récupéré de: chem.ucla.edu
- James Ashenhurst. (2020). t-butyle. Récupéré de: masterorganicchemistry.com


Personne n'a encore commenté ce post.