
Structure de l'oxyde de fer, propriétés, nomenclature, utilisations
UNE oxyde de fer C'est l'un des composés formés entre le fer et l'oxygène. Ils se caractérisent par le fait qu'ils sont ioniques et cristallins, et sont dispersés en raison de l'érosion de leurs minéraux, composant les sols, la masse végétale et même l'intérieur des organismes vivants..
C'est alors l'une des familles de composés qui prédomine dans la croûte terrestre. Que sont-ils exactement? Seize oxydes de fer sont connus à ce jour, la plupart d'origine naturelle et d'autres synthétisés dans des conditions extrêmes de pression ou de température..

Une portion d'oxyde ferrique en poudre est représentée sur l'image ci-dessus. Sa couleur rouge caractéristique recouvre le fer de divers éléments architecturaux dans ce que l'on appelle la rouille. De même, il est observé sur les pentes, les montagnes ou les sols, mélangé à de nombreux autres minéraux, comme la poudre jaune de goethite (α-FeOOH).
Les oxydes de fer les plus connus sont l'hématite (α-FedeuxOU ALORS3) et de la maghémite (ϒ- FedeuxOU ALORS3), tous deux polymorphes de l'oxyde ferrique; et non des moindres, la magnétite (Fe3OU ALORS4). Leurs structures polymorphes et leur grande surface en font des matériaux intéressants comme sorbants, ou pour la synthèse de nanoparticules avec de larges applications..
Index des articles
- 1 Structure
- 1.1 Polymorphisme
- 1.2 Liens structurels
- 2 propriétés
- 3 Nomenclature
- 3.1 Nomenclature systématique
- 3.2 Nomenclature des stocks
- 3.3 Nomenclature traditionnelle
- 4 utilisations
- 4.1 Nanoparticules
- 4.2 Pigments
- 5 Références
Structure
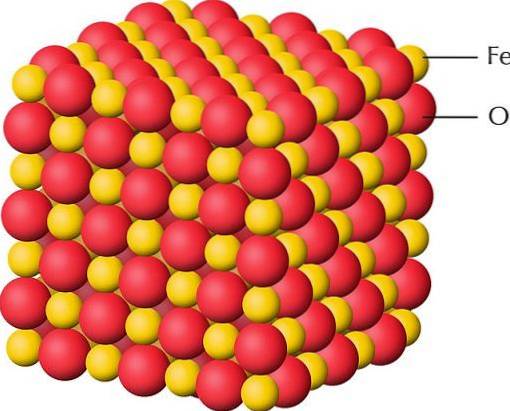
L'image du haut est une représentation de la structure cristalline de FeO, l'un des oxydes de fer où le fer a une valence de +2. Les sphères rouges correspondent aux anions Odeux-, tandis que les jaunes aux cations Fedeux+. Notez également que chaque foideux+ est entouré de six Odeux-, formant une unité octaédrique de coordination.
Par conséquent, la structure de FeO peut être "émiettée" en unités de FeO.6, où l'atome central est Fedeux+. Dans le cas des oxyhydroxydes ou hydroxydes, l'unité octaédrique est FeO3(OH)3.
Dans certaines structures, au lieu de l'octaèdre, il y a des unités tétraédriques, FeO4. Pour cette raison, les structures des oxydes de fer sont généralement représentées par des octaèdres ou des tétraèdres avec des centres de fer..
Les structures des oxydes de fer dépendent des conditions de pression ou de température, du rapport Fe / O (c'est-à-dire du nombre d'oxygène qu'il y a par fer et vice versa), et de la valence du fer (+2, +3 et, très rarement dans les oxydes synthétiques, +4).
En général, les anions volumineux Odeux- sont des feuilles de formation alignées dont les trous logent les cations Fedeux+ o foi3+. Ainsi, il existe des oxydes (comme la magnétite) qui ont des fers avec les deux valences.
Polymorphisme
Les oxydes de fer présentent un polymorphisme, c'est-à-dire des structures ou des arrangements cristallins différents pour le même composé. Oxyde ferrique, FedeuxOU ALORS3, a jusqu'à quatre polymorphes possibles. Hématite, α-FedeuxOU ALORS3, c'est le plus stable de tous; suivi de la maghémite, ϒ- FaithdeuxOU ALORS3, et par le β-Fe synthétiquedeuxOU ALORS3 et ε- FedeuxOU ALORS3.
Ils ont tous leurs propres types de structures et de systèmes cristallins. Cependant, le rapport 2: 3 reste constant, il y a donc trois anions Odeux- pour deux cations Fe3+. La différence réside dans la façon dont les unités octaédriques FeO sont situées.6 dans l'espace et comment êtes-vous réunis.
Liens structurels

Unités octaédriques FeO6 peut être visualisé en utilisant l'image ci-dessus. Aux coins de l'octaèdre se trouvent le Odeux-, tandis qu'en son centre la foideux+ o foi3+(dans le cas de FedeuxOU ALORS3). La façon dont ces octaèdres sont disposés dans l'espace révèle la structure de l'oxyde.
Cependant, ils influencent également la manière dont ils sont liés. Par exemple, deux octaèdres peuvent être joints en touchant deux de leurs sommets, ce qui est représenté par un pont oxygène: Fe-O-Fe. De même, les octaèdres peuvent se rejoindre par leurs bords (adjacents les uns aux autres). Il serait alors représenté par deux ponts oxygène: Fe- (O)deux-Foi.
Et enfin, les octaèdres peuvent interagir à travers leurs visages. Ainsi, la représentation serait maintenant avec trois ponts oxygène: Fe- (O)3-Fe. La manière dont les octaèdres sont liés ferait varier les distances internucléaires Fe-Fe et, par conséquent, les propriétés physiques de l'oxyde.
Propriétés
Un oxyde de fer est un composé aux propriétés magnétiques. Ceux-ci peuvent être anti, ferro ou ferrimagnétiques et dépendent des valences du Fe et de la manière dont les cations interagissent dans le solide..
Parce que les structures des solides sont très variées, leurs propriétés physiques et chimiques le sont aussi.
Par exemple, les polymorphes et hydrates de FedeuxOU ALORS3 ils ont des valeurs de points de fusion (qui varient entre 1 200 et 1 600 ° C) et des densités différentes. Cependant, ils ont en commun la faible solubilité due au Fe3+, la même masse moléculaire, sont de couleur brune et se dissolvent avec parcimonie dans les solutions acides.
Nomenclature
L'IUPAC établit trois façons de nommer un oxyde de fer. Tous les trois sont très utiles, bien que pour les oxydes complexes (tels que Fe7OU ALORS9) les règles systématiques sur les autres par sa simplicité.
Nomenclature systématique
Les nombres d'oxygène et de fer sont pris en considération, en les nommant avec les préfixes de numérotation grecs mono-, di-, tri-, etc. Selon cette nomenclature, le FedeuxOU ALORS3 il s'appelle: trioxyde de donnéfer. Et pour la foi7OU ALORS9 son nom serait: oxyde de fer non hepta.
Nomenclature des stocks
Cela considère la valence du fer. Si c'est à propos de Faithdeux+, l'oxyde de fer s'écrit ..., et sa valence avec des chiffres romains entre parenthèses. Pour la foideuxOU ALORS3 son nom est: oxyde de fer (III).
Notez que le Fe3+ peut être déterminé par des sommes algébriques. Si le Odeux- Il a deux charges négatives, et il y en a trois, elles totalisent -6. Pour neutraliser ce -6, il faut +6, mais il y a deux Fe, donc ils doivent être divisés par deux, + 6/2 = +3:
2X (valence métallique) + 3 (-2) = 0
En résolvant simplement X, la valence de Fe dans l'oxyde est obtenue. Mais si X n'est pas un entier (comme c'est le cas avec presque tous les oxydes restants), alors il y a un mélange de Fedeux+ et foi3+.
Nomenclature traditionnelle
Le suffixe -ico est donné au préfixe ferr- quand Fe a une valence +3, et -oso quand sa valence est 2+. Ainsi, le FedeuxOU ALORS3 ça s'appelle: oxyde ferrique.
Applications
Nanoparticules
Les oxydes de fer ont en commun une énergie de cristallisation élevée, ce qui permet de créer de très petits cristaux mais avec une grande surface..
Pour cette raison, ils sont d'un grand intérêt dans les domaines de la nanotechnologie, où ils conçoivent et synthétisent des nanoparticules d'oxyde (NP) à des fins spécifiques:
-Comme catalyseurs.
-En tant que réservoir de médicaments ou de gènes dans le corps
-Dans la conception de surfaces sensorielles pour différents types de biomolécules: protéines, sucres, graisses
-Pour stocker des données magnétiques
Des pigments
Parce que certains oxydes sont très stables, ils peuvent être utilisés pour teindre des textiles ou donner des couleurs vives aux surfaces de n'importe quel matériau. Des mosaïques sur les sols; peintures rouges, jaunes et orange (même vertes); céramique, plastique, cuir et même des œuvres architecturales.
Les références
- Administrateurs du Dartmouth College. (18 mars 2004). Stoechiométrie des oxydes de fer. Tiré de: dartmouth.edu
- Ryosuke Sinmyo et coll. (2016, 8 septembre). Découverte de Fe7OU ALORS9: un nouvel oxyde de fer à structure monoclinique complexe. Récupéré de: nature.com
- M. Cornell, U. Schwertmann. Les oxydes de fer: structure, propriétés, réactions, occurrences et utilisations. [PDF]. WILEY-VCH. Tiré de: epsc511.wustl.edu
- Alice Bu. (2018). Nanoparticules d'oxyde de fer, caractéristiques et applications. Tiré de: sigmaaldrich.com
- Ali, A., Zafar, H., Zia, M., ul Haq, I., Phull, A. R., Ali, J. S., et Hussain, A. (2016). Synthèse, caractérisation, applications et défis des nanoparticules d'oxyde de fer. Nanotechnology, Science and Applications, 9, 49-67. http://doi.org/10.2147/NSA.S99986
- Pigments de Golchha. (2009). Oxydes de fer: applications. Tiré de: golchhapigments.com
- Formulation chimique. (2018). Oxyde de fer (II). Tiré de: formulacionquimica.com
- Wikipédia. (2018). Oxyde de fer (III). Tiré de: https://en.wikipedia.org/wiki/Iron(III)_oxide


Personne n'a encore commenté ce post.