
Types de corps de cétogenèse, synthèse et dégradation
La cétogenèse C'est le processus par lequel l'acétoacétate, le β-hydroxybutyrate et l'acétone sont obtenus, qui sont ensemble appelés corps cétoniques. Ce mécanisme complexe et finement régulé se déroule dans les mitochondries, à partir du catabolisme des acides gras.
L'obtention des corps cétoniques a lieu lorsque le corps est soumis à des périodes de jeûne exhaustives. Bien que ces métabolites soient principalement synthétisés dans les cellules hépatiques, ils sont considérés comme une source d'énergie importante dans divers tissus, tels que les muscles squelettiques et dans les tissus cardiaques et cérébraux..
Le Β-hydroxybutyrate et l'acétoacétate sont des métabolites utilisés comme substrats dans le muscle cardiaque et le cortex rénal. Dans le cerveau, les corps cétoniques deviennent d'importantes sources d'énergie lorsque le corps a épuisé sa réserve de glucose.
Index des articles
- 1 Caractéristiques générales
- 2 Types et propriétés des corps cétoniques
- 3 Synthèse des corps cétoniques
- 3.1 Conditions de la cétogenèse
- 3.2 Mécanisme
- 3.3 La β-oxydation et la cétogenèse sont liées
- 3.4 Régulation de la β-oxydation et son effet sur la cétogenèse
- 4 Dégradation
- 5 Pertinence médicale des corps cétoniques
- 5.1 Diabète sucré et accumulation de corps cétoniques
- 6 Références
Caractéristiques générales
La cétogenèse est considérée comme une fonction physiologique ou une voie métabolique très importante. Généralement, ce mécanisme a lieu dans le foie, bien qu'il ait été démontré qu'il peut être réalisé dans d'autres tissus capables de métaboliser les acides gras.
La formation de corps cétoniques est la principale dérivation métabolique de l'acétyl-CoA. Ce métabolite est obtenu à partir de la voie métabolique connue sous le nom de β-oxydation, qui est la dégradation des acides gras.
La disponibilité de glucose dans les tissus où se produit la β-oxydation détermine le devenir métabolique de l'acétyl-CoA. Dans des situations particulières, les acides gras oxydés sont dirigés presque entièrement vers la synthèse des corps cétoniques..
Types et propriétés des corps cétoniques
Le principal corps cétonique est l'acétoacétate ou l'acide acétoacétique, qui est principalement synthétisé dans les cellules hépatiques. Les autres molécules qui composent les corps cétoniques sont dérivées de l'acétoacétate.
La réduction de l'acide acétoacétique donne naissance au D-β-hydroxybutyrate, le deuxième corps cétonique. L'acétone est un composé difficile à dégrader et produit par une réaction de décarboxylation spontanée de l'acétoacétate (il ne nécessite donc l'intervention d'aucune enzyme), lorsqu'il est présent à des concentrations élevées dans le sang.
La désignation des corps cétoniques a été établie par convention, puisque le β-hydroxybutyrate à proprement parler n'a pas de fonction cétone. Ces trois molécules sont solubles dans l'eau, ce qui facilite leur transport dans le sang. Sa fonction principale est de fournir de l'énergie à certains tissus tels que le muscle squelettique et cardiaque.
Les enzymes impliquées dans la formation des corps cétoniques se trouvent principalement dans les cellules hépatiques et rénales, ce qui explique pourquoi ces deux localisations sont les principaux producteurs de ces métabolites. Sa synthèse se produit uniquement et exclusivement dans la matrice mitochondriale des cellules.
Une fois ces molécules synthétisées, elles passent dans la circulation sanguine, se dirigeant vers les tissus qui en ont besoin, où elles sont dégradées en acétyl-CoA..
Synthèse des corps cétoniques
Conditions de la cétogenèse
Le devenir métabolique de l'acétyl-CoA résultant de la β-oxydation dépend des besoins métaboliques de l'organisme. Cela s'oxyde en COdeux et HdeuxOu via le cycle de l'acide citrique ou la synthèse d'acides gras, si le métabolisme des lipides et des glucides est stable dans l'organisme.
Lorsque le corps a besoin de la formation de glucides, l'oxaloacétate est utilisé pour la fabrication du glucose (gluconéogenèse) au lieu de démarrer le cycle de l'acide citrique. Cela se produit, comme mentionné, lorsque le corps a une certaine incapacité à obtenir du glucose, dans des cas tels que le jeûne prolongé ou la présence de diabète.
De ce fait, l'acétyl-CoA résultant de l'oxydation des acides gras est utilisé pour la production de corps cétoniques..
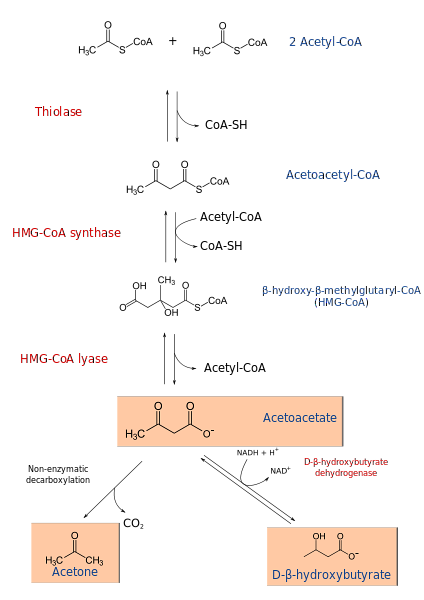
Mécanisme
Le processus de cétogenèse commence à partir des produits de la β-oxydation: l'acétacétyl-CoA ou l'acétyl-CoA. Lorsque le substrat est l'acétyl-CoA, la première étape consiste en la condensation de deux molécules, une réaction catalysée par l'acétyl-CoA transférase, pour produire de l'acétacétyl-CoA.
L'acétacétyl-CoA est condensé avec un troisième acétyl-CoA par l'action de l'HMG-CoA synthase, pour produire HMG-CoA (β-hydroxy-β-méthylglutaryl-CoA). L'HMG-CoA est dégradée en acétoacétate et acétyl-CoA par l'action de la HMG-CoA lyase. De cette manière, le premier corps cétonique est obtenu.
L'acétoacétate est réduit en β-hydroxybutyrate par l'intervention de la β-hydroxybutyrate déshydrogénase. Cette réaction dépend du NADH.
Le principal corps acétoacétate cétone est un β-cétoacide, qui subit une décarboxylation non enzymatique. Ce processus est simple et produit de l'acétone et du COdeux.
Cette série de réactions donne ainsi naissance à des corps cétoniques. Ceux-ci étant solubles dans l'eau peuvent être facilement transportés à travers la circulation sanguine, sans qu'il soit nécessaire de les ancrer à une structure albumine, comme c'est le cas des acides gras insolubles en milieu aqueux..
La Β-oxydation et la cétogenèse sont liées
Le métabolisme des acides gras produit les substrats de la cétogenèse, de sorte que ces deux voies sont fonctionnellement liées.
L'acétoacétyl-CoA est un inhibiteur du métabolisme des acides gras, car il arrête l'activité de l'acyl-CoA déshydrogénase, qui est la première enzyme de la β-oxydation. En outre, il exerce également une inhibition sur l'acétyl-CoA transférase et l'HMG-CoA synthase.
L'enzyme HMG-CoA synthase, subordonnée par la CPT-I (une enzyme impliquée dans la production d'acyl-carnitine en β-oxydation), joue un rôle régulateur important dans la formation des acides gras.
Régulation de la β-oxydation et son effet sur la cétogenèse
L'alimentation des organismes régule un ensemble complexe de signaux hormonaux. Les glucides, acides aminés et lipides consommés dans l'alimentation se déposent sous forme de triacylglycérols dans le tissu adipeux. L'insuline, une hormone anabolique, est impliquée dans la synthèse des lipides et la formation des triacylglycérols.
Au niveau mitochondrial, la β-oxydation est contrôlée par l'entrée et la participation de certains substrats dans les mitochondries. L'enzyme CPT I synthétise l'Acyl Carnitine à partir de l'Acyl CoA cytosolique.
Lorsque le corps est nourri, l'acétyl-CoA carboxylase est activée et le citrate augmente les niveaux de CPT I, tandis que sa phosphorylation diminue (réaction dépendante de l'AMP cyclique).
Cela provoque une accumulation de malonyl CoA, qui stimule la synthèse des acides gras et bloque leur oxydation, empêchant ainsi la génération d'un cycle futile..
Dans le cas du jeûne, l'activité carboxylase est très faible car les niveaux de l'enzyme CPT I ont été réduits et elle a également été phosphorylée, activant et favorisant l'oxydation des lipides, ce qui permettra par la suite la formation de corps cétoniques par acétyl- CoA.
Dégradation
Les corps cétoniques diffusent hors des cellules où ils ont été synthétisés et sont transportés vers les tissus périphériques par la circulation sanguine. Dans ces tissus, ils peuvent être oxydés par le cycle de l'acide tricarboxylique.
Dans les tissus périphériques, le β-hydroxybutyrate est oxydé en acétoacétate. Par la suite, l'acétoacétate présent est activé par l'action de l'enzyme 3-cétoacyl-CoA transférase.
Succinyl-CoA agit comme un donneur de CoA en se convertissant en succinate. L'activation de l'acétoacétate se produit pour empêcher le succinyl-CoA de se convertir en succinate dans le cycle de l'acide citrique, avec la synthèse couplée de GTP par l'action de la succinyl-CoA synthase.
L'acétoacétyl-CoA résultant subit une dégradation thiolytique produisant deux molécules d'acétyl-CoA qui sont incorporées dans le cycle de l'acide tricarboxylique, mieux connu sous le nom de cycle de Krebs..
Les cellules hépatiques manquent de 3-cétoacyl-CoA transférase, ce qui empêche l'activation de ce métabolite dans ces cellules. De cette manière, il est garanti que les corps cétoniques ne s'oxydent pas dans les cellules où ils ont été produits, mais qu'ils peuvent être transférés vers les tissus où leur activité est requise..
Pertinence médicale des corps cétoniques
Dans le corps humain, des concentrations élevées de corps cétoniques dans le sang peuvent provoquer des conditions spéciales appelées acidose et cétonémie..
La fabrication de ces métabolites correspond au catabolisme des acides gras et des glucides. L'une des causes les plus courantes d'un état de cétogenèse pathologique est la concentration élevée de fragments de dicarbonate acétique qui ne sont pas dégradés par la voie d'oxydation des acides tricarboxyliques..
En conséquence, il y a une augmentation des taux de corps cétoniques dans le sang au-dessus de 2 à 4 mg / 100 N et de leur présence dans l'urine. Cela entraîne une perturbation du métabolisme intermédiaire de ces métabolites..
Certains défauts des facteurs neuroglandulaires hypophysaires qui régulent la dégradation et la synthèse des corps cétoniques, ainsi que des troubles du métabolisme des hydrocarbures, sont à l'origine de l'hypercétonémie..
Diabète sucré et accumulation de corps cétoniques
Le diabète sucré (type 1) est une maladie endocrinienne qui entraîne une production accrue de corps cétoniques. Une production insuffisante d'insuline désactive le transport du glucose vers les muscles, le foie et le tissu adipeux, s'accumulant ainsi dans le sang.
Les cellules en l'absence de glucose entament le processus de gluconéogenèse et de dégradation des graisses et des protéines pour restaurer leur métabolisme. En conséquence, les concentrations d'oxaloacétate diminuent et l'oxydation des lipides augmente..
Il se produit alors une accumulation d'acétyl-CoA qui, en l'absence d'oxaloacétate, ne peut pas suivre la voie de l'acide citrique, provoquant ainsi la forte production de corps cétoniques, caractéristique de cette maladie..
L'accumulation d'acétone est détectée par sa présence dans l'urine et la respiration des personnes atteintes de cette maladie, et est en fait l'un des symptômes qui indiquent la manifestation de cette maladie.
Les références
- Blázquez Ortiz, C. (2004). Cétogenèse dans les astrocytes: caractérisation, régulation et rôle cytoprotecteur possible (Thèse de doctorat, Université Complutense de Madrid, Service des publications).
- Devlin, T. M. (1992). Manuel de biochimie: avec corrélations cliniques.
- Garrett, R. H., et Grisham, C. M. (2008). Biochimie. Thomson Brooks / Cole.
- McGarry, J. D., Mannaerts, G. P. et Foster, D. W. (1977). Un rôle possible du malonyl-CoA dans la régulation de l'oxydation hépatique des acides gras et de la cétogenèse. Le Journal d'investigation clinique, 60(1), 265-270.
- Melo, V., Ruiz, V. M. et Cuamatzi, O. (2007). Biochimie des processus métaboliques. Reverte.
- Nelson, D. L., Lehninger, A. L. et Cox, M. M. (2008). Principes de Lehninger de la biochimie. Macmillan.
- Pertierra, A. G., Gutiérrez, C. V., et autres, C. M. (2000). Fondamentaux de la biochimie métabolique. Éditorial Tébar.
- Voet, D., et Voet, J. G. (2006). Biochimie. Panamerican Medical Ed..


Personne n'a encore commenté ce post.