
Structure, propriétés, utilisations de l'acide stéarique (CH3 (CH2) 16COOH)

le acide stéarique est un composé organique solide dont la formule chimique est CH3(CHdeux)16COOH. C'est un acide carboxylique qui appartient au groupe des acides gras saturés à longue chaîne. Il est de couleur blanc jaunâtre et a une odeur similaire à celle du suif ou de la graisse animale..
Il est appelé acide gras car il est présent dans de nombreuses graisses et huiles animales et végétales. Il fait partie du métabolisme de la plupart des êtres vivants et se trouve généralement sous forme d'ester de glycérine.

Le cacao en contient une proportion élevée, ainsi que le suif des bovins, la graisse de porc et le beurre. Il est également présent dans les huiles végétales comme le maïs. Pour l'obtenir, la tristéarine est hydrolysée, c'est-à-dire qu'elle est traitée avec de l'eau et un alcali..
L'ingestion d'acide stéarique avec des aliments et son effet sur la santé pose actuellement des doutes pour les chercheurs. Il semble avoir des effets plus nocifs que bénéfiques.
Il est utile dans la préparation de médicaments, d'emballages isolants pour l'eau, de bougies à la paraffine, de graisses lubrifiantes, de matériaux pour le moulage de figurines, de cosmétiques, de pommades, de crèmes, parmi de nombreuses autres applications..
Index des articles
- 1 Structure
- 2 Nomenclature
- 3 Propriétés physiques
- 3.1 État physique
- 3.2 Poids moléculaire
- 3.3 Point de fusion
- 3.4 Point d'ébullition
- 3.5 Point d'éclair
- 3.6 Densité
- 3.7 Solubilité
- 3.8 Constante de dissociation
- 4 Propriétés chimiques
- 5 Situation dans la nature
- 5.1 Effet de l'ingestion d'acide stéarique avec des aliments sur la santé humaine
- 6 Obtention
- 7 utilisations
- 7.1 Dans diverses applications
- 7.2 Attraper les moustiques vecteurs de maladies
- 8 Références
Structure
La molécule d'acide stéarique a une chaîne droite de 18 atomes de carbone dans laquelle le dernier atome de carbone fait partie d'un groupe carboxylique -COOH. La chaîne carbonée n'a que des liaisons simples C-C car il s'agit d'un acide gras saturé.
Sa formule élargie est:
CH3-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-CHdeux-COOH
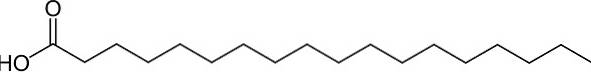
Nomenclature
-Acide stéarique
-Acide octadécanoïque
-Acide stéarique
Propriétés physiques
État physique
Solide cristallin blanc à légèrement jaune avec une légère odeur de sébum.
Poids moléculaire
284,5 g / mol
Point de fusion
69,3 ºC
Point d'ébullition
383 ºC
Point d'inflammation
196 ºC (méthode en vase clos).
Densité
0,9408 g / cm3 à 20 ºC
Solubilité
Insoluble dans l'eau et flotte dessus. Légèrement soluble dans l'alcool. Soluble dans l'éther, l'acétone et le chloroforme.
Constante de dissociation
paquetà = 4,75
Propriétés chimiques
L'acide stéarique réagit avec l'hydroxyde de sodium (NaOH) pour former du stéarate de sodium qui est un savon. La plupart des savons contiennent du stéarate de sodium.
L'acide stéarique et le stéarate de sodium sont considérés comme des composés généralement sûrs et non toxiques..
Emplacement dans la nature
L'acide stéarique est l'un des constituants de nombreuses huiles et graisses d'origine végétale et animale. On le trouve généralement sous la forme de son ester de glycérine.

Il est présent dans de nombreuses graisses solides telles que le suif et dans une moindre mesure dans les graisses semi-solides telles que le saindoux, le beurre et dans les huiles végétales telles que le maïs et le coton..

C'est un composant important du beurre de cacao (38%) et du karité (arbre africain qui produit un type de noix) (38,1%).

Il fait partie du métabolisme de nombreux êtres vivants, tels que les plantes, les mammifères, les humains, les crustacés et les algues. Cela signifie que, par exemple, les humains peuvent le synthétiser dans leur corps.
Effet de l'ingestion d'acide stéarique avec des aliments sur la santé humaine
L'acide stéarique, bien qu'il se produise naturellement dans le corps humain, est également ingéré avec des aliments qui le contiennent à la fois de sa source et ajoutés à sa composition..
Il convient de noter que parmi les aliments transformés industriellement, les graisses ont été abandonnées trans pour être très nocif pour la santé humaine. Ces graisses ont été remplacées par des acides gras saturés, dont l'acide stéarique.
Les effets de cette substitution sont toujours à l'étude. En général, les acides gras saturés à longue chaîne augmentent les taux de cholestérol de basse densité, ce qui est lié à la mortalité par maladie coronarienne et cardiaque.
Cependant, certaines études indiquent que l'acide stéarique réduit le cholestérol de basse densité, ce qui suggère qu'il a des propriétés antiathérogènes, c'est-à-dire qu'il ne provoque pas la formation de plaques dans les artères, mais favorise plutôt la santé des vaisseaux sanguins..
D'autre part, d'autres recherches indiquent qu'il a le potentiel prothrombotique le plus élevé d'acides gras saturés à longue chaîne, cela signifie qu'il peut favoriser les événements de bouchage des vaisseaux sanguins..
De plus, des taux élevés d'acide stéarique dans le sang se sont avérés toxiques pour certaines cellules du pancréas, ce qui peut aggraver les symptômes du diabète de type 2. Cette maladie est fréquente chez les personnes en surpoids..

C'est pour ces raisons que ses effets sont toujours à l'étude car il n'a pas été possible de clarifier si son action est favorable ou non à la santé de l'organisme humain..
Obtention
Il peut être obtenu par hydrolyse du stéarate de glycérine ou de la tristéarine C3H5(COOC17H35)3, selon la réaction chimique suivante:
Triestéarine + hydroxyde de sodium → stéarate de sodium + glycérine
Pour le produire commercialement, on procède à l'hydrogénation d'acides gras insaturés à 18 atomes de carbone, tels que ceux contenus dans les graines de coton et autres légumes..
En d'autres termes, l'hydrogène est ajouté aux doubles liaisons C = C des acides gras insaturés, restant sous forme de liaisons simples C-C, comme suit:
-CH = CH- + Hdeux → -CHdeux-CHdeux-
Applications
Dans diverses applications
L'acide stéarique est un composé chimique commercial important.
Il est utilisé dans l'industrie pharmaceutique pour la fabrication de divers médicaments, tels que des suppositoires, des pilules enrobées pour les affections intestinales ou pour enrober des remèdes amers, entre autres. C'est aussi un ingrédient dans les pommades ou les onguents.
Parce qu'il est insoluble dans l'eau, il est utilisé dans l'industrie alimentaire pour les emballages isolants et dans la préparation de divers types de matériaux imperméables..
Il est également utilisé comme ingrédient dans les gelées, les puddings, les bonbons et les boissons non alcoolisées car il leur confère une certaine viscosité..
Il est utilisé dans la fabrication de bougies en stéarine et est ajouté à la cire de paraffine en petites quantités. En raison de sa texture, il est également utilisé dans les matériaux moulables qui sont utilisés pour fabriquer des modèles tridimensionnels..
Fonctionne également dans les revêtements contre l'électricité statique.
Son sel de sodium est un savon et est également utilisé pour durcir les savons. Parce que c'est un composé inoffensif pour les humains, il est utilisé pour fabriquer des cosmétiques, comme émollient ou comme graisse dans les crèmes. Sert également à ramollir les plastiques.


L'acide stéarique est utilisé pour préparer d'autres composés chimiques tels que certains stéarates métalliques, par exemple l'aluminium, qui est utilisé pour fabriquer des graisses lubrifiantes en épaississant les huiles qui les composent..
De plus, il est un ingrédient de certains pesticides, il est utilisé dans les séchoirs à vernis et comme activateur de vulcanisation pour le caoutchouc synthétique..
Attraper les moustiques porteurs de maladies
L'acide stéarique a été utilisé avec succès dans les pièges à lumière ultraviolette (UV) pour attirer les moustiques transmettant la dengue.
Son odeur caractéristique est similaire à celle de l'acide lactique, qui est celle que l'on trouve sur la peau des êtres humains.Par conséquent, lorsqu'il est placé dans les pièges, il attire les moustiques, qui sont piégés dans l'appareil et meurent..
Les références
- Tvrzicka, E. et al. (2011). Acides gras en tant que biocomposés: leur rôle dans le métabolisme humain, la santé et la maladie - Un examen. Partie 1: Classification, sources alimentaires et fonctions biologiques. Biomed Pap Med Fac Univ Palacky Olomouc République tchèque. 2011 Jun; 155 (2): 117-130. Récupéré de biomed.upol.cz.
- Tseng, W.-H. et coll. (2019). Conception de dispositif de lentille secondaire Freedom avec acide stéarique pour un système de piégeage de moustiques à faible éblouissement avec diodes électroluminescentes ultraviolettes. Electronics 2019, 8, 624. Récupéré de mdpi.com.
- Encyclopédie de chimie de Van Nostrand (2005). Acide stéarique et stéarates. Récupéré de onlinelibrary.wiley.com.
- NOUS. Bibliothèque nationale de médecine. (2019). Acide stéarique. Récupéré de: pubchem.ncbi.nlm.nih.gov.
- Lu, H. et coll. (2016). L'acide stéarique circulant élevé conduit à un effet lipotoxique majeur sur les cellules bêta pancréatiques de souris dans l'hyperlipidémie via une voie PERK / p53 médiée par miR-34a-5p. Diabetologia 2016, 59 (6): 1247-57. Récupéré de ncbi.nlm.nih.gov.


Personne n'a encore commenté ce post.