
Structure de l'acide maléique, propriétés, production, utilisations

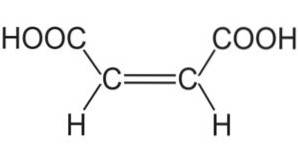
le acide maléique est un composé organique acide dont la formule chimique est HOOC-CH = CH-COOH. C'est un acide dicarboxylique. Il est également connu sous le nom d'acide cis-acide butènedioïque, maléinique, acide malénique et acide toxilique.
L'acide maléique se trouve naturellement dans le tabac, le ginseng et les boissons telles que la bière et le vin. On le trouve également dans la fumée de cigarette et les gaz d'échappement des voitures.
Sa double liaison et les deux groupes -COOH le rendent sensible à diverses réactions chimiques, c'est pourquoi il est utilisé pour synthétiser de nombreux autres composés, matériaux et produits..
Il est également d'une grande aide pour le traitement des textiles tels que le coton, la laine et la soie. Il permet d'obtenir des colles, des résines et des huiles synthétiques. Il est utilisé pour empêcher l'oxydation des graisses et des huiles. À leur tour, bon nombre de ses dérivés sont utilisés dans des applications médicales et vétérinaires..
Selon certaines recherches, c'est l'un des composants des boissons fermentées qui stimule la sécrétion d'acide gastrique.
Index des articles
- 1 Structure
- 2 Nomenclature
- 3 propriétés
- 3.1 État physique
- 3.2 Poids moléculaire
- 3.3 Point de fusion
- 3.4 Point d'ébullition
- 3.5 Poids spécifique
- 3.6 Solubilité
- 3.7 Constantes de dissociation
- 3.8 Propriétés chimiques
- 4 Obtention
- 5 utilisations de l'acide maléique
- 5.1 Dans la production d'autres composés chimiques
- 5.2 Dans diverses applications
- 5.3 Dans l'industrie textile
- 5.4 En médecine
- 5.5 En dentisterie
- 5.6 En médecine vétérinaire
- 5.7 Utilisation potentielle comme désinfectant
- 6 Effets de l'acide maléique contenu dans les boissons fermentées telles que la bière et le vin
- 7 risques
- 8 Références
Structure
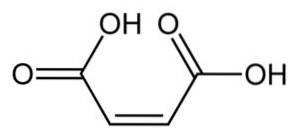
La molécule d'acide maléique est formée d'un squelette de 4 atomes de carbone, dont les deux extrémités forment des groupes carboxyle -COOH et les deux centrales forment une double liaison C = C..
Les groupes -COOH sont situés en position cis en ce qui concerne la double liaison. Les oxygènes et les hydrogènes du -COOH sont logés de telle manière qu'un hydrogène se trouve entre les oxygènes..
Nomenclature
- Acide maléique
- Acide cis-butènedioïque
- Acide toxique
- Acide maléinique
- Acide maléique
Propriétés
État physique
Solide cristallin incolore, cristaux monocliniques.

Poids moléculaire
116,07 g / mol
Point de fusion
130,5 ºC
Point d'ébullition
135 ºC (se décompose)
Poids spécifique
1 609
Solubilité
Très soluble dans l'eau: 79 g / 100 g HdeuxOu à 20 ºC
Constantes de dissociation
K1 = 1 000 x 10-5
Kdeux = 0,055 x 10-5
Propriétés chimiques
L'acide maléique a deux groupes -COOH et une double liaison centrale C = C comme sites réactifs.
Son anhydride est une molécule cyclique de 5 atomes, dont les produits sont instables vis-à-vis de l'hydrolyse, en particulier les produits de réaction avec des groupes amino -NHdeux.
Cela en fait un bloqueur réversible des groupes -NH.deux pour les masquer temporairement et les empêcher de réagir lorsque d'autres réactions se produisent.
Ceci est utile à des fins multiples, en particulier pour modifier les protéines au niveau du laboratoire..
Obtention
Industriellement, il est obtenu par oxydation catalytique du benzène en présence de pentoxyde de vanadium..
Également par oxydation du n-butane ou du n-butylène en phase vapeur avec de l'air, en présence d'un catalyseur solide.
Il peut également être obtenu par hydrolyse de l'anhydride maléique.
Il est également obtenu comme sous-produit lors de la fabrication de l'anhydride phtalique à partir du naphtalène..
Utilisations d'acide maléique
Dans la production d'autres composés chimiques
L'acide maléique permet d'obtenir de nombreux autres composés chimiques. Il est utilisé dans la synthèse des acides aspartique, malique, tartrique, succinique, lactique, malonique, propionique et acrylique.
En tant qu'intermédiaire chimique, l'acide maléique est utilisé dans presque tous les domaines de la chimie industrielle..
Dans diverses applications
L'acide maléique permet d'obtenir des colles synthétiques, des colorants, des résines alkydes et des huiles synthétiques.
Ses dérivés, les sels de maléate, sont utilisés dans des formulations antihistaminiques et des médicaments similaires..
Il est utilisé comme conservateur dans les graisses et les huiles car il sert à retarder l'apparition du rancissement.
Il est utilisé dans les inhibiteurs de corrosion et les produits antisalissures. Il fonctionne également comme un agent pour réguler le pH.
Dans l'industrie textile
Il est utilisé dans le traitement de la laine, de la soie et du coton.
L'obtention d'oligomères (polymères de quelques unités) d'acide maléique a été étudiée pour les utiliser comme agent de finition dans l'obtention de coton pressé permanent, afin de ne pas utiliser de polymères de formaldéhyde.
Dans ce cas, la polymérisation de l'acide maléique est réalisée en milieu aqueux en présence de NaHdeuxPOdeux et un initiateur radical tel que NadeuxSdeuxOU ALORS8. L'oligomère d'acide maléique a des groupes carboxyle -COOH attachés au -CHdeux- parties adjacentes de votre squelette moléculaire.
Il est appliqué sur le tissu de coton comme agent de formation de réseau et le processus de durcissement est effectué.
Ainsi, l'oligomère d'acide maléique est efficace pour réticuler la cellulose de coton et conférer des niveaux élevés de résistance aux plis aux tissus de coton..
De plus, les tissus traités avec des polymères d'acide maléique ne présentaient pas de jaunissement et présentaient une plus grande rétention de résistance ou de résistance que ceux traités avec des polymères de formaldéhyde..

En médecine
Il existe plusieurs composés à base d'acide maléique qui sont utilisés dans le traitement du cancer.
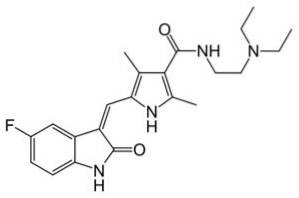
Le maléate de sunitinib (Sutent) est un médicament anticancéreux qui agit de plusieurs manières pour inhiber la prolifération des cellules tumorales et l'angiogenèse..
Il est approuvé pour le traitement du carcinome rénal et des tumeurs gastro-intestinales pharmacorésistantes. Son activité dans le carcinome hépatocellulaire et le cancer des cellules pulmonaires est à l'étude. Fourni par voie orale en gélules.
Selon une étude réalisée en 2015, des nanoparticules ont été préparées avec un copolymère styrène-acide maléique auquel le médicament Paclitaxel utilisé pour le traitement du cancer était lié via une liaison ester..
Ces nanoparticules ont montré une plus grande rétention dans le plasma et dans la tumeur, inhibant la croissance de cette dernière avec une amélioration de l'effet d'apoptose (mort) des cellules cancéreuses..
Ils n'ont pas montré de toxicité dans les principaux organes, tissus et système hématologique.
Pour ces raisons, ils sont proposés comme système alternatif de délivrance ou de délivrance de médicament dans les tumeurs solides.
En dentisterie
Selon certaines recherches, l'acide maléique à 10% réduit la perte de minéraux des dents lorsqu'il est appliqué dans les traitements dentaires.
Il est utilisé pour éroder en douceur la surface de la dent et ainsi favoriser l'adhérence d'autres matériaux.
Il est rapporté qu'il peut produire des forces de liaison ou d'adhérence égales à celles avec 37% d'acide orthophosphorique.
En médecine vétérinaire
Le maléate d'accepromazine est utilisé comme tranquillisant en médecine vétérinaire pour la sédation des animaux avant l'anesthésie. Ce composé protège contre les effets générateurs d'arythmie de l'anesthésie.
Utilisation potentielle comme désinfectant
Il a été récemment découvert (2018) que l'acide maléique pouvait inhiber la résistance des bactéries Listeria monocytogenes aux acides le rendant sensible à l'action de ceux-ci lorsqu'ils sont utilisés pour désinfecter dans les industries alimentaires.
On pense qu'il agit sur une enzyme qui favorise la résistance de ces microorganismes aux acides, en la désactivant. Il a également été démontré que l'acide maléique élimine les biofilms de ces bactéries..
Ces caractéristiques en font un candidat potentiel pour la désinfection des équipements dans l'industrie alimentaire..
Effets de l'acide maléique contenu dans les boissons fermentées telles que la bière et le vin
Des études menées sur des humains qui ont ingéré des solutions de glucose fermenté ont révélé que les acides dicarboxyliques tels que l'acide maléique sont de puissants stimulants de l'acide gastrique..
Selon les chercheurs, cela est très susceptible de se produire dans le cas de boissons fermentées telles que la bière, le champagne et le vin, mais pas dans les boissons alcoolisées distillées telles que le whisky et le cognac..
En effet, l'effet stimulant de l'acide gastrique est causé par les acides dicarboxyliques tels que l'acide maléique et non par l'alcool (éthanol).
Des risques
Le contact de l'acide maléique avec les yeux ou la peau provoque une irritation et peut provoquer une dermatite en cas de contact prolongé. L'inhalation provoque une irritation du nez et de la gorge. Peut avoir un effet néfaste sur les reins.
Lorsqu'il est exposé à la chaleur ou à une flamme, sa combustion se produit et les gaz ou fumées produits provoquent une irritation..
Si de l'acide maléique est libéré, l'environnement devrait être décomposé ou décomposé par des micro-organismes. Ne s'accumule pas dans les organismes aquatiques.
Les références
- NOUS. Bibliothèque nationale de médecine. (2019). Acide maléique. Récupéré de: pubchem.ncbi.nlm.nih.gov.
- Hermanson, G.T. (2013). Objectifs fonctionnels pour la bioconjugaison. In Bioconjugate Techniques (troisième édition). Récupéré de sciencedirect.com.
- Teyssen, S. et coll. (1999). L'acide maléique et l'acide succinique dans les boissons alcoolisées fermentées sont les stimulants de la sécrétion d'acide gastrique. J. Clin. Investir. 1999; 103 (5): 707-713. Récupéré de jci.org.
- Flecknell, P. et coll. (2015). Préanesthésie, anesthésie, analgésie et euthanasie. In Laboratory Animal Medicine (troisième édition). Récupéré de sciencedirect.com.
- Chen, D. et coll. (2005). Polymérisation aqueuse de l'acide maléique et réticulation de la cellulose de coton par poly (acide maléique). Ind. Eng. Chem. Res. 2005, 44, 7921-7927. Récupéré de pubs.acs.org.
- Carver, J.R. (2011). Prise en charge des effets secondaires liés au traitement cardiaque et pulmonaire. En oncologie de soutien. Récupéré de sciencedirect.com.
- SerdarÜsümez, NejatErverdi. (2010). Adhésifs et collage en orthodontie. Dans la thérapie actuelle en orthodontie. Récupéré de sciencedirect.com.
- Dalela, M. et coll. (2015). Nanoparticules biocompatibles sensibles au pH de poly conjugué au paclitaxel (acide styrène-co-maléique) pour l'administration de médicaments anticancéreux dans les tumeurs solides de souris syngéniques. Interfaces ACS Appl Mater. 9 décembre 2015; 7 (48): 26530-48. Récupéré de ncbi.nlm.nih.gov.
- Paudyal, R. et coll. (2018). Une nouvelle approche de la désinfection acide grâce à l'inhibition des mécanismes de résistance aux acides; L'inhibition médiée par l'acide maléique de l'activité de la glutamate décarboxylase augmente la sensibilité à l'acide de Listeria monocytogenes. Nourriture Mycrobiol. 2018 février 69: 96-104. Récupéré de ncbi.nlm.nih.gov.


Personne n'a encore commenté ce post.