
Domaine d'étude et applications de la chimie de l'environnement
La chimie environnementale étudie les processus chimiques qui ont lieu au niveau environnemental. C'est une science qui applique les principes chimiques à l'étude des performances environnementales et des impacts générés par les activités humaines..
De plus, la chimie environnementale conçoit des techniques de prévention, d'atténuation et de remédiation pour les dommages environnementaux existants..
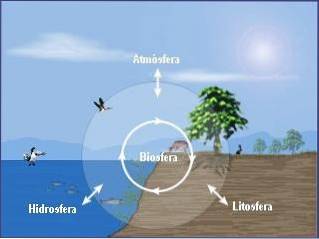
La chimie de l'environnement peut être subdivisée en trois disciplines de base qui sont:
- Chimie environnementale de l'atmosphère.
- Chimie environnementale de l'hydrosphère.
- Chimie environnementale du sol.
Une approche intégrale de la chimie environnementale nécessite en outre l'étude des interrelations entre les processus chimiques qui se produisent dans ces trois compartiments (atmosphère, hydrosphère, sol) et leurs relations avec la biosphère..
Index des articles
- 1 Chimie environnementale de l'atmosphère
- 1.1 -Stratosphère
- 1.2 -Troposphère
- 2 Chimie environnementale de l'hydrosphère
- 2.1 -Eau douce
- 2.2 -Le cycle de l'eau
- 2.3 - Impacts anthropologiques sur le cycle de l'eau
- 3 Chimie environnementale du sol
- 3.1 Le sol
- 3.2 Impacts anthropologiques sur le sol
- 4 Relation chimique-environnement
- 4.1 -Modèle Garrels et Lerman
- 5 Applications de la chimie environnementale
- 6 Références
Chimie environnementale de l'atmosphère
L'atmosphère est la couche de gaz qui entoure la Terre; constitue un système très complexe, où la température, la pression et la composition chimique varient avec l'altitude dans de très larges gammes.
Le soleil bombarde l'atmosphère de radiations et de particules à haute énergie; ce fait a des effets chimiques très importants dans toutes les couches de l'atmosphère, mais en particulier, dans les couches supérieure et externe.
-Stratosphère
Des réactions de photodissociation et de photoionisation se produisent dans les régions extérieures de l'atmosphère. Dans la région entre 30 et 90 km de hauteur mesurée à partir de la surface de la terre, dans la stratosphère, il y a une couche qui contient principalement de l'ozone (O3), appelée couche d'ozone.
Couche d'ozone
L'ozone absorbe le rayonnement ultraviolet à haute énergie qui provient du soleil et sans l'existence de cette couche, aucune forme de vie connue sur la planète ne pourrait survivre..
En 1995, les chimistes atmosphériques Mario J. Molina (mexicain), Frank S. Rowland (américain) et Paul Crutzen (néerlandais), ont remporté le prix Nobel de chimie pour leurs recherches sur la destruction et l'appauvrissement de l'ozone dans la stratosphère..
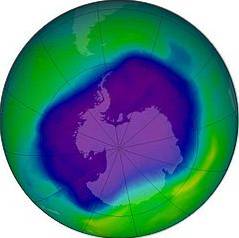
En 1970, Crutzen a montré que les oxydes d'azote détruisent l'ozone par des réactions chimiques catalytiques. Plus tard, Molina et Rowland, en 1974, ont montré que le chlore contenu dans les composés chlorofluorocarbonés (CFC) est également capable de détruire la couche d'ozone..
-Troposphère
La couche atmosphérique immédiate à la surface de la terre, entre 0 et 12 km de haut, appelée troposphère, est composée principalement d'azote (Ndeux) et l'oxygène (Odeux).
Gaz toxiques
En raison des activités humaines, la troposphère contient de nombreux autres produits chimiques considérés comme des polluants atmosphériques tels que:
- Dioxyde et monoxyde de carbone (COdeux et Cie).
- Méthane (CH4).
- Oxyde d'azote (NO).
- Dioxyde de soufre (SOdeux).
- Ozone O3 (considéré comme polluant dans la troposphère)
- Composés organiques volatils (COV), poudres ou particules solides.
Parmi de nombreuses autres substances qui affectent la santé humaine, végétale et animale.
Pluie acide
Oxydes de soufre (SOdeux Et donc3) et ceux de l'azote comme le protoxyde d'azote (NOdeux), causent un autre problème environnemental appelé les pluies acides.
Ces oxydes, présents dans la troposphère principalement sous forme de produits de la combustion de combustibles fossiles dans les activités industrielles et le transport, réagissent avec les eaux de pluie produisant de l'acide sulfurique et de l'acide nitrique, avec les précipitations acides qui en résultent..
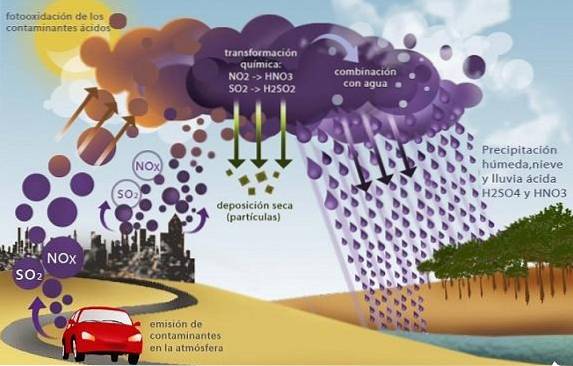
En précipitant cette pluie qui contient des acides forts, elle déclenche plusieurs problèmes environnementaux tels que l'acidification des mers et des eaux douces. Cela provoque la mort des organismes aquatiques; l'acidification des sols qui cause la mort des cultures et la destruction par action chimique corrosive des bâtiments, ponts et monuments.
D'autres problèmes environnementaux atmosphériques sont le smog photochimique, causé principalement par les oxydes d'azote et l'ozone troposphérique.
Réchauffement global
Le réchauffement climatique est produit par de fortes concentrations de COdeux les gaz à effet de serre (GES) atmosphériques et autres, qui absorbent une grande partie du rayonnement infrarouge émis par la surface de la Terre et emprisonnent la chaleur dans la troposphère. Cela génère un changement climatique sur la planète.
Chimie environnementale de l'hydrosphère
L'hydrosphère est constituée de toutes les masses d'eau de la Terre: surface ou zones humides - océans, lacs, rivières, sources - et souterrains ou aquifères..
-Eau fraiche
L'eau est la substance liquide la plus répandue sur la planète, elle couvre 75% de la surface terrestre et est absolument essentielle à la vie..
Toutes les formes de vie dépendent de l'eau douce (définie comme une eau dont la teneur en sel est inférieure à 0,01%). 97% de l'eau de la planète est de l'eau salée.
Sur les 3% d'eau douce restants, 87% se trouvent dans:
- Les pôles de la Terre (qui fondent et se déversent dans les mers en raison du réchauffement climatique).
- Glaciers (également en voie de disparition).
- Eaux souterraines.
- Eau sous forme de vapeur présente dans l'atmosphère.
Seulement 0,4% de l'eau douce totale de la planète est disponible pour la consommation. L'évaporation de l'eau des océans et les précipitations fournissent en permanence ce petit pourcentage..
La chimie environnementale de l'eau étudie les processus chimiques qui interviennent dans le cycle de l'eau ou le cycle hydrologique et développe également des technologies pour la purification de l'eau destinée à la consommation humaine, le traitement des eaux usées industrielles et urbaines, le dessalement de l'eau de mer, le recyclage et la sauvegarde de cette ressource, entre autres.
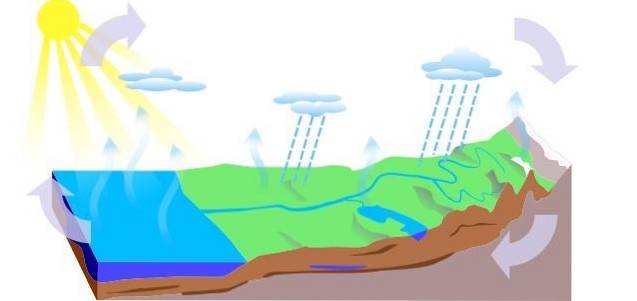
-Le cycle de l'eau
Le cycle de l'eau sur Terre se compose de trois processus principaux: l'évaporation, la condensation et les précipitations, dont trois circuits sont dérivés:
- Ruissellement de surface
- Évapotranspiration végétale
- L'infiltration, dans laquelle l'eau passe aux niveaux souterrains (phréatiques), circule dans les canaux aquifères et sort par des sources, des fontaines ou des puits.
-Impacts anthropologiques sur le cycle de l'eau
L'activité humaine a des impacts sur le cycle de l'eau; certaines des causes et des effets de l'action anthropologique sont les suivantes:
Modification de la surface du sol
Il est généré par la destruction des forêts et des champs avec la déforestation. Cela affecte le cycle de l'eau en éliminant l'évapotranspiration (prise d'eau par les plantes et retour dans l'environnement par transpiration et évaporation) et en augmentant le ruissellement..
L'augmentation du ruissellement de surface produit une augmentation du débit des rivières et des crues.
L'urbanisation modifie également la surface du sol et affecte le cycle de l'eau, car le sol poreux est remplacé par du ciment et de l'asphalte imperméables, ce qui rend l'infiltration impossible..
Pollution du cycle de l'eau
Le cycle de l'eau concerne toute la biosphère et par conséquent, les déchets d'origine humaine sont incorporés à ce cycle par différents processus..
Les polluants chimiques de l'air sont incorporés à la pluie. Les produits agrochimiques appliqués au sol subissent des lixiviats et des infiltrations dans les aquifères ou s'écoulent dans les rivières, les lacs et les mers.
Aussi les déchets de graisses et d'huiles et les lixiviats des décharges sanitaires, sont entraînés par infiltration vers les eaux souterraines.
Extraction des approvisionnements en eau avec découvert sur les ressources en eau
Ces pratiques de découvert entraînent l'épuisement des réserves d'eau souterraine et de surface, affectent les écosystèmes et produisent un affaissement local du sol.
Chimie environnementale du sol
Les sols sont l'un des facteurs les plus importants de l'équilibre de la biosphère. Ils fournissent l'ancrage, l'eau et les nutriments aux plantes, qui sont des producteurs dans les chaînes trophiques terrestres.
Le sol
Le sol peut être défini comme un écosystème complexe et dynamique de trois phases: une phase solide avec support minéral et organique, une phase liquide aqueuse et une phase gazeuse; caractérisé par une faune et une flore particulières (bactéries, champignons, virus, plantes, insectes, nématodes, protozoaires).
Les propriétés du sol sont constamment modifiées par les conditions environnementales et par l'activité biologique qui s'y déroule..
Impacts anthropologiques sur le sol
La dégradation du sol est un processus qui réduit la capacité de production du sol, capable de produire un changement profond et négatif de l'écosystème..
Les facteurs qui produisent la dégradation des sols sont: le climat, la physiographie, la lithologie, la végétation et l'action humaine.

Par l'action humaine peut se produire:
- Dégradation physique du sol (par exemple, compactage dû à des pratiques agricoles et d'élevage inappropriées).
- Dégradation chimique du sol (acidification, alcalinisation, salinisation, contamination par des produits agrochimiques, avec des effluents d'activités industrielles et urbaines, déversements d'hydrocarbures, entre autres).
- Dégradation biologique du sol (diminution de la teneur en matière organique, dégradation du couvert végétal, perte de microorganismes fixateurs d'azote, entre autres).
Relation chimique-environnement
La chimie environnementale étudie les différents processus chimiques qui ont lieu dans les trois compartiments environnementaux: atmosphère, hydrosphère et sol. Il est intéressant de passer en revue une approche supplémentaire sur un modèle chimique simple, qui tente d'expliquer les transferts globaux de matière qui se produisent dans l'environnement..
-Modèle Garrels et Lerman
Garrels et Lerman (1981), ont développé un modèle simplifié de la biogéochimie de la surface de la Terre, qui étudie les interactions entre les compartiments atmosphère, hydrosphère, croûte terrestre et la biosphère incluse..
Le modèle de Garrels et Lerman considère sept minéraux constitutifs majeurs de la planète:
- Gypse (CaSO4)
- Pyrite (FeSdeux)
- Carbonate de calcium (CaCO3)
- Carbonate de magnésium (MgCO3)
- Silicate de magnésium (MgSiO3)
- Oxyde ferrique (FedeuxOU ALORS3)
- Dioxyde de silicium (SiOdeux)
La matière organique constituant la biosphère (vivante et morte), est représentée par CHdeuxOu, qui est la composition stoechiométrique approximative des tissus vivants.
Dans le modèle de Garrels et Lerman, les changements géologiques sont étudiés comme des transferts nets de matière entre ces huit composantes de la planète, par le biais de réactions chimiques et d'un bilan de conservation de masse net..
L'accumulation de COdeux dans l'atmosphère
Par exemple, le problème de l'accumulation de COdeux dans l'atmosphère est étudiée dans ce modèle, en disant que: nous brûlons actuellement le carbone organique stocké dans la biosphère sous forme de charbon, de pétrole et de gaz naturel déposés dans le sous-sol dans le passé géologique.
Conséquence de cette combustion intensive de combustibles fossiles, la concentration de COdeux atmosphérique augmente.
Augmentation des concentrations de COdeux dans l'atmosphère terrestre est due au fait que le taux de combustion du carbone fossile dépasse le taux d'absorption du carbone par les autres composants du système biogéochimique terrestre (comme les organismes photosynthétiques et l'hydrosphère, par exemple).
De cette manière, l'émission de COdeux à l'atmosphère en raison des activités humaines, contourne le système de régulation qui module les changements sur Terre.
La taille de la biosphère
Le modèle développé par Garrels et Lerman considère également que la taille de la biosphère augmente et diminue en raison de l'équilibre entre la photosynthèse et la respiration..
Au cours de l'histoire de la vie sur Terre, la masse de la biosphère a augmenté par étapes avec des taux élevés de photosynthèse. Cela s'est traduit par un stockage net de carbone organique et des émissions d'oxygène:
COdeux + HdeuxO → CHdeuxO + Odeux
La respiration, en tant qu'activité métabolique des micro-organismes et des animaux supérieurs, convertit le carbone organique en dioxyde de carbone (COdeux) et de l'eau (HdeuxO), c'est-à-dire qu'il inverse la réaction chimique précédente.
La présence d'eau, le stockage du carbone organique et la production d'oxygène moléculaire sont fondamentaux pour l'existence de la vie..
Applications de chimie environnementale
La chimie environnementale propose des solutions pour la prévention, l'atténuation et la réparation des dommages environnementaux causés par l'activité humaine. Parmi certaines de ces solutions, on peut citer:
- La conception de nouveaux matériaux appelés MOF (pour son acronyme en anglais: Cadres organiques métalliques). Ceux-ci sont très poreux et ont la capacité de: absorber et retenir le COdeux, obtenir HdeuxOu de la vapeur d'air du désert et stocker Hdeux dans de petits contenants.
- La conversion des déchets en matières premières. Par exemple, l'utilisation de pneus usés dans la production de gazon artificiel ou de semelles de chaussures. Aussi l'utilisation des déchets de taille des cultures, dans la production de biogaz ou de bioéthanol.
- Synthèses chimiques de substituts CFC.
- Le développement d'énergies alternatives, telles que les cellules à hydrogène, pour la production d'électricité non polluante.
- Contrôle de la pollution atmosphérique, avec des filtres inertes et des filtres réactifs.
- Dessalement de l'eau de mer par osmose inverse.
- Le développement de nouveaux matériaux pour la floculation de substances colloïdales en suspension dans l'eau (procédé d'épuration).
- Le renversement de l'eutrophisation des lacs.
- Le développement de la «chimie verte», une tendance qui propose la substitution de composés chimiques toxiques par des composés moins toxiques et des procédés chimiques «respectueux de l'environnement». Par exemple, il est appliqué dans l'utilisation de solvants et de matières premières moins toxiques, dans l'industrie, dans le nettoyage à sec de blanchisseries, entre autres..
Les références
- Calvert, J. G., Lazrus, A., Kok, G. L., Heikes, B. G., Walega, J. G., Lind, J., et Cantrell, C. A. (1985). Mécanismes chimiques de génération d'acide dans la troposphère. Nature, 317 (6032), 27-35. doi: 10.1038 / 317027a0.
- Crutzen, P.J. (1970). L'influence des oxydes d'azote sur le contenu atmosphérique. Q.J.R. Métheorol. Soc Wiley-Blackwell. 96: 320-325.
- Garrels, R.M. et Lerman, A. (1981). Cycles phanérozoïques du carbone sédimentaire et du soufre. Actes de l'Académie des sciences naturelles. LES USAGES. 78: 4 652 à 4 656.
- Hester, R. E. et Harrison, R. M. (2002). Changement environnemental global. Société royale de chimie. pp 205.
- Hites, R. A. (2007). Éléments de chimie environnementale. Wiley-Interscience. pp 215.
- Manahan, S. E. (2000). Chimie environnementale. Septième édition. CRC. pp 876
- Molina, M.J. et Rowland, F.S. (1974). Puits stratosphérique pour les chlorofluorométhanes: destruction de l'ozone catalysée par des atomes de chlore. Nature. 249: 810-812.
- Morel, F.M. et Hering, J.M. (2000). Principes et applications de la chimie aquatique. New York: John Wiley.
- Stockwell, W. R., Lawson, C. V., Saunders, E., et Goliff, W. S. (2011). Un examen de la chimie atmosphérique troposphérique et des mécanismes chimiques en phase gazeuse pour la modélisation de la qualité de l'air. Atmosphère, 3 (1), 1-32. doi: 10.3390 / atmos3010001



Personne n'a encore commenté ce post.