
Caractéristiques du glutathion, structure, fonctions, biosynthèse
le glutathion (GSH) est une petite molécule de tripeptide (avec seulement trois résidus d'acides aminés) non protéique qui participe à de nombreux phénomènes biologiques tels que la mécanique enzymatique, la biosynthèse des macromolécules, le métabolisme intermédiaire, la toxicité de l'oxygène, le transport intracellulaire, etc..
Ce petit peptide, présent chez les animaux, les plantes et certaines bactéries, est considéré comme un "amortir" oxydo-réducteur, car c'est l'un des principaux composés de bas poids moléculaire qui contient du soufre et n'a pas la toxicité associée aux résidus de cystéine.
Certaines maladies chez l'homme ont été associées à une carence en enzymes spécifiques du métabolisme du glutathion, et cela est dû à ses multiples fonctions dans le maintien de l'homéostasie corporelle..
La malnutrition, le stress oxydatif et d'autres pathologies subies par l'homme peuvent être mis en évidence par une diminution drastique du glutathion, c'est pourquoi il est parfois un bon indicateur de l'état de santé des systèmes corporels..
Pour les plantes, de la même manière, le glutathion est un facteur essentiel de leur croissance et de leur développement, car il remplit également des fonctions dans de multiples voies de biosynthèse et est essentiel pour la détoxification cellulaire et l'homéostasie interne, où il agit comme un puissant antioxydant..
Index des articles
- 1 Fonctionnalités
- 2 Structure
- 3 fonctions
- 3.1 Coenzyme
- 3.2 Stockage de la cystéine
- 3.3 Pliage des protéines
- 3.4 Fonction dans les érythrocytes
- 3.5 Métabolisme xénobiotique
- 3.6 État oxydatif des cellules
- 4 Biosynthèse
- 4.1 Glutathion réduit (GSH)
- 4.2 Glutathion oxydé (GSSG)
- 5 avantages de son apport
- 5.1 Cancer
- 5.2 VIH
- 5.3 Activité musculaire
- 5.4 Pathologies hépatiques
- 5.5 Antioxydant
- 5.6 "Absorption"
- 6 effets secondaires
- 7 Références
Caractéristiques
Les premières études menées en relation avec la localisation subcellulaire du glutathion ont montré qu'il est présent dans les mitochondries. Plus tard, il a également été observé dans la région correspondant à la matrice nucléaire et dans les peroxysomes.
Actuellement, on sait que le compartiment où sa concentration est la plus abondante est dans le cytosol, car il y est activement produit et transporté vers d'autres compartiments cellulaires tels que les mitochondries..
Dans les cellules de mammifères, la concentration de glutathion est de l'ordre du millimole, tandis que dans le plasma sanguin, sa forme réduite (GSH) se trouve à des concentrations micromolaires..
Cette concentration intracellulaire ressemble étroitement à la concentration de glucose, de potassium et de cholestérol, éléments essentiels pour la structure cellulaire, la fonction et le métabolisme..
Certains organismes ont des molécules de glutathion analogues ou variantes. Les parasites protozoaires qui affectent les mammifères ont une forme connue sous le nom de «trypanothion» et dans certaines bactéries, ce composé est remplacé par d'autres molécules de soufre telles que le thiosulfate et la glutamylcystéine..
Certaines espèces végétales possèdent, en plus du glutathion, des molécules homologues qui ont des résidus autres que la glycine à l'extrémité C-terminale (homoglutathion), et qui se caractérisent par des fonctions similaires à celles du tripeptide en question..
Malgré l'existence d'autres composés similaires au glutathion dans différents organismes, c'est l'un des "thiols" trouvés à la concentration intracellulaire la plus élevée..
Le rapport élevé qui existe normalement entre la forme réduite (GSH) et la forme oxydée (GSSG) du glutathion est une autre caractéristique distinctive de cette molécule..
Structure
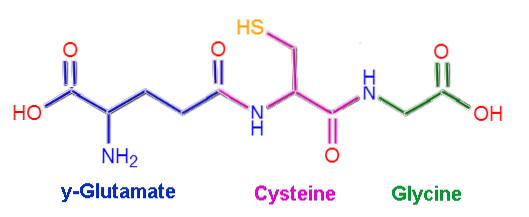
Le glutathion ou L-γ-glutamyl-L-cystéinyl-glycine, comme son nom l'indique, est composé de trois résidus d'acides aminés: le L-glutamate, la L-cystéine et la glycine. Les résidus cystéine et glycine sont liés ensemble par des liaisons peptidiques communes, c'est-à-dire entre le groupe α-carboxyle d'un acide aminé et le groupe α-amino de l'autre..
Cependant, la liaison qui se produit entre le glutamate et la cystéine n'est pas typique des protéines, car elle se produit entre la partie γ-carboxyle du groupe R du glutamate et le groupe α-amino de la cystéine.est appelée liaison γ.
Cette petite molécule a une masse molaire d'un peu plus de 300 g / mol et la présence de la liaison y apparaît cruciale pour l'immunité de ce peptide contre l'action de nombreuses enzymes aminopeptidases..
Caractéristiques
Comme mentionné, le glutathion est une protéine qui participe à de nombreux processus cellulaires chez les animaux, les plantes et certains procaryotes. En ce sens, sa participation générale à:
-Les processus de synthèse et de dégradation des protéines
-La formation de précurseurs de ribonucléotides d'ADN
-Régulation de l'activité de certaines enzymes
-Protection des cellules en présence d'espèces réactives de l'oxygène (ROS) et d'autres radicaux libres
-Transduction du signal
-Expression génétique et en
-Apoptose ou mort cellulaire programmée
Coenzyme
Il a également été déterminé que le glutathion fonctionnait comme coenzyme dans de nombreuses réactions enzymatiques, et qu'une partie de son importance est liée à sa capacité à transporter des acides aminés sous forme d'acides aminés γ-glutamyl par voie intracellulaire..
Le glutathion qui peut quitter la cellule (ce qu'il fait sous sa forme réduite) est capable de participer à des réactions d'oxydoréduction au voisinage de la membrane plasmique et de l'environnement cellulaire environnant, ce qui protège les cellules des dommages contre différentes classes d'agents oxydants.
Stockage de la cystéine
Ce tripeptide fonctionne également comme source de stockage de la cystéine et contribue au maintien de l'état réduit des groupements sulfhydryle des protéines à l'intérieur de la cellule et de l'état ferreux du groupement hème des protéines contenant ledit cofacteur..
Repliement des protéines
Lorsqu'il participe au repliement des protéines, il semble avoir une fonction importante en tant qu'agent réducteur des ponts disulfure qui se sont formés de manière inappropriée dans les structures protéiques, ce qui est généralement dû à une exposition à des agents oxydants tels que l'oxygène, le peroxyde d'hydrogène, le peroxynitrite et certains superoxydes..
Fonction érythrocytaire
Dans les érythrocytes, le glutathion réduit (GSH) produit par l'enzyme glutathion réductase, qui utilise le NADPH produit par la voie du pentose phosphate, contribue à l'élimination du peroxyde d'hydrogène par la réaction catalysée par une autre enzyme: la glutathion peroxydase, qui produit de l'eau et du glutathion oxydé. (GSSG).
La dégradation du peroxyde d'hydrogène et, par conséquent, la prévention de son accumulation dans les érythrocytes, prolonge la durée de vie de ces cellules, car elle évite les dommages oxydatifs qui peuvent survenir dans la membrane cellulaire et qui peuvent aboutir à une hémolyse..
Métabolisme xénobiotique
Le glutathion est également un acteur important dans le métabolisme des xénobiotiques, grâce à l'action des enzymes glutathion S-transférase qui génèrent des conjugués de glutathion qui peuvent ensuite être métabolisés intracellulairement..
Il est prudent de se rappeler que le terme «xénobiotique» est utilisé pour désigner les médicaments, les polluants environnementaux et les cancérogènes chimiques auxquels un organisme est exposé..
État oxydatif des cellules
Puisque le glutathion existe sous deux formes, l'une réduite et l'autre oxydée, la relation entre les deux molécules détermine l'état redox des cellules. Si le rapport GSH / GSSG est supérieur à 100, les cellules sont considérées comme saines, mais s'il est proche de 1 ou 10, cela peut être un indicateur que les cellules sont en état de stress oxydatif.
Biosynthèse
Le tripeptide glutathion est synthétisé à l'intérieur des cellules, tant chez les plantes que chez les animaux, par l'action de deux enzymes: (1) la γ-glutamylcystéine synthétase et (2) la glutathion synthétase (GSH synthétase), tandis que sa dégradation ou «décomposition» dépend de l'action de l'enzyme γ-glutamyl transpeptidase.
Dans les organismes végétaux, chacune des enzymes est codée par un seul gène et des défauts dans l'une des protéines ou leurs gènes codants peuvent entraîner la létalité chez les embryons.
Chez l'homme, comme chez d'autres mammifères, le site principal de synthèse et d'exportation du glutathion est le foie, en particulier dans les cellules hépatiques (hépatocytes) qui entourent les canaux veineux qui transportent le sang et d'autres substances vers et depuis l'organe en question..
La synthèse de novo le glutathion, sa régénération ou son recyclage, nécessitent l'énergie de l'ATP pour se produire.
Glutathion réduit (GSH)
Le glutathion réduit est dérivé des acides aminés glycine, glutamate et cystéine, comme déjà mentionné, et sa synthèse commence par l'activation (en utilisant l'ATP) du groupe γ-carboxyle du glutamate (du groupe R) pour former un acyl phosphate intermédiaire, qui est attaqué par le groupe α-amino de la cystéine.
Cette première réaction de condensation de deux acides aminés est catalysée par la y-glutamylcystéine synthétase et est généralement affectée par la disponibilité intracellulaire des acides aminés glutamate et cystéine..
Le dipeptide ainsi formé est ensuite condensé avec une molécule de glycine grâce à l'action de la GSH synthétase. Au cours de cette réaction, une activation par l'ATP du groupement α-carboxyle de la cystéine se produit également pour former un acylphosphate et ainsi favoriser la réaction avec le résidu glycine..
Glutathion oxydé (GSSG)
Lorsque le glutathion réduit participe aux réactions d'oxydoréduction, la forme oxydée est en fait constituée de deux molécules de glutathion liées entre elles par des ponts disulfure; c'est pour cette raison que la forme oxydée est abrégée par les initiales "GSSG".
La formation des espèces oxydées de glutathion dépend d'une enzyme connue sous le nom de glutathion peroxydase ou GSH peroxydase, qui est une peroxydase qui contient une sélénocystéine (un résidu cystéine qui au lieu d'avoir un atome de soufre a un atome de sélénium) en place . actif.
L'interconversion entre les formes oxydée et réduite se produit grâce à la participation d'une GSSG réductase ou glutathion réductase, qui utilise le NAPDH pour catalyser la réduction du GSSG en présence d'oxygène, avec la formation concomitante de peroxyde d'hydrogène.
Avantages de son apport
Le glutathion peut être administré par voie orale, topique, intraveineuse, intranasale ou nébulisée, afin d'augmenter sa concentration systémique chez les patients souffrant de stress oxydatif, par exemple.
Cancer
Les recherches sur l'administration orale de glutathion suggèrent que son apport peut réduire les risques de cancer de la bouche et que, lorsqu'il est administré en conjonction avec une chimiothérapie oxydative, il réduit les effets négatifs de la thérapie chez les patients cancéreux..
VIH
En règle générale, les patients infectés par le virus de l'immunodéficience acquise (VIH) présentent des carences intracellulaires en glutathion à la fois dans les globules rouges et les lymphocytes T et les monocytes, ce qui détermine leur bon fonctionnement..
Dans une étude de Morris et al., Il a été montré que la fourniture de glutathion aux macrophages de patients séropositifs améliorait considérablement la fonction de ces cellules, en particulier contre les infections par des agents pathogènes opportunistes tels que M. tuberculosis.
Activité musculaire
D'autres études portent sur l'amélioration de l'activité contractile musculaire, la défense antioxydante et les dommages oxydatifs causés en réponse à des lésions d'ischémie / reperfusion après administration orale de GSH pendant un entraînement en résistance physique..
Pathologies hépatiques
Il a été considéré, à son tour, que son ingestion ou son administration intraveineuse avait des fonctions dans la prévention de la progression de certains types de cancer et dans la réduction des dommages cellulaires résultant de certaines pathologies hépatiques..
Antioxydant
Bien que toutes les études rapportées n'aient pas été réalisées chez des patients humains, mais soient généralement des tests sur des modèles animaux (généralement murins), les résultats obtenus dans certains essais cliniques confirment l'efficacité du glutathion exogène en tant qu'antioxydant..
Pour cette raison, il est utilisé pour le traitement de la cataracte et du glaucome, comme produit «anti-âge», pour le traitement de l'hépatite, de nombreuses maladies cardiaques, de la perte de mémoire et pour renforcer le système immunitaire, et pour la clairance après les métaux lourds et intoxication médicamenteuse.
"Absorption"
Le glutathion administré de manière exogène ne peut pénétrer dans les cellules que s'il est hydrolysé en ses acides aminés constitutifs. Par conséquent, l'effet direct de l'administration (orale ou intraveineuse) de ce composé est l'augmentation de la concentration intracellulaire de GSH grâce à l'apport des acides aminés nécessaires à sa synthèse, qui peuvent être efficacement transportés vers le cytosol.
Effets secondaires
Bien que l'apport de glutathion soit considéré comme «sûr» ou inoffensif, peu d'études ont été effectuées sur ses effets secondaires..
Cependant, d'après les quelques études rapportées, on sait qu'il peut avoir des effets négatifs résultant de l'interaction avec d'autres médicaments et qui peuvent être nocifs pour la santé dans divers contextes physiologiques..
S'ils sont pris à long terme, il semble qu'ils agissent pour diminuer excessivement les niveaux de zinc et, de plus, s'ils sont inhalés, ils peuvent produire de graves crises d'asthme chez les patients asthmatiques..
Les références
- Allen, J., et Bradley, R. (2011). Effets de la supplémentation orale en glutathion sur les biomarqueurs de stress oxydatif systémique chez les volontaires humains. Le Journal of Alternative and Complementary Medicine, 17(9), 827-833.
- Conklin, K. A. (2009). Antioxydants alimentaires pendant la chimiothérapie anticancéreuse: impact sur l'efficacité de la chimiothérapie et sur le développement d'effets secondaires. Nutrition et cancer, 37(1), 1-18.
- Meister, A. (1988). Métabolisme du glutathion et sa modification sélective. Le journal de chimie biologique, 263(33), 17205-17208.
- Meister, A. et Anderson, M. E. (1983). Glutathion. Ann. Rev Biochem., 52, 711-760.
- Morris, D., Guerra, C., Khurasany, M., Guilford, F., et Saviola, B. (2013). La supplémentation en glutathion améliore les fonctions des macrophages dans le VIH. Journal of Interferon & Cytokine Research, Onze.
- Murray, R., Bender, D., Botham, K., Kennelly, P., Rodwell, V. et Weil, P. (2009). La biochimie illustrée de Harper (28e éd.). McGraw-Hill Médical.
- Nelson, D. L. et Cox, M. M. (2009). Principes de biochimie de Lehninger. Éditions Omega (5e éd.). https://doi.org/10.1007/s13398-014-0173-7.2
- Noctor, G., Mhamdi, A., Chaouch, S., Han, Y. I., Neukermans, J., Marquez-garcia, B.,… Foyer, C. H. (2012). Glutathion dans les plantes: un aperçu intégré. Plante, cellule et environnement, 35, 454-484.
- Pizzorno, J. (2014). Glutathion! Médecine d'investigation, 13(1), 8-12.
- Qanungo, S., Starke, D. W., Pai, H. V, Mieyal, J. J., et Nieminen, A. (2007). La supplémentation en glutathion potentialise l'apoptose hypoxique par S-glutathionylation de p65-NFkB. Le journal de chimie biologique, 282(25), 18427-18436.
- Ramires, P. R. et Ji, L. L. (2001). La supplémentation en glutathion et l'entraînement augmentent la résistance du myocarde à l'ischémie-reperfusion in vivo. Ann. J. Physiol. Heart Circ. Physiol., 281, 679-688.
- Sies, H. (2000). Le glutathion et son rôle dans les fonctions cellulaires. Biologie et médecine radicales gratuites R, 27(99), 916-921.
- Wu, G., Fang, Y., Yang, S., Lupton, J. R. et Turner, N. D. (2004). Métabolisme du glutathion et ses implications pour la santé. Société américaine pour les sciences de la nutrition, 489-492.



Personne n'a encore commenté ce post.