
Cary Blair Medium Justification, préparation et utilisations
le moitié Cary Blair est une gélose semi-solide, utilisée pour le transport et la conservation d'échantillons biologiques qui hébergent des agents pathogènes intestinaux, des microorganismes labiles et anaérobies. Comme tout moyen de transport, sa fonction est de conserver l'échantillon dans des conditions optimales jusqu'à sa culture. Les microorganismes pathogènes présents, ainsi que le microbiote qui l'accompagne, doivent rester viables, mais sans augmenter leur population..
Cary Blair Medium est le résultat du changement de formulation du Stuart Transport Medium. La modification a été effectuée en 1964 et a consisté à remplacer le système de régulation du pH (glycérophosphate) par un tampon phosphate inorganique..
La reformulation était nécessaire car ses créateurs se sont rendu compte que le glycérophosphate au bout d'un certain temps pouvait être métabolisé par certaines bactéries saprophytes. Ceux-ci se multiplient chevauchent les agents pathogènes présents.
D'autres changements ont été l'élimination du bleu de méthylène, ainsi qu'un réajustement du pH vers l'alcalinité (pH 8,4). Tous ces changements ont amélioré l'efficacité des moyens de transport.
À l'origine, le milieu Cary Blair était utilisé pour le maintien des agents pathogènes intestinaux, tels que Shigella flexneri, Salmonella sp, Vibrio cholerae et Campylobacter sp.
Cependant, plus tard, l'efficacité de la préservation de la viabilité de micro-organismes pathogènes exigeants et labiles a été constatée, tels que: Neisseria gonorrhoeae, Haemophilus influenzae, Neisseria meningitidis, Bordetella pertussis, Streptococcus pneumoniae et quelques anaérobies.
Index des articles
- 1 Justification
- 2 Préparation
- 3 Utilisation
- 3.1 Type d'échantillons
- 3.2 Prélèvement d'échantillons
- 3.3 Identification de l'échantillon
- 3.4 Transfert
- 4 Enquêtes menées sur les moyens de transport Cary Blair
- 5 Contrôle de la qualité
- 6 Références
Base
Le milieu Cary Blair contient du chlorure de sodium, du thioglycolate de sodium, du phosphate disodique, du chlorure de calcium et de la gélose.
Le chlorure de sodium maintient l'équilibre osmotique du milieu, le phosphate disodique et le chlorure de calcium équilibrent le pH. De son côté, le thioglycollate de sodium maintient un faible potentiel d'oxydoréduction, tandis que la petite portion d'agar donne la consistance semi-solide..
Le milieu Cary Blair ne contient pas de substances nutritives, car la fonction d'un milieu de transport est de maintenir l'échantillon sans qu'il subisse des changements en termes d'humidité et de charge microbienne; c'est-à-dire qu'il évite la déshydratation de l'échantillon tout en préservant la viabilité et la quantité des microorganismes présents.
Enfin, le pH légèrement alcalin évite la mort des microorganismes par acidité, en particulier les Vibrios sont très sensibles aux acides.
préparation
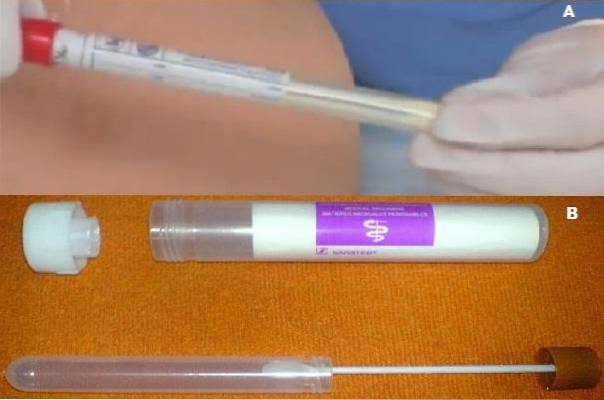
Le média Cary Blair est disponible dans le commerce sous forme de dispositif spécial prêt à l'emploi. Le système de transport est couvert par un sac Peel Pack en plastique. À l'intérieur, il contient un écouvillon pour recueillir l'échantillon et le tube contenant le milieu semi-solide de Cary Blair..
Il existe également sur le marché des maisons commerciales qui fournissent le milieu déshydraté pour sa préparation en laboratoire..
Pour ce faire, pesez 13,2 g de milieu déshydraté et dissolvez-le dans un litre d'eau distillée. Chauffer et agiter la préparation jusqu'à dissolution complète. Répartir le milieu dans des tubes à essai à bouchon à vis (bakélite).
Cuire les tubes à la vapeur pendant 15 minutes. Laisser refroidir et conserver à température ambiante jusqu'à utilisation.
Le milieu Cary Blair non ensemencé peut être conservé de manière optimale jusqu'à 18 mois à température ambiante.
Le pH du milieu doit être ajusté à 8,4 ± 0,2. La couleur du milieu préparé est beige, avec une certaine opalescence.
Utiliser
Type d'échantillons
Cary Blair Medium est utilisé lorsque les échantillons de selles, d'écouvillon rectal et d'écouvillon vaginal ne peuvent pas être traités immédiatement.
Lorsqu'aucun moyen de transport n'est disponible, les échantillons peuvent être conservés à -70 ° C.
Prise d'échantillon
L'écouvillon est imprégné de l'échantillon et il est introduit dans le milieu Cary Blair, sans atteindre le fond.
Identification des échantillons
Le milieu Cary Blair doit porter une étiquette sur laquelle sont placées les données de base, telles que: prénom et nom du patient, numéro d'identification de l'échantillon, source du prélèvement, médecin traitant, date et heure du prélèvement. , diagnostic présomptif, traitement antibiotique.
Transfert
Bien couvert et transporté à température ambiante pour les échantillons fécaux. Alors que, pour les échantillons vaginaux à la recherche de microorganismes anaérobies, il est recommandé de transporter les échantillons à 4 ° C.
Dans tous les cas, le temps de transfert recommandé est de 4 à 6 heures, avec un maximum de 24 heures..
Si la présence de Campylobacter jejuni dans des échantillons de selles et ceux-ci ne peuvent pas être traités dans les 24 heures, le stockage en milieu Cary Blair à 4 ° C est recommandé.
Recherches menées sur le moyen de transport Cary Blair
Plusieurs études ont montré que le milieu Cary Blair peut rester viable pour les microorganismes entéropathogènes du genre Shigella et Salmonella jusqu'à 49 jours après le prélèvement de l'échantillon..
Pour sa part, Vibrio cholerae, un autre pathogène intestinal important, est capable de survivre pendant 22 jours, tandis que Yersinia pestis (agent causal de la peste bubonique et pneumonique) peut être récupéré après 75 jours.
Cependant, malgré la durabilité démontrée en termes de récupération de ces microorganismes, il est recommandé que les échantillons prélevés soient transportés dans le milieu Cary Blair vers le laboratoire le plus rapidement possible..
De même, une fois que l'échantillon atteint le laboratoire, il doit être semé sans délai dans les milieux de culture respectifs..
D'autre part, le milieu Cary Blair, en plus d'être utile pour le transport de microorganismes facultatifs, est également recommandé pour les échantillons contenant des pathogènes anaérobies..
En ce sens, DeMarco et ses collaborateurs ont réalisé en 2017 une étude intitulée: Survie des micro-organismes vaginaux dans trois systèmes de transport disponibles dans le commerce.
Ils ont démontré que le milieu de transport Cary Blair est le meilleur moyen de transport pour la conservation et la récupération des micro-organismes anaérobies vaginaux. De même, ils ont montré que le taux de récupération le plus élevé était atteint lorsque la température de transfert était de 4 ° C..
Par conséquent, il est conclu que la température de transport des écouvillons vaginaux (micro-organismes anaérobies) doit être de 4 ° C. Alors que pour les échantillons fécaux à la recherche de micro-organismes facultatifs, la température idéale est la température ambiante..
Contrôle de qualité
Souches appelées Shigella sonnei ATCC 11060, Salmonella choleraesuis ATCC 14028, Vibrio cholerae Oui Campylobacter sp.
Le milieu est ensemencé avec la souche choisie et conservé à température ambiante pendant 24 heures. Ils sont ensuite semés dans les milieux de culture correspondants. Dans tous les cas, une récupération satisfaisante du microorganisme en question est attendue..
Les références
- DeMarco AL, Rabe LK, Austin MN, et al. Survie des micro-organismes vaginaux dans trois systèmes de transport disponibles dans le commerce. Anaérobe. 2017; 45: 44-49.
- Wasfy M, Oyofo B, Elgindy A, Churilla A. Comparaison des milieux de conservation pour le stockage des échantillons de selles. J Clin Microbiol. Année mille neuf cents quatre-vingts-quinze; 33 (8): 2176-2178.
- Dan M, Richardson J, Miliotis MD, Koornhof HJ. Comparaison des milieux de conservation et des conditions de congélation pour le stockage des échantillons de matières fécales. J Med Microbiol. 1989; 28 (2): 151-4.
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Diagnostic microbiologique. 5e éd. Éditorial Panamericana S.A. Argentine.
- Forbes B, Sahm D, Weissfeld A. (2009). Diagnostic microbiologique Bailey & Scott. 12 éd. Éditorial Panamericana S.A. Argentine.
- Laboratoires Conda Pronadisa. La moitié de Cary Blair. Disponible sur: condalab.com
- Laboratoire Metrix. Cary Blair. Disponible sur: metrixlab.mx



Personne n'a encore commenté ce post.