
Réactif de Benoît à quoi il sert, composants, préparation
le Réactif de Benoît est une solution bleuâtre de cuivre utilisée pour détecter la présence de sucres réducteurs: aldéhydes, alpha-hydroxy-cétones et hémicétals. Il a été développé par Stanley R. Benedict (1884-1936).
Les sucres alpha-hydroxy-cétones sont caractérisés en ce qu'ils ont un groupe hydroxyle au voisinage de la cétone. Pendant ce temps, un hémicétal est un composé qui résulte de l'ajout d'un alcool à un aldéhyde ou une cétone. Le réactif de Benedict réagit sans discernement avec tous ces sucres réducteurs.
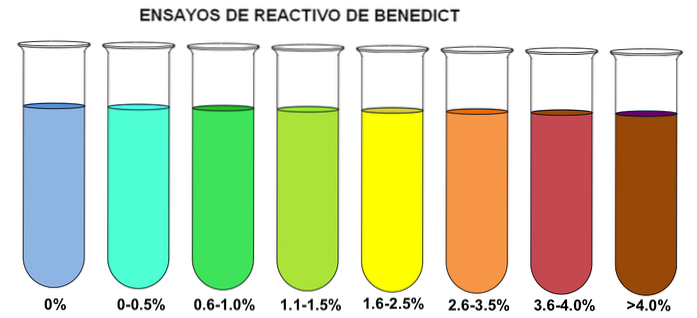
La méthode de Benoît est basée sur l'action réductrice des sucres sur Cudeux+, de coloration bleue, qui le transforme en Cu+. Le CU+ forme un précipité rouge brique d'oxyde cuivreux. Cependant, en fonction de la concentration de sucres, un spectre de couleurs apparaît (image du haut).
A noter que si le réactif de Benedict est ajouté dans un tube à essai sans réduire les sucres (0%), il ne subit aucun changement de sa couleur bleutée. Ainsi, lorsque la concentration est supérieure à 4%, le tube à essai est taché de brun..
Index des articles
- 1 Histoire
- 2 À quoi sert le réactif de Benedict?
- 2.1 Détection du glucose dans l'urine
- 2.2 Coloration de la solution
- 2.3 Détection de divers monosaccharides et disaccharides
- 3 composants
- 4 Procédure d'utilisation
- 5 Réaction au test de Benoît
- 6 Préparation du réactif de Benoît
- 7 Références
Histoire
Le réactif a été créé par le chimiste américain Stanley Rossiter Benedict en 1909, qui a publié son article scientifique Un réactif pour la détection des sucres réducteurs, dans la revue J. Biol. Chem.
En outre, Lewis et Benedict (1915) ont publié une méthode pour la détermination des sucres réducteurs dans le sang, en utilisant le picrate comme indicateur; mais a cessé d'être utilisé en raison d'un manque de spécificité.
Le réactif de Benedict est très similaire à celui de Fehling. Ils diffèrent en ce que Benedict utilise l'ion citrate et le sel de carbonate de sodium; tandis que Fehling utilise l'ion tartrate et l'hydroxyde de sodium.
Le test Benedict est qualitatif, c'est-à-dire qu'il ne détecte que la présence de sucres réducteurs. Cependant, le réactif de Benedict peut être quantitatif s'il contient du thiocyanate de potassium en solution, qui forme un précipité blanc de thiocyanate de cuivre qui peut être titré à l'aide d'étalons de glucose..
À quoi sert le réactif de Benedict?
Détection du glucose dans l'urine
Le réactif Benedict est toujours utilisé pour détecter la présence de glucose dans l'urine et est une indication de diabète chez le patient, dont l'urine est soumise au test ou test Benedict. Cependant, il ne peut être exclu que la glucosurie ait une origine différente.
Par exemple, une glycosurie accrue se trouve dans des conditions telles que: la grossesse, la glycosurie rénale primaire, l'acidose tubulaire rénale, le syndrome de Fanconi primaire ou secondaire, l'hyperaldostéronisme et la pancréatite aiguë ou le cancer du pancréas..
Le réactif de Benoît est bleu en raison de la présence de Cudeux+, qui est réduit en Cu+ par l'action de réduire les sucres; dans ce cas, glucose, formant un précipité d'oxyde de cuivre (I) rouge brique.
Coloration en solution
La coloration et la formation du précipité dans le test Benedict appliqué à l'urine varient en fonction de la concentration du sucre réducteur. Si la concentration de glucose dans l'urine est inférieure à 500 mg / dL, la solution devient verte et il n'y a pas de formation de précipité.
Une concentration de glucose urinaire de 500 à 1 000 mg / dL provoque un précipité vert dans le test Benedict. À une concentration supérieure à 1000 à 1500 mg / dL, il provoque la formation d'un précipité jaune.
Si la concentration de glucose est de 1 500 à 2 000 mg / dL, un précipité orange apparaîtra. Enfin, une concentration de glucose dans l'urine est supérieure à 2 000 mg / dL, elle provoquera la formation d'un précipité rouge brique..
Cela indique que le test Benedict a un caractère semi-quantitatif et que le résultat est rapporté à l'aide de croisements. Ainsi, par exemple, la formation d'un précipité vert correspond à une croix (+); et la formation d'un précipité rouge brique, correspond à quatre croix (++++).
Détection de divers monosaccharides et disaccharides
Le réactif de Benedict détecte la présence de sucres réducteurs qui ont un groupe fonctionnel libre ou un groupe fonctionnel cétone libre, dans le cadre de leur structure moléculaire. C'est le cas du glucose, du galactose, du mannose et du fructose (monosaccharides), ainsi que du lactose et du maltose (disaccharides).
Le saccharose et l'amidon ne réagissent pas avec le réactif de Benedict car ils ont des groupes réducteurs libres. En outre, il existe des composés qui interfèrent avec le test Benedict dans l'urine, donnant une fausse positivité; c'est le cas du salicylate, de la pénicilline, de la streptomycine, de la lévodopa, de l'acide nalidixique et de l'isoniazide.
Il y a des produits chimiques présents dans l'urine qui peuvent réduire la réaction de Benedict; par exemple: créatinine, urate et acide ascorbique.
Composants (modifier)
Les composants du réactif de Benedict sont les suivants: sulfate de cuivre pentahydraté, carbonate de sodium, citrate trisodique et eau distillée..
Sulfate de cuivre pentahydraté, CuSO45HdeuxO, contient du Cudeux+: est le composé qui donne au réactif de Benedict sa couleur bleue. Les sucres réducteurs agissent sur le Cudeux+, produisant sa réduction en Cu+ et la formation d'un précipité d'oxyde cuivreux (CudeuxO) rouge brique.
Le carbonate de sodium génère un milieu alcalin, nécessaire à la réduction du cuivre. Le carbonate de sodium réagit avec l'eau, générant du bicarbonate de sodium et l'ion hydroxyle, OH-, responsable de l'alcalinité du milieu nécessaire au processus de réduction.
Le citrate de sodium forme un complexe avec le cuivre (II) qui l'empêche de subir une réduction en Cu (I) pendant le stockage.
Procédure d'utilisation
5 mL de réactif de Benedict sont placés dans un tube à essai de 20 x 160 mm et 8 gouttes d'urine y sont ajoutées. Le tube à essai est doucement secoué et placé dans un récipient d'eau bouillante pendant 5 à 10 minutes..
Passé ce délai, le tube est retiré du bain d'eau chaude et sa surface est refroidie à l'eau courante pour enfin avoir la lecture du résultat obtenu lors de la réalisation du test Benedict (les couleurs).
La réaction au test de Benoît
La réduction de Cu (II) pendant le test Benedict peut être esquissée comme suit:
RCHO + 2 Cudeux+ (en complexe) + 5 OH- => RCOO- + CudeuxO + 3 HdeuxOU ALORS
RCHO = aldéhyde; RCOO- = (ion carboxylate); CudeuxO = oxyde cuivreux, un précipité rouge brique.
Préparation du réactif de Benoît
173 grammes de citrate de sodium et 100 grammes de carbonate de sodium sont pesés et dissous ensemble dans 800 ml d'eau distillée chaude. Si des traces de substances non dissoutes sont observées, la solution doit être filtrée.
En revanche, 17,3 grammes de sulfate de cuivre pentahydraté sont dissous dans 100 mL d'eau distillée..
Par la suite, les deux solutions aqueuses sont mélangées doucement et continuées sous agitation permanente, jusqu'à 1 000 ml avec de l'eau distillée..
Les références
- Graham Solomons T.W., Craig B. Fryhle. (2011). Chimie organique. Amines. (dixe édition.). Wiley plus.
- Clark J. (2015). Oxydation des aldéhydes et des cétones. Récupéré de: chemguide.co.uk
- Wikipédia. (2020). Le réactif de Benoît. Récupéré de: en.wikipedia.org
- Équipe éditoriale. (9 janvier 2019). Test de Benoît: principe, préparation des réactifs, procédure et interprétation. Récupéré de: Laboratoryinfo.com
- Dr Whitson. (s.f.). Réactif de Benedict: un test pour réduire les sucres. Récupéré de: nku.edu



Personne n'a encore commenté ce post.